1.10: ATP
ATP structuur en functie
In het hart van ATP bevindt zich het nucleotide adenosinemonofosfaat (AMP). Evenals de andere nucleotiden is AMP opgebouwd uit een stikstofhoudende base (een adeninemolecuul) gebonden aan een ribosemolecuul en een enkele fosfaatgroep. De toevoeging van een tweede fosfaatgroep aan dit kernmolecuul leidt tot de vorming van adenosinedifosfaat (ADP); de toevoeging van een derde fosfaatgroep vormt adenosinetrifosfaat (ATP).
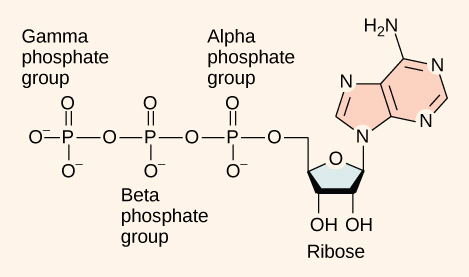
ATP (adenosinetrifosfaat) heeft drie fosfaatgroepen die door hydrolyse kunnen worden verwijderd om ADP (adenosinedifosfaat) of AMP (adenosinemonofosfaat) te vormen. Als er helemaal geen fosfaten zijn, wordt de molecule een “nucleoside” genoemd, in plaats van een “nucleotide”.
De fosforylering of condensatie van fosfaatgroepen op AMP is een endergonisch proces. Daarentegen is de hydrolyse (splitsing door water) van een of twee fosfaatgroepen uit ATP, een proces dat defosforylering wordt genoemd, exergetisch. Waarom? Laten we niet vergeten dat de termen endergonisch en exergonisch verwijzen naar het teken van het verschil in vrije energie van een reactie tussen de producten en de reactanten, ΔG. In dit geval geven we expliciet richting aan de reactie, hetzij in de richting van fosforylering of defosforylering van de nucleotide. In deze fosforyleringsreactie zijn de reactanten het nucleotide en een anorganisch fosfaat, terwijl de producten een gefosforyleerd nucleotide en water zijn. Bij de defosforylering/hydrolyse-reactie zijn de reactanten het gefosforyleerde nucleotide en water, terwijl de producten anorganisch fosfaat en het nucleotide minus één fosfaat zijn.
Gibbs vrije energie is een “toestandsfunctie”, het maakt niet uit hoe de reactie plaatsvindt, je kijkt alleen naar de begin- en eindtoestand. De reactanten ATP en water worden gekarakteriseerd door hun atomaire samenstelling en de soorten bindingen tussen de samenstellende atomen en er kan wat vrije energie geassocieerd worden met elk van de bindingen en hun mogelijke configuraties – net zo voor de producten. De hydrolyse van ATP impliceert het verbreken van de bindingen en hun reconstitutie in een nieuwe ordening. Als we de reactie bekijken vanuit het standpunt van de producten en de reactanten en ons afvragen “hoe kunnen we atomen en bindingen in de reactanten recombineren om de producten te verkrijgen?”, vinden we dat een fosfoanhydride binding tussen een zuurstof en een fosfor moet worden verbroken in het ATP, een binding tussen een zuurstof en een waterstof moet worden verbroken in het water, een binding wordt gevormd tussen het OH (afkomstig van de splitsing van het water) en het fosfor (van het vrijgekomen PO3-2), en een binding moet worden gevormd tussen het H (afkomstig van de splitsing van het water), en de eindzuurstof op de gefosforyleerde nucleotide. De som van de energieveranderingen die gepaard gaan met al deze bindingsherschikkingen (inclusief die welke direct verband houden met water) maakt deze reactie exergetisch. Een soortgelijke analyse kan gemaakt worden met de omgekeerde reactie.
Mogelijke oefening
Gebruik de bovenstaande figuur van ATP en je kennis van hoe een watermolecuul eruit ziet om een figuur te tekenen van de hierboven beschreven reactiestappen: verbreken van fosfoanhydride binding, verbreken van water, en vorming van nieuwe bindingen om ADP en anorganisch fosfaat te vormen. Volg de atomen in verschillende kleuren als dat helpt.
Een andere gedachte-
De beschrijving van bindingsherschikkingen hierboven verklaart niet waarom de scheiding van toevoeging van een derde fosfaatgroep aan ADP om ATP te maken endergonisch is (onder standaardomstandigheden). Als je naar de voor en na structuren kijkt, kun je dan een verklaring bedenken waarom het toevoegen van een fosfaat arbeid vereist (heeft een positieve ∆G), maar het afbreken van een fosfaat een negatieve ∆G vertegenwoordigt?




