Hemoglobin a jeho měření
Normální funkce buněk závisí na neustálém přísunu kyslíku. Při spotřebě kyslíku během buněčného metabolismu vzniká oxid uhličitý.
Zásadní funkcí krve je dodávka kyslíku (O2), přítomného ve vdechovaném vzduchu, z plic ke každé buňce v těle a dodávka oxidu uhličitého (CO2) z buněk do plic, aby byl vyloučen z těla ve vydechovaném vzduchu.
Tyto životně důležité funkce přenosu plynů jsou závislé na bílkovině hemoglobinu obsažené v erytrocytech (červených krvinkách). Každý z 5 × 1010 erytrocytů běžně přítomných v 1 ml krve obsahuje přibližně 280 milionů molekul hemoglobinu.
1. STRUKTURA A FUNKCE HEMOGLOBINU
Molekula hemoglobinu (Hb) je přibližně kulovitá a skládá se ze dvou párů různorodých podjednotek (OBRÁZEK 1).
Každá z podjednotek je složený polypeptidový řetězec (globinová část) s připojenou hemovou skupinou (odvozenou od porfyrinu).
V centru každé hemové skupiny se nachází jeden atom železa ve stavu železa (Fe2+). Hém je tedy metalo-porfyrin, mimochodem zodpovědný za červenou barvu krve.
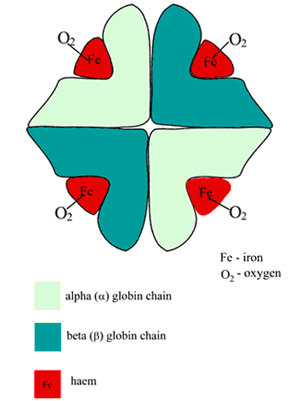
Obrázek 1: Schéma struktury okysličeného hemoglobinu (HbA)
Místo vazby kyslíku v Hb je hemová kapsa přítomná v každém ze čtyř polypeptidových řetězců; jediný atom kyslíku vytváří v každém z těchto míst vratnou vazbu se železem, takže molekula Hb váže čtyři molekuly kyslíku; produktem je oxyhemoglobin (O2Hb).
Přenosová funkce Hb, tj. jeho schopnost „vyzvedávat“ kyslík v plicích a „uvolňovat“ ho do tkáňových buněk, je umožněna drobnými konformačními změnami kvartérní struktury, ke kterým dochází v molekule hemoglobinu a které mění afinitu hemové kapsy ke kyslíku. Hb má dva kvartérní strukturní stavy: deoxy stav (nízká afinita ke kyslíku) a oxy stav (vysoká afinita ke kyslíku).
Řada faktorů prostředí určuje kvartérní stav Hb, a tím i jeho relativní afinitu ke kyslíku. Mikroprostředí v plicích upřednostňuje oxy-kvartérní stav, a proto zde má Hb vysokou afinitu ke kyslíku.
Mikroprostředí tkání naopak vyvolává konformační změnu struktury Hb, která snižuje jeho afinitu ke kyslíku, a umožňuje tak uvolňování kyslíku do buněk tkání.
1.1. HEMOGLOBIN A ELIMINACE DIOXIDU UHLÍKU
Malé množství (až 20 %) CO2 je transportováno z tkání do plic volně vázané na N-koncovou aminokyselinu čtyř globinových polypeptidových jednotek hemoglobinu; produktem tohoto spojení je karbaminohemoglobin. Většina CO2 je však transportována jako hydrogenuhličitan v krevní plazmě.
Přeměna CO2 v erytrocytech na bikarbonát, která je pro tento způsob transportu CO2 nezbytná, vede k produkci vodíkových iontů (H+). Tyto vodíkové ionty jsou pufrovány deoxygenovaným hemoglobinem.
Úloha hemoglobinu při transportu kyslíku a oxidu uhličitého je shrnuta na obr. 2a a 2b.
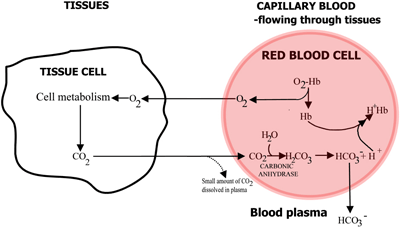
Obrázek 2a: O2 difunduje z krve do tkání, CO2 difunduje z tkání do krve
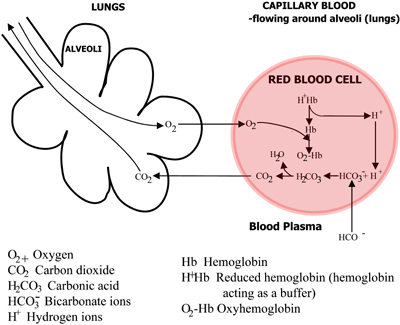
OBRÁZEK 2b: PLÍCE CO2 difunduje z krve do plic, O2 difunduje z plic do krve
V kapilární krvi protékající tkáněmi se kyslík uvolňuje z hemoglobinu a přechází do buněk tkání. Oxid uhličitý difunduje z tkáňových buněk do erytrocytů, kde enzym červených krvinek karboanhydráza umožňuje jeho reakci s vodou za vzniku kyseliny uhličité.
Kyselina uhličitá disociuje na hydrogenuhličitan (který přechází do krevní plazmy) a vodíkové ionty, které se spojí s nyní deoxygenovaným hemoglobinem. Krev proudí do plic a v kapilárách plicních alveolů se výše uvedené cesty obrátí. Bikarbonát vstupuje do erytrocytů a zde se spojuje s vodíkovými ionty uvolněnými z hemoglobinu za vzniku kyseliny uhličité.
Tato se disociuje na oxid uhličitý a vodu. Oxid uhličitý difunduje z krve do plicních sklípků a je vyloučen ve vydechovaném vzduchu. Mezitím kyslík difunduje z plicních sklípků do kapilární krve a spojuje se s hemoglobinem.
1.2. HEMOGLOBIN, KTERÝ NEMŮŽE VÁZAT KYSLÍK
Ačkoli je normálně přítomen pouze ve stopovém množství, existují tři druhy hemoglobinu: methemoglobin (MetHb nebo Hi), sulfhemoglobin (SHb) a karboxyhemoglobin (COHb), které nemohou vázat kyslík.
Jsou tedy funkčně nedostatečné a zvýšené množství některého z těchto druhů hemoglobinu, obvykle v důsledku působení specifických léků nebo toxinů z prostředí, může vážně ohrozit dodávku kyslíku.
Komplexní popis struktury a funkce hemoglobinu je uveden v odkazu .
ctHb, celková koncentrace hemoglobinu je obvykle definována jako součet okysličeného hemoglobinu, deoxygenovaného hemoglobinu, karboxyhemoglobinu a methemoglobinu.
KLINICKÁ VYUŽITELNOST MĚŘENÍ ctHb
Zásadním důvodem měření ctHb je detekce anémie a posouzení její závažnosti.
Anémii lze definovat jako snížení schopnosti krve přenášet kyslík v důsledku snížení počtu erytrocytů a/nebo snížení ctHb, takže anémie je stanovena, pokud je ctHb pod dolní hranicí referenčního (normálního) rozmezí (TABULKA I). Čím nižší je ctHb, tím závažnější je anémie.
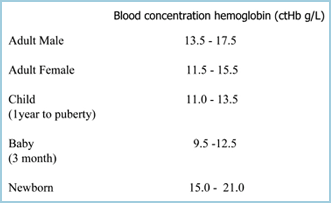
TABULKA I: referenční rozmezí ctHb (Ref 2)
Anémie není chorobná jednotka, spíše důsledek nebo příznak onemocnění. Důvodem, proč je ctHb tak často požadovaným krevním testem, je skutečnost, že anémie je znakem řady patologických stavů, z nichž mnohé jsou relativně časté (tabulka II).
Běžnými příznaky, z nichž většina je nespecifická, jsou: bledost, únava a letargie, dušnost – zejména při námaze, závratě a mdloby, bolesti hlavy, zácpa a zvýšená tepová frekvence, palpitace, tachykardie.

Tabulka II: Některé klinické stavy spojené s anémií
Přítomnost těchto příznaků nevylučuje anémii; mnoho mírně anemických jedinců zůstává bez příznaků, zejména pokud se anémie rozvíjí pomalu.
2.2. POLYCYTÉMIE
Zatímco anémie je charakterizována sníženým ctHb, zvýšený ctHb ukazuje na polycytemii. Polycytemie vzniká jako reakce na jakýkoli fyziologický nebo patologický stav, při kterém krev obsahuje méně kyslíku než normálně (hypoxemie).
Reakce organismu na hypoxemii zahrnuje zvýšenou tvorbu erytrocytů, aby se zvýšila dodávka kyslíku, a v důsledku toho se ctHb zvyšuje. Tato tzv. sekundární polycytemie je součástí fyziologické adaptace na vysokou nadmořskou výšku a může být projevem chronického plicního onemocnění.
Primární polycytemie je mnohem méně časté zhoubné onemocnění kostní dřeně zvané polycytemia vera, které je charakterizováno nekontrolovanou tvorbou všech krevních buněk včetně erytrocytů. Polycytemie, ať už sekundární nebo primární, je obecně mnohem méně častá než anemie.
3.1. HISTORICKÝ PERSPEKTIV
První klinický test měření Hb vymyšlený před více než sto lety spočíval v přidávání kapek destilované vody do odměřeného objemu krve, dokud se její barva neshodovala s barvou umělého barevného standardu.
Pozdější modifikace zahrnovala nejprve nasycení krve uhelným plynem (oxidem uhelnatým), aby se hemoglobin přeměnil na stabilnější karboxyhemoglobin. Moderní hemoglobinometrie se datuje od 50. let 20. století po rozvoji spektrofotometrie a metody hemiglobincyanidu (cynamethemoglobinu).
Následovala adaptace této a dalších metod pro použití v automatických hematologických analyzátorech. V posledních dvou desetiletích se pokrok zaměřil na vývoj metod, které umožňují vyšetření hemoglobinu v místě péče (POCT).
Tato část se zabývá nejprve úvahou o některých metodách používaných v současné době v laboratoři a poté o těch metodách POCT, které se používají mimo laboratoř.
3.2. HEMIGLOBINCYANID – SPEKTROTOMETRICKÁ METODA
Téměř 40 let poté, co byl poprvé přijat jako referenční metoda pro měření hemoglobinu Mezinárodním výborem pro standardizaci v hematologii (ICSH) , zůstává hemiglobincyanidový (HiCN) test doporučenou metodou ICSH, podle které jsou posuzovány a standardizovány všechny nové metody ctHb.
Následující podrobná úvaha odráží jeho přetrvávající význam jako referenční i rutinní laboratorní metody.
3.2.1. Princip zkoušky
Krev se ředí v roztoku obsahujícím ferrikyanid draselný a kyanid draselný. Ferrikyanid draselný oxiduje železo v hemu do železitého stavu za vzniku methemoglobinu, který je kyanidem draselným převeden na hemiglobincyanid (HiCN).
HiCN je stabilní barevný produkt, který má v roztoku absorpční maximum při 540 nm a striktně se řídí Beer-Lambertovým zákonem. Absorbance zředěného vzorku při 540 nm se porovná s absorbancí při stejné vlnové délce standardního roztoku HiCN, jehož ekvivalentní koncentrace hemoglobinu je známa.
Většina derivátů hemoglobinu (oxyhemoglobin, methemoglobin a karboxyhemoglobin, ale ne sulfhemoglobin) se převádí na HiCN, a proto se měří touto metodou.
3.2.1.1. Ředidlo činidla (modifikovaný Drabkinův roztok)
| Fericianid draselný (K3Fe(CN)6) | 200 mg |
| Kyanid draselný (KCN) | 50 mg |
| Dihydrogenfosforečnan draselný (KH2 PO4) | 140 mg |
| Nepř.iontový detergent (např.např. Triton X-100) | 1 ml |
| Výše uvedené se zředí na 1000 ml v destilované vodě |
3.2.1.2. V případě, že se jedná o čisticí prostředek, je třeba jej zředit na 1000 ml. Manuální metoda
25 µl krve se přidá k 5,0 ml činidla, promíchá se a nechá se působit 3 minuty. Absorbance se odečte při vlnové délce 540 nm oproti slepému vzorku činidla. Stejným způsobem se měří absorbance standardu HiCN.
3.2.1.3. ICSH standard HiCN
Hlavní výhodou této metody je, že existuje standardní roztok HiCN vyrobený a přiřazený hodnotě koncentrace podle velmi přesných kritérií stanovených a pravidelně revidovaných Mezinárodní radou pro standardizaci v hematologii (ICSH) .
Tento mezinárodní standardní roztok je primární kalibrací pro komerční standardní roztoky používané v klinických laboratořích po celém světě. Všichni, kdo používají standardizaci HiCN, tak ve skutečnosti používají stejný standard, jehož hodnota byla pečlivě ověřena.
3.2.1.4. Interference
Rušivost způsobená bílkovinami, lipidy a buněčnou hmotou je potenciálním problémem při spektrofotometrickém odhadu jakékoli složky krve, včetně hemoglobinu.
Velké ředění (1:251) vzorku tento problém do značné míry eliminuje, ale falešně zvýšené výsledky ctHb se mohou objevit u pacientů, jejichž koncentrace plazmatických bílkovin je obzvláště vysoká .
Silně lipemické vzorky a vzorky obsahující velmi vysoký počet bílých krvinek (leukocytů) mohou také podobným mechanismem arteficiálně zvýšit ctHb .
3.2.1.5. Výhody HiCN
- Mezinárodní standard – přesný
- Snadno přizpůsobitelný automatickým hematologickým analyzátorům; tudíž reprodukovatelný (nízký SD a CV – v rámci šarže typicky CV
- Dobře zavedený a důkladně prozkoumaný – doporučený ICSH
- Nenákladné činidlo
3.2.1.6. Nevýhody HiCN
- Ruční metoda vyžaduje přesné pipetování a spektrofotometr
- Činidlo (kyanid) nebezpečné
- Výše uvedené omezuje jeho použití mimo laboratoř
- Podléhá interferenci zvýšených lipidů, plazmatických proteinů a počtu leukocytů
- Nerozlišuje ty deriváty hemoglobinu, které nemají schopnost přenášet kyslík (MetHb, COHb, SHb). Může tedy nadhodnocovat schopnost krve přenášet kyslík, pokud jsou přítomny v abnormálním (více než stopovém) množství.
3.3. ALTERNATIVNÍ (BEZCYANIDOVÉ) LABORATORNÍ METODY
Laurylsíran sodný (SLS) je povrchově aktivní látka, která jednak lyzuje erytrocyty, jednak rychle vytváří komplex s uvolněným hemoglobinem. Produkt SLS-MetHb je stabilní po dobu několika hodin a má charakteristické spektrum s maximem absorbance při 539 nm .
Komplex se řídí Beer-Lambertovým zákonem, takže existuje přesná lineární korelace mezi koncentrací Hb a absorbancí SLS-MetHb.
Metoda jednoduše spočívá ve smíchání 25 µl krve s 5,0 ml 2,08 mmol/l roztoku SLS (pufrovaného na pH 7,2) a odečtení absorbance při 539 nm. Bylo prokázáno, že výsledky ctHb metodou SLS-Hb velmi těsně korelují (r = 0,998) s referenční metodou HiCN .
Metoda byla přizpůsobena pro automatické hematologické analyzátory a je stejně spolehlivá z hlediska přesnosti i preciznosti jako automatické metody HiCN . Hlavní výhodou je, že činidlo není toxické. Je také méně náchylná k interferenci lipemií a zvýšenou koncentrací leukocytů .
Dlouhodobá nestabilita SDS-MetHb vylučuje jeho použití jako standardu, takže metoda musí být kalibrována s krví, jejíž ctHb byl stanoven referenční metodou HiCN.
3.3.2. Kalibrační metody Azid-methemoglobinová metoda
Tato metoda je založena na přeměně hemoglobinu na stabilní barevný produkt azid-methemoglobin, který má téměř identické absorpční spektrum jako HiCN .
Reagencie používaná v této metodě je velmi podobná té, která se používá v referenční metodě HiCN, s náhradou azidu sodného za toxičtější kyanid draselný. Stejně jako v metodě HiCN je hemoglobin převeden na methemoglobin pomocí kyanoželeznatanu draselného; azid pak tvoří komplex s methemoglobinem.
Výsledky stanoveníctHb touto metodou jsou srovnatelné s výsledky získanými referenční metodou HiCN; jedná se o přijatelnou alternativní manuální metodu. Výbušný potenciál azidu sodného však brání jeho použití na automatických hematologických analyzátorech . Reakce azid-MetHb byla upravena pro hemoglobinometry POCT.
3.4. Reakce azid-MetHb byla upravena pro hemoglobinometry POCT. MĚŘENÍ ctHb MIMO LABORATORII
Uvažované metody POCT jsou:
- Přenosné hemoglobinometry
- CO-oxymetrie – metoda využívaná v analyzátorech krevních plynů POCT
- Barevná stupnice WHO
3.4.1. Měření ctHb mimo laboratoř
Měření ctHb mimo laboratoř. Přenosné hemoglobinometry
Přenosné hemoglobinometry jako HemoCue-B umožňují přesné stanovení hemoglobinu u lůžka pacienta. Jsou to v podstatě fotometry, které umožňují měření intenzity barvy roztoků.
Mikrokamera na jedno použití, ve které se tato měření provádějí, slouží také jako reakční nádoba. Činidla potřebná jak pro uvolňování Hb z erytrocytů, tak pro přeměnu Hb na stabilní barevný produkt jsou přítomna v sušené formě na stěnách kyvety.
Jediné, co je zapotřebí, je zavedení malého vzorku (obvykle 10 µl) kapilární, venózní nebo arteriální krve do mikrokuvety a vložení mikrokuvety do přístroje.
Přístroj je předem kalibrován z výroby pomocí standardu HiCN a absorbance testovaného roztoku je automaticky převedena na ctHb. Výsledek se zobrazí za méně než minutu.
3.4.1.1. Mezi výhody moderních hemoglobinometrů patří
- Přenosnost
- Napájení z baterie nebo ze sítě, lze použít kdekoli
- Malý objem vzorku (10 µl) získaný vpichem prstu
- Rychlost (výsledek za 60 sekund)
- Snadné použití – bez pipetování
- Minimální nutnost zaškolení nelaboratorního personálu
- Standardizace proti HiCN – výsledky srovnatelné s výsledky získanými v laboratoři
- Korekce na zákal. V tomto ohledu jsou přenosné hemoglobinometry lepší než většina metod ctHb .
Tato technologie byla rozsáhle hodnocena v různých prostředích a většina studií potvrdila přijatelnou přesnost a preciznost ve srovnání s laboratorními metodami.
3.4.1.2. V případě, že se jedná o laboratorní metodu, je možné, že se jedná o metodu, která se používá v různých podmínkách. Nevýhody
Některé studie však vyjádřily obavy , že v rukou nelaboratorního personálu mohou být výsledky méně uspokojivé. Navzdory jednoduchosti obsluhy nejsou tyto přístroje imunní vůči chybám obsluhy a účinné školení je nezbytné.
Existují důkazy, které naznačují, že výsledky získané z kapilárních (prstem píchnutých) vzorků jsou méně přesné než výsledky získané z dobře promíchaných kapilárních nebo žilních vzorků odebraných do lahviček EDTA .
3.4.2. CO-oxymetrie
CO-oxymetr je specializovaný spektrofotometr, jehož název odráží původní použití, které spočívalo v měření COHb a MetHb.
Mnoho moderních analyzátorů krevních plynů má zabudovaný CO-oxymetr, který umožňuje současné stanovení ctHb během analýzy krevních plynů.
Měření ctHb pomocí CO-oxymetrie je založeno na skutečnosti, že hemoglobin a všechny jeho deriváty jsou barevné bílkoviny, které absorbují světlo při specifických vlnových délkách a mají tak charakteristické absorpční spektrum (OBRÁZEK 3).
Beer-Lambertův zákon říká, že absorbance jedné sloučeniny je úměrná koncentraci této sloučeniny. Pokud je známa spektrální charakteristika každé absorbující látky v roztoku, lze odečty absorbance roztoku při více vlnových délkách použít k výpočtu koncentrace každé absorbující látky.
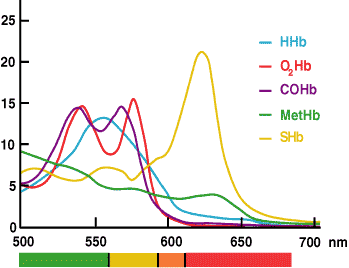
Obr. 3.
V CO-oxymetru se měření absorbance hemolyzovaného vzorku krve při více vlnových délkách v rozsahu, v němž druhy hemoglobinu absorbují světlo (520-620 nm), používají v nainstalovaném softwaru k výpočtu koncentrace každého z derivátů hemoglobinu (HHb, O2Hb, MetHb a COHb). ctHb je vypočtený součet těchto derivátů.
Operátor musí pouze vstříknout dobře promíchaný vzorek arteriální krve do analyzátoru krevních plynů/CO-oxymetru.
Vzorek nebo jeho část se automaticky čerpá do měřicí kyvety CO-oxymetru, kde se – buď chemickým, nebo fyzikálním působením – lyzují erytrocyty a uvolňuje se hemoglobin, který se spektroskopicky snímá, jak je popsáno výše.
Výsledky se zobrazí spolu s výsledky krevních plynů během minuty nebo dvou.
Několik studií potvrdilo, že výsledky ctHb získané pomocí CO-oxymetrie se klinicky významně neliší od výsledků získaných referenčními laboratorními metodami. CO-oxymetrie poskytuje přijatelný způsob urgentního odhadu ctHb v podmínkách intenzivní péče.
3.4.2.1. CO-oxymetrie je přijatelný způsob urgentního odhadu ctHb v podmínkách intenzivní péče. Mezi konkrétní výhody ctHb pomocí CO-oxymetrie patří
- Rychlost analýzy
- Snadnost analýzy
- Malý objem vzorku
- Žádné investiční náklady nebo náklady na spotřební materiál nad rámec nákladů potřebných pro analýzu krevních plynů
- Další parametry (MetHb, COHb, O2Hb) měřeny
- Není ovlivněno vysokým počtem bílých krvinek
3.4.3. Barevná škála hemoglobinu WHO (HCS)
Tento technologicky nenáročný test, vyvinutý pro Světovou zdravotnickou organizaci (WHO), má omezené použití ve vyspělých zemích, ale má obrovský význam pro ekonomicky chudé země rozvojového světa, kde je anémie nejrozšířenější.
V oblastech, kde nejsou k dispozici laboratorní zařízení a kde není dostatek prostředků na financování sofistikovanějších hemoglobinometrů POCT, je to prakticky jediný způsob stanovení ctHb.
Test HCS je založen na jednoduchém principu, že barva krve je funkcí ctHb. Kapka krve se nasaje na papír a její barva se porovná s tabulkou šesti odstínů červené barvy, přičemž každý odstín představuje ekvivalent ctHb: nejsvětlejší 40 g/l a nejtmavší 140 g/l. Ačkoli je v principu velmi jednoduchý, při jeho vývoji bylo použito značného výzkumu a technologií, aby byla zajištěna maximální možná přesnost a preciznost .
Například při konečném výběru papíru pro matrici testovacího proužku byly použity rozsáhlé zkoušky různých papírů a spektrofotometrická analýza krve a směsí barviv, aby se dospělo k co nejtěsnější shodě mezi barvou grafu a barvou krve při každé referenční hodnotě ctHb.
3.4.3.1. Zkoušky a testování Výhody testu HCS
- Snadno se používá – vyžaduje pouze 30 minut školení
- Nevyžaduje žádné vybavení ani energii
- Je rychlý – výsledek do 1 minuty
- Potřebuje pouze vzorek odebraný vpichem do prstu (kapiláry)
- Je velmi levný (asi 0,12 USD za test)
3.4.3.2. Nevýhody testu HCS
Spolehlivé výsledky závisí na přísném dodržování pokynů k testu .
Mezi nejčastější chyby patří:
- Nedostatek nebo nadbytek krve na testovacím proužku
- Odčítání výsledku příliš pozdě (po 2 minutách) nebo příliš brzy (méně než 30 sekund)
- Odčítání výsledku za špatných světelných podmínek
Test HSC má zjevně přirozená omezení . V nejlepším případě může určit, že ctHb vzorku pacienta leží v jednom ze šesti koncentračních rozmezí: 30-50 g/l, 50-70 g/l, 70-90 g/l, 90-110 g/l, 110-130 g/l nebo 130-150 g/l . Přesto je to teoreticky dostačující k identifikaci všech pacientů s výjimkou těch nejmírněji anemických a k orientačnímu určení závažnosti.
Jedna z prvních studií prokázala schopnost testu identifikovat anémii (definovanou jako ctHb
SUMMARY
ctHb je jedním ze dvou parametrů, které se rutinně používají k posouzení schopnosti krve přenášet kyslík, a tím ke stanovení diagnózy anémie a polycytemie.
Alternativní test, nazývaný hematokrit (Hct) nebo objem balených buněk (PCV), byl předmětem předchozího doprovodného článku, kde byl diskutován vztah mezi ctHb a Hct . Tento článek se zaměřil na měření ctHb.
Bylo navrženo mnoho metod, většina z nich je založena na měření barvy hemoglobinu nebo jeho derivátu. Pro tento krátký přehled bylo nevyhnutelně nutné být selektivní. Metody vybrané k diskusi patří k nejčastěji používaným v současnosti.
Při výběru byla snaha zprostředkovat škálu technologií, které se v současné době používají, a způsob jejich použití k uspokojení klinické poptávky po ctHb v prostředí, které sahá od chudých oblastí rozvojového světa, kde má lékařská péče sotva zázemí, až po špičkový svět moderních jednotek intenzivní péče.




