1.10: ATP
ATP struktur og funktion
Hjertet i ATP er nukleotidet adenosinmonofosfat (AMP). Ligesom de andre nukleotider består AMP af en nitrogenbas (et adeninmolekyle) bundet til et ribose-molekyle og en enkelt fosfatgruppe. Tilføjelsen af en anden fosfatgruppe til dette kernemolekyle resulterer i dannelsen af adenosindiphosphat (ADP); tilføjelsen af en tredje fosfatgruppe danner adenosintrifosfat (ATP).
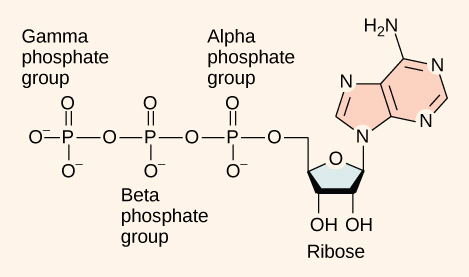
ATP (adenosintrifosfat) har tre fosfatgrupper, der kan fjernes ved hydrolyse for at danne ADP (adenosindiphosphat) eller AMP (adenosinmonofosfat). Hvis der slet ikke er nogen fosfater, kaldes molekylet et “nukleosid” i stedet for et “nukleotid”.
Fosforyleringen eller kondensationen af fosfatgrupper på AMP er en endergonisk proces. Derimod er hydrolyse (spaltning med vand) af en eller to fosfatgrupper fra ATP, en proces, der kaldes dephosphorylering, exergonisk. Hvorfor? Lad os huske på, at udtrykkene endergonisk og exergonisk henviser til fortegnet på forskellen i fri energi for en reaktion mellem produkterne og reaktanterne, ΔG. I dette tilfælde tildeler vi udtrykkeligt reaktionen en retning, enten i retning af fosforylering eller defosforylering af nukleotidet. I denne fosforyleringsreaktion er reaktanterne nukleotidet og et uorganisk fosfat, mens produkterne er et fosforyleret nukleotid og vand. I defosforylerings-/hydrolysereaktionen er reaktanterne det fosforylerede nukleotid og vand, mens produkterne er uorganisk fosfat og nukleotidet minus et fosfat.
Gibbs frie energi er en “tilstandsfunktion”, det er ligegyldigt hvordan reaktionen foregår, man betragter blot begyndelses- og sluttilstanden. Reaktanterne ATP og vand er karakteriseret ved deres atomare opbygning og arten af bindinger mellem de enkelte bestanddelatomer, og der kan knyttes en vis fri energi til hver af bindingerne og deres mulige konfigurationer – det samme gælder for produkterne. Hydrolysen af ATP indebærer, at bindingerne brydes og genopbygges i en ny opstilling. Hvis vi undersøger reaktionen ud fra produkternes og reaktanternes synspunkt og spørger “hvordan kan vi rekombinerer atomer og bindinger i reaktanterne for at få produkterne?”, finder vi, at en fosforanhydridbinding mellem et oxygen og et phosphor skal brydes i ATP, en binding mellem et oxygen og hydrogen brydes i vandet, der dannes en binding mellem OH (der kom fra spaltningen af vand) og phosphor (fra det frigjorte PO3-2), og der skal dannes en binding mellem H (der stammer fra spaltningen af vand) og det terminale oxygen på det fosforylerede nukleotid. Summen af energiforandringer i forbindelse med alle disse omlægninger af bindinger (herunder dem, der er direkte forbundet med vand) gør denne reaktion exergonisk. En lignende analyse kunne foretages med den omvendte reaktion.
Mulig øvelse
Brug figuren af ATP ovenfor og din viden om, hvordan et vandmolekyle ser ud, til at tegne en figur over de reaktionstrin, der er beskrevet ovenfor: brud på fosforanhydridbindingen, brud på vandet og dannelse af nye bindinger for at danne ADP og uorganisk fosfat. Spor atomerne i forskellige farver, hvis det hjælper.
En anden tanke-
Den ovenfor præsenterede beskrivelse af bindingsomlægninger forklarer ikke, hvorfor adskillelsen af tilføjelse af en tredje fosfatgruppe til ADP for at lave ATP er endergonisk (under standardbetingelser). Hvis du ser på før- og efterstrukturerne, kan du så komme med en forklaring på, hvorfor tilføjelse af et fosfat ville kræve arbejde (har en positiv ∆G), men afbrydning af et fosfat repræsenterer en negativ ∆G?




