Hæmoglobin og måling af hæmoglobin
Normal cellefunktion afhænger af en kontinuerlig tilførsel af ilt. Når ilt forbruges under cellestofskiftet, dannes der kuldioxid.
En af blodets hovedfunktioner er levering af ilt (O2), der findes i den indåndede luft, fra lungerne til alle celler i kroppen og levering af kuldioxid (CO2) fra cellerne til lungerne med henblik på udskillelse fra kroppen i udåndingsluften.
Disse vitale gastransportfunktioner er afhængige af proteinet hæmoglobin, der findes i erytrocytter (røde blodlegemer). Hver af de 5 × 1010 erytrocytter, der normalt findes i 1 ml blod, indeholder ca. 280 millioner hæmoglobinmolekyler.
1. HEMOGLOBINETS STRUKTUR OG FUNKTION
Hæmoglobin (Hb)-molekylet er nogenlunde kugleformet og består af to par uensartede underenheder (FIGUR 1).
Hver af underenhederne er en foldet polypeptidkæde (globindelen) med en hæmgruppe (afledt af porphyrin) tilknyttet.
I midten af hver hæmgruppe er der et enkelt jernatom i jernholdig (Fe2+) tilstand. Hæm er således et metallo-porfyrin, som i øvrigt er ansvarlig for den røde farve i blodet.
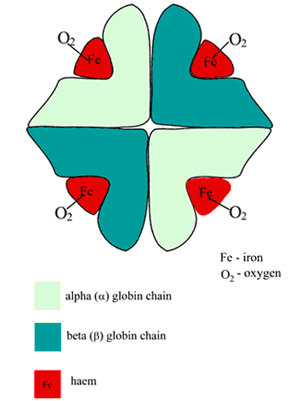
FIGUR 1: Skematisk fremstilling af oxygeneret hæmoglobins (HbA) struktur
Det iltbindende sted i Hb er den hæmlomme, der findes i hver af de fire polypeptidkæder; et enkelt iltatom danner en reversibel binding med jernholdigt jern på hvert af disse steder, så et Hb-molekyle binder fire iltmolekyler; produktet er oxyhæmoglobin (O2Hb).
Hb’s iltleveringsfunktion, dvs. dets evne til at “opsamle” ilt i lungerne og “afgive” det til vævscellerne, er muliggjort ved hjælp af små konformationsændringer i den kvaternære struktur, der forekommer i hæmoglobinmolekylet, og som ændrer hæmlommens affinitet for ilt. Hb har to kvaternære strukturtilstande: deoxytilstanden (lav iltaffinitet) og oxytilstanden (høj iltaffinitet).
En række miljøfaktorer bestemmer Hb’s kvaternære tilstand og dermed dets relative iltaffinitet. Mikromiljøet i lungerne favoriserer den kvaternære oxytilstand, og Hb har derfor høj affinitet for ilt her.
Mikromiljøet i vævene inducerer derimod den konformationsændring i Hb-strukturen, der reducerer dens affinitet for ilt, hvorved ilt kan frigives til vævscellerne.
1.1. HEMOGLOBIN OG KOBONDIOXIDUDDYKNING
En lille mængde (op til 20 %) CO2 transporteres fra vævene til lungerne løst bundet til den N-terminale aminosyre i de fire globin-polypeptid-enheder i hæmoglobin; produktet af denne kombination er carbaminohæmoglobin. Det meste CO2 transporteres dog som bicarbonat i blodplasma.
Den erytrocytternes omdannelse af CO2 til bikarbonat, der er nødvendig for denne CO2-transportform, resulterer i produktion af hydrogenioner (H+). Disse hydrogenioner bliver bufferet af deoxygeneret hæmoglobin.
Hæmoglobins rolle i transporten af ilt og kuldioxid er opsummeret i FIGUR 2a og 2b.
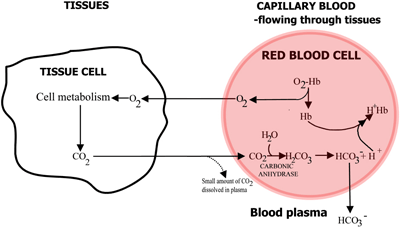
FIGUR 2a: TISSUES O2 diffunderer fra blodet til vævene, CO2 diffunderer fra vævene til blodet
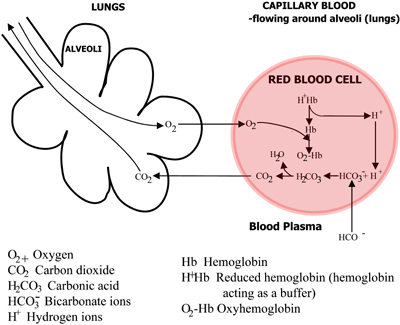
FIGUR 2b: LUNGER CO2 diffunderer fra blodet til lungerne, O2 diffunderer fra lungerne til blodet
I kapillært blod, der strømmer gennem vævene, frigøres ilt fra hæmoglobin og passerer ind i vævscellerne. Kuldioxid diffunderer ud af vævscellerne til erytrocytterne, hvor de røde cellers enzym kulsyreanhydrase muliggør dets reaktion med vand til dannelse af kulsyre.
Kulsyren dissocieres til bicarbonat (som passerer over i blodplasmaet) og hydrogenioner, som kombineres med det nu deoxygenerede hæmoglobin. Blodet strømmer til lungerne, og i kapillærerne i lungealveolerne er de ovennævnte veje omvendt. Bikarbonat kommer ind i erytrocytterne og kombineres her med hydrogenioner, der frigøres fra hæmoglobin, for at danne kulsyre.
Dette dissocieres til kuldioxid og vand. Kuldioxiden diffunderer fra blodet ind i lungernes alveoler og udskilles med udåndingsluften. I mellemtiden diffunderer ilten fra alveolerne til kapillærblodet og kombinerer sig med hæmoglobin.
1.2. HEMOGLOBIN, DER IKKE BINDER OXYGEN
Og selv om det normalt kun findes i spormængder, findes der tre arter af hæmoglobin: methæmoglobin (MetHb eller Hi), sulfhæmoglobin (SHb) og carboxyhæmoglobin (COHb), som ikke kan binde ilt.
De er således funktionelt mangelfulde, og øgede mængder af en af disse hæmoglobinarter, som regel resultatet af eksponering for specifikke lægemidler eller miljøgifte, kan alvorligt kompromittere ilttilførslen.
En omfattende redegørelse for hæmoglobinets struktur og funktion findes i reference .
ctHb, den samlede hæmoglobinkoncentration er typisk defineret som summen af iltet hæmoglobin, deoxygeneret hæmoglobin, carboxyhæmoglobin og methæmoglobin.
CLINISK NØDVENDIGHED AF ctHb-MÅLING
Den vigtigste grund til at måle ctHb er påvisning af anæmi og vurdering af dens sværhedsgrad.
Anemi kan defineres som en reduktion af blodets ilttransporterende evne som følge af en reduktion af antallet af erytrocytter og/eller en reduktion af ctHb, således at der er tale om anæmi, hvis ctHb er under den nedre grænse for referenceområdet (normalområdet) (TABEL I). Jo lavere ctHb, jo mere alvorlig er anæmien.
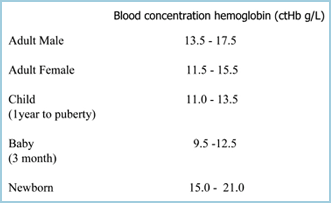
TABEL I: ctHb-referenceintervaller (Ref 2)
Anemi er ikke en sygdomsenhed, men snarere en konsekvens eller et tegn på sygdom. Grunden til, at ctHb er en så hyppigt efterspurgt blodprøve, er, at anæmi er et træk ved en række patologier, hvoraf mange er relativt almindelige (tabel II).
Fælles symptomer, hvoraf de fleste er uspecifikke, omfatter: bleghed, træthed og sløvhed, åndenød – især ved anstrengelse, svimmelhed og besvimelse, hovedpine, forstoppelse og øget pulsfrekvens, hjertebanken, takykardi.

TABEL II: Nogle af de kliniske tilstande, der er forbundet med anæmi
Afværet af disse symptomer udelukker ikke anæmi; mange let anæmiske personer forbliver asymptomatiske, især hvis anæmien har udviklet sig langsomt.
2.2. POLYCYTHEMI
Mens anæmi er karakteriseret ved nedsat ctHb, er et forhøjet ctHb tegn på polycytæmi. Polycytæmi opstår som en reaktion på enhver fysiologisk eller patologisk tilstand, hvor blodet indeholder mindre ilt end normalt (hypoxæmi).
Kroppens reaktion på hypoxæmi omfatter øget produktion af erytrocytter for at øge ilttilførslen, og som følge heraf er ctHb forhøjet. Denne såkaldte sekundære polycytæmi er en del af den fysiologiske tilpasning til stor højde og kan være et træk ved kronisk lungesygdom.
Primær polycytæmi er en langt mindre almindelig malignitet i knoglemarven kaldet polycytæmi vera, som er karakteriseret ved en ukontrolleret produktion af alle blodceller, herunder erytrocytter. Polycytæmi, hvad enten den er sekundær eller primær, er generelt langt mindre almindelig end anæmi.
3.1. HISTORISK PERSPEKTIV
Den første kliniske test af Hb-måling, der blev udtænkt for mere end et århundrede siden, bestod i at tilsætte dråber destilleret vand til et afmålt blodvolumen, indtil dets farve svarede til farven på en kunstig farvet standard.
En senere ændring bestod i først at mætte blodet med kulgas (kulmonoxid) for at omdanne hæmoglobin til det mere stabile carboxyhæmoglobin. Moderne hæmoglobinometri stammer fra 1950’erne efter udviklingen af spektrofotometri og hæmiglobincyanidmetoden (cynamethemoglobin).
Adaptering af denne og andre metoder til brug i automatiserede hæmatologiske analysatorer fulgte. I de seneste to årtier har fremskridtene fokuseret på udvikling af metoder, der muliggør point-of-care-testning (POCT) af hæmoglobin.
Dette afsnit omhandler først en gennemgang af nogle af de metoder, der i øjeblikket anvendes i laboratoriet, og derefter de POCT-metoder, der anvendes uden for laboratoriet.
3.2. HEMIGLOBINCYANID – EN SPECTROPHOTOMETRISK METODE
Næsten 40 år efter at den første gang blev vedtaget som referencemetode til måling af hæmoglobin af Den Internationale Komité for Standardisering i Hæmatologi (ICSH) , er hæmiglobincyanid (HiCN)-testen stadig den af ICSH anbefalede metode, som alle nye ctHb-metoder bedømmes og standardiseres i forhold til.
Den detaljerede gennemgang, der følger, afspejler dens fortsatte betydning både som reference- og rutinelaboratoriemetode.
3.2.1. Testprincip
Blod fortyndes i en opløsning, der indeholder kaliumferricyanid og kaliumcyanid. Kaliumferricyanid oxiderer jernet i hæm til jernstatus for at danne methæmoglobin, som omdannes til hæmiglobincyanid (HiCN) af kaliumcyanid.
HiCN er et stabilt farvet produkt, som i opløsning har et absorbansmaksimum ved 540 nm og følger nøje Beer-Lambert’s lov. Absorbansen af den fortyndede prøve ved 540 nm sammenlignes med absorbansen ved samme bølgelængde af en standard HiCN-opløsning, hvis ækvivalente hæmoglobinkoncentration er kendt.
De fleste hæmoglobinderivater (oxyhæmoglobin, methæmoglobin og carboxyhæmoglobin, men ikke sulfhæmoglobin) omdannes til HiCN og kan derfor måles ved denne metode.
3.2.1.1. Reagensfortynder (modificeret Drabkin-opløsning)
| Kaliumferricyanid (K3Fe(CN)6) | 200 mg |
| Kaliumcyanid (KCN) | 50 mg |
| Dihydrogenkaliumphosphat (KH2 PO4) | 140 mg |
| Non-ionisk vaske- og rengøringsmiddel (f.eks.f.eks. Triton X-100) | 1 mL |
| Overstående fortyndet til 1000 mL i destilleret vand |
3.2.1.2. Manuel metode
25 µl blod tilsættes til 5,0 mL reagens, blandes og stilles i 3 minutter. Absorbansen aflæses ved 540 nm i forhold til en blindprøve af reagens. Absorbansen af HiCN-standarden måles på samme måde.
3.2.1.3. ICSH HiCN-standard
Den store fordel ved denne metode er, at der findes en standard HiCN-opløsning, som fremstilles og tildeles en koncentrationsværdi efter meget præcise kriterier, der er fastlagt og revideret med jævne mellemrum af Det Internationale Råd for Standardisering inden for Hæmatologi (ICSH) .
Denne internationale standardopløsning er det primære kalibreringsmiddel for de kommercielle standardopløsninger, der anvendes i kliniske laboratorier over hele verden. Alle, der anvender HiCN-standardisering, anvender således i praksis den samme standard, hvis værdi er blevet nøje valideret.
3.2.1.4. Interferens
Turbiditet på grund af proteiner, lipider og cellulært materiale er et potentielt problem ved spektrofotometrisk estimering af enhver blodbestanddel, herunder hæmoglobin.
Den store fortynding (1:251) af prøven eliminerer stort set problemet, men fejlagtigt forhøjede ctHb-resultater kan forekomme hos patienter, hvis plasmaproteinkoncentration er særlig høj .
Stærk lipæmiske prøver og prøver, der indeholder et meget stort antal hvide celler (leukocytter), kan også kunstigt forhøje ctHb ved en lignende mekanisme .
3.2.1.5. Fordele ved HiCN
- International standard – nøjagtig
- Let tilpasset automatiserede hæmatologiske analysatorer; dermed reproducerbar (lav SD og CV – inden for batch CV typisk
- Vel etableret og grundigt undersøgt – ICSH anbefalet
- Billigt reagens
3.2.1.6. Ulemper ved HiCN
- Manuel metode kræver nøjagtig pipettering og spektrofotometer
- Reagens (cyanid) farligt
- Overstående begrænser dens anvendelse uden for laboratoriet
- Underlagt interferens fra forhøjede lipider, plasmaproteiner og leukocytantal
- Underskiller ikke de hæmoglobinderivater, der ikke har nogen ilttransporterende evne (MetHb, COHb, SHb). Kan således overvurdere blodets ilttransporterende kapacitet, hvis disse er til stede i unormale (mere end spor) mængder.
3.3. ALTERNATIVE (CYANIDFRI) LABORATORIEMETODER
Natriumlaurylsulfat (SLS) er et overfladeaktivt stof, som både lyserer erytrocytter og hurtigt danner et kompleks med det frigjorte hæmoglobin. Produktet SLS-MetHb er stabilt i nogle få timer og har et karakteristisk spektrum med maksimal absorbans ved 539 nm .
Komplekset adlyder Beer-Lamberts lov, så der er en præcis lineær korrelation mellem Hb-koncentrationen og absorbansen af SLS-MetHb.
Metoden består simpelthen i at blande 25 µL blod med 5,0 mL af en 2,08-mmol/L opløsning af SLS (bufferet til pH 7,2) og at aflæse absorbansen ved 539 nm. Resultaterne af ctHb ved SLS-Hb-metoden har vist sig at korrelere meget tæt (r = 0,998) med HiCN-referencemetoden .
Metoden er blevet tilpasset til automatiserede hæmatologiske analysatorer og er lige så pålidelig med hensyn til både nøjagtighed og præcision som automatiserede HiCN-metoder . En stor fordel er, at reagenset er ikke-toksisk. Den er også mindre tilbøjelig til at blive forstyrret af lipæmi og øget koncentration af leukocytter .
Den langsigtede ustabilitet af SDS-MetHb udelukker dets anvendelse som standard, så metoden skal kalibreres med blod, hvis ctHb er blevet bestemt ved hjælp af HiCN-referencemetoden.
3.3.3.2. Azid-methæmoglobin-metoden
Denne metode er baseret på omdannelse af hæmoglobin til et stabilt farvet produkt azid-methæmoglobin, som har et næsten identisk absorbansspektrum som HiCN .
Det reagens, der anvendes i denne metode, ligner meget det, der anvendes i HiCN-referencemetoden, idet det mere giftige kaliumcyanid erstattes af natriumazid. Som i HiCN-metoden omdannes hæmoglobin til methæmoglobin ved hjælp af kaliumferricyanid; azid danner derefter et kompleks med methæmoglobin.
ctHb-resultater ved denne metode er sammenlignelige med resultater opnået ved reference-HiCN-metoden; dette er en acceptabel alternativ manuel metode. Natriumazids eksplosive potentiale forhindrer imidlertid, at den kan anvendes på automatiserede hæmatologiske analysatorer . Azid-MetHb-reaktionen er blevet tilpasset til POCT-hæmoglobinometre.
3.4. MÅLING AF ctHb UDEN FOR LABORATORIET
De POCT-metoder, der overvejes her, er:
- Bærbare hæmoglobinometre
- CO-oximetri – en metode, der anvendes i POCT-blodgasanalysatorer
- WHO-farveskala
3.4.1. Bærbare hæmoglobinometre
Bærbare hæmoglobinometre som HemoCue-B giver mulighed for nøjagtig bestemmelse af hæmoglobin ved sengekanten. De er i det væsentlige fotometre, der muliggør måling af farveintensiteten af opløsninger.
Mikrokuvetten til engangsbrug, hvori disse målinger foretages, fungerer også som reaktionsbeholder. De reagenser, der er nødvendige for både frigivelse af Hb fra erythrocytterne og omdannelse af Hb til et stabilt farvet produkt, er til stede i tørret form på væggene i kuvetten.
Det eneste, der kræves, er, at en lille prøve (typisk 10 µL) af kapillært, venøst eller arterielt blod føres over i mikrokuvetten og mikrokuvetten indsættes i instrumentet.
Instrumentet er prækalibreret på fabrikken ved hjælp af HiCN-standard, og testopløsningens absorbans konverteres automatisk til ctHb. Resultatet vises på mindre end et minut.
3.4.1.1.1. Fordelene ved moderne hæmoglobinometre er bl.a.
- Portabilitet
- Batteri eller netdrift, kan anvendes hvor som helst
- Lille prøvevolumen (10 µL), der opnås ved fingerprik
- Hurtigt (resultat på 60 sekunder)
- Benyttelsesvenlighed – ingen pipettering
- Minimal uddannelse nødvendig for ikke-laboratoriepersonale
- Standardiseret i forhold til HiCN – resultater sammenlignelige med dem, der opnås i laboratoriet
- Korrektion for turbiditet. I denne henseende er bærbare hæmoglobinometre overlegne i forhold til de fleste ctHb-metoder .
Denne teknologi er blevet grundigt evalueret i en række sammenhænge, og de fleste undersøgelser har bekræftet acceptabel nøjagtighed og præcision sammenlignet med laboratoriemetoder.
3.4.1.2. Ulemper
I nogle undersøgelser er der imidlertid blevet udtrykt bekymring for, at resultaterne kan være mindre tilfredsstillende, hvis de anvendes af personale, der ikke er ansat på laboratorier. På trods af den enkle betjening er disse instrumenter ikke ubeskyttede mod operatørfejl, og det er vigtigt med effektiv uddannelse.
Der er tegn på, at resultater fra kapillærprøver (fingerstikprøver) er mindre præcise end resultater fra velblandede kapillære eller venøse prøver, der er opsamlet i EDTA-flasker.
3.4.2. CO-oximetri
Et CO-oximeter er et specialiseret spektrofotometer, hvis navn afspejler den oprindelige anvendelse, som var til måling af COHb og MetHb.
Mange moderne blodgasanalysatorer har et indbygget CO-oximeter, hvilket giver mulighed for samtidig estimering af ctHb under blodgasanalysen.
Måling af ctHb ved CO-oximetri er baseret på det faktum, at hæmoglobin og alle dets derivater er farvede proteiner, som absorberer lys ved bestemte bølgelængder og dermed har et karakteristisk absorbansspektrum (FIGUR 3).
Beer-Lamberts lov foreskriver, at absorbansen af en enkelt forbindelse er proportional med koncentrationen af denne forbindelse. Hvis spektralkarakteristikken for hvert absorberende stof i en opløsning er kendt, kan absorbansaflæsninger af opløsningen ved flere bølgelængder anvendes til at beregne koncentrationen af hvert absorberende stof.
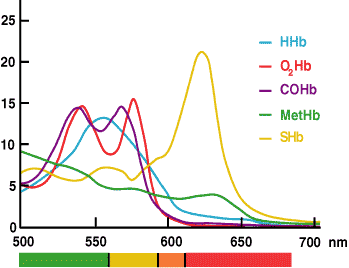
FIGUR 3.
I CO-oximeteret anvendes absorbansmålinger af en hæmolyseret blodprøve ved flere bølgelængder i det område, hvor hæmoglobinarter absorberer lys (520-620 nm), af den installerede software til at beregne koncentrationen af hvert af hæmoglobinderivaterne (HHb, O2Hb, MetHb og COHb). ctHb er den beregnede sum af disse derivater.
Det eneste, der kræves af operatøren, er indsprøjtning af en godt blandet arteriel blodprøve i blodgasanalysatoren/CO-oximeteret.
Proven eller en del af den pumpes automatisk til CO-oximeterets målekuvette, hvor erythrocytterne – enten ved kemisk eller fysisk påvirkning – lyseres for at frigøre hæmoglobin, der spektroskopisk scannes som beskrevet ovenfor.
Resultaterne vises sammen med blodgasresultaterne inden for et minut eller to.
Flere undersøgelser har bekræftet, at ctHb-resultater opnået ved CO-oximetri ikke er klinisk signifikant forskellige fra dem, der er afledt af referencelaboratoriemetoder. CO-oximetri er et acceptabelt middel til hurtig estimering af ctHb på intensivafdelingen.
3.4.2.1. De særlige fordele ved ctHb ved CO-oximetri omfatter
- Speed of analysis
- Ease of analysis
- Små prøvevolumen
- Ingen kapital- eller forbrugsmaterialeomkostninger ud over de omkostninger, der er nødvendige for blodgasanalyse
- Tilføjelige parametre (MetHb, COHb, O2Hb) måles
- Indvirker ikke på højt antal hvide celler
3.4.3. WHO’s hæmoglobinfarveskala (HCS)
Denne lavteknologiske test, der er udviklet for Verdenssundhedsorganisationen (WHO), har begrænset anvendelse i de udviklede lande, men har stor betydning for de økonomisk dårligt stillede lande i udviklingslandene, hvor anæmi er mest udbredt.
I områder, hvor der ikke er laboratoriefaciliteter og utilstrækkelige ressourcer til at finansiere mere sofistikerede POCT-hæmoglobinometre, er det stort set den eneste måde at bestemme ctHb på.
HCS-testen er baseret på det enkle princip, at blodets farve er en funktion af ctHb. En dråbe blod absorberes på papir, og dens farve sammenlignes med et skema med seks røde nuancer, hvor hver nuance repræsenterer et tilsvarende ctHb: den lyseste 40 g/L og den mørkeste 140 g/L. Selv om det i princippet er meget enkelt, er der anvendt betydelig forskning og teknologi under udviklingen for at sikre størst mulig nøjagtighed og præcision .
F.eks. blev der foretaget omfattende forsøg med forskellige papirtyper til grund for det endelige valg af papir til teststrimmematrixen, og der blev anvendt spektrofotometrisk analyse af blod og farvestofblandinger for at opnå den tættest mulige overensstemmelse mellem diagramfarven og blodfarven ved hvert reference-ctHb.
3.4.3.1. Fordele ved HCS-testen
- Er nem at bruge – kræver kun 30 minutters oplæring
- Kræver intet udstyr eller strøm
- Er hurtig – resultat inden for 1 minut
- Kræver kun en fingerprikprøve (kapillærprøve)
- Er meget billig (ca. 0,12 USD pr. test)
3.4.3.3.2. Ulemper ved HCS-testen
Pålidelige resultater afhænger af, at testinstruktionerne overholdes nøje .
Hyppige fejl omfatter:
- Udstrækkeligt eller for meget blod på teststrimlen
- Aflæsning af resultatet for sent (over 2 minutter) eller for tidligt (mindre end 30 sceonds)
- Aflæsning af resultatet under dårlige lysforhold
HSC-testen har klart iboende begrænsninger . Den kan i bedste fald bestemme, at ctHb i en patientprøve ligger inden for et af seks koncentrationsintervaller: 30-50 g/L, 50-70 g/L, 70-90 g/L, 90-110 g/L, 110-130 g/L eller 130-150 g/L. Alligevel er dette teoretisk set tilstrækkeligt til at identificere alle undtagen de mest let anæmiske patienter og give en indikation af sværhedsgraden.
En tidlig undersøgelse viste testens evne til at identificere anæmi (defineret som ctHb
SUMMARY
ctHb er en af to parametre, der rutinemæssigt anvendes til at vurdere blodets ilttransporterende kapacitet og dermed stille en diagnose af anæmi og polycytæmi.
Den alternative test, kaldet hæmatokrit (Hct) eller Packed Cell Volume (PCV), var emnet for en tidligere ledsagende artikel, hvor forholdet mellem ctHb og Hct blev diskuteret . Fokus i denne artikel har været måling af ctHb.
Der er blevet udtænkt talrige metoder, hvoraf de fleste er baseret på måling af farven på hæmoglobin eller et derivat af hæmoglobin. I denne korte gennemgang har det uundgåeligt været nødvendigt at være selektivt. De metoder, der er valgt til diskussion, er blandt de mest almindeligt anvendte i dag.
I forbindelse med udvælgelsen er der gjort et forsøg på at formidle den vifte af teknologier, der i øjeblikket anvendes, og hvordan disse anvendes til at opfylde den kliniske efterspørgsel efter ctHb i omgivelser, der spænder fra fattige områder i udviklingslandene, hvor lægehjælp knap nok har fodfæste, til den moderne intensivafdelings højteknologiske verden.




