CNIO, neue Schritte für eine künftige Therapie gegen altersbedingte Lungenfibrose
Die Gruppe Telomere und Telomerase des Spanischen Nationalen Krebsforschungszentrums (CNIO) hat eine wirksame Therapie bei Mäusen mit altersbedingter Fibrose nachgewiesen, nachdem sie die gleiche Heilung für Mäuse mit Fibrose aufgrund genetischer Fehler entwickelt hatte. In der Studie, die im Journal of Cell Biology veröffentlicht wurde, wird eine Gentherapie entwickelt, die die körpereigene Produktion von Telomerase aktiviert.
Diopathische Lungenfibrose ist eine unbehandelte und potenziell tödliche Krankheit, die mit bestimmten Mutationen und auch mit dem Alter zusammenhängt.
Telomerase ist das Enzym, das für die Reparatur der Enden der Chromosomen verantwortlich ist, wo sich die Telomere befinden. Die Therapie war bei Tieren hochwirksam, und es wurden keine Nebenwirkungen beobachtet. Dies erklärte die Studienleiterin Maria Blaso.
„Wenn wir an den Menschen denken, deutet unser Ergebnis auf die Möglichkeit hin, eine Therapie zu entwickeln, die in der Lage ist, die Entwicklung der altersbedingten Lungenfibrose bei jedem Patienten zu verhindern“, sagt Blasco.
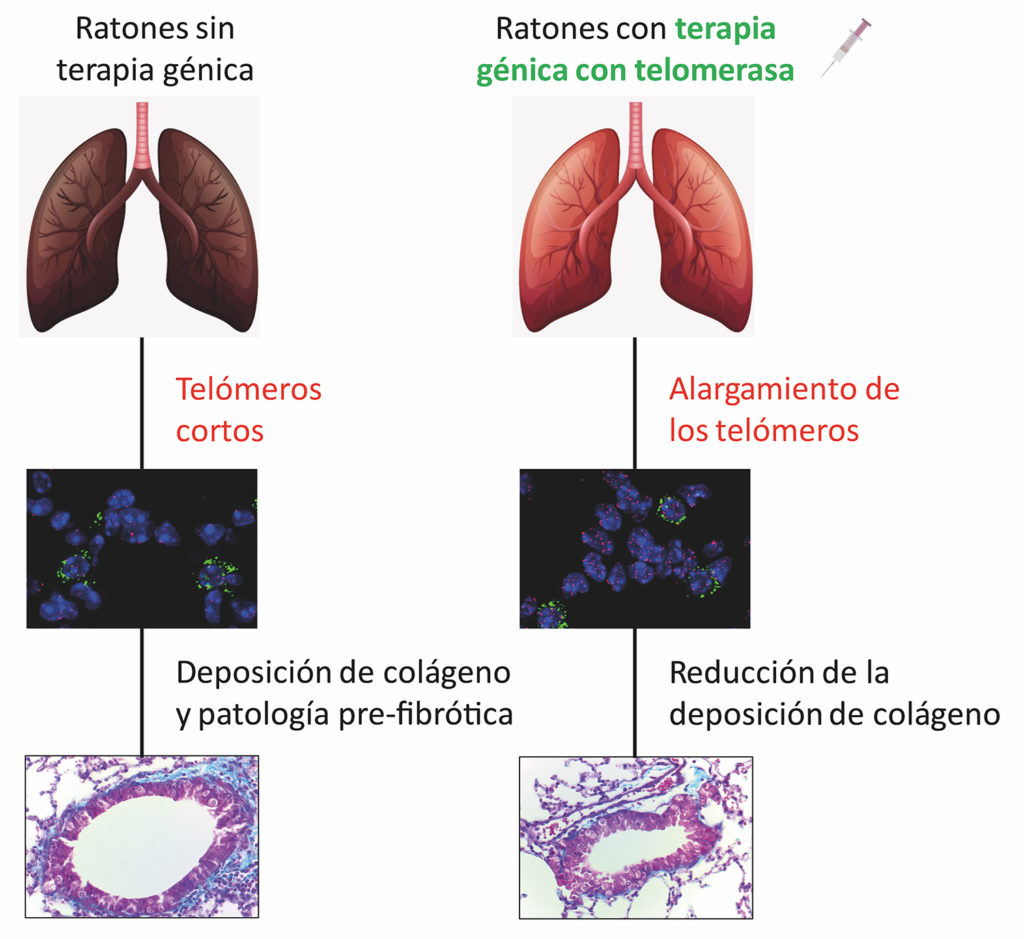
Telomerdysfunktion am Ursprung der Fibrose
Lungenfibrose betrifft etwa 8.000 Menschen in Spanien. Bei dieser Krankheit vernarbt das Lungengewebe und wird steif, was zu einem fortschreitenden Verlust der Atemkapazität führt.
Die Ursache wird auf eine Kombination aus Genetik und Umwelt zurückgeführt: Umweltgifte spielen eine wichtige Rolle, aber damit sich die Krankheit manifestieren kann, muss es entweder eine genetische Ursache oder eine mit dem Alter verbundene Alterung geben.
Die CNIO-Gruppe hatte bereits in früheren Studien nachgewiesen, dass diese genetische Ursache in einer Fehlfunktion der Telomere liegt. Telomere sind Strukturen, die wie Kappen die Integrität der in allen Zellen vorhandenen Chromosomen schützen.
Im Jahr 2015 schufen sie ein Tiermodell für Lungenfibrose, eine Maus, der das Telomerase-Gen fehlt. Bei diesen Tieren sterben die Zellen, die für die Regeneration des Lungengewebes zuständig sind, die so genannten alveolären Pneumozyten vom Typ II, schließlich aufgrund einer Telomerdysfunktion ab. Die Maus entwickelt daraufhin eine aggressive Fibrose, weil sich das Epithel der Lunge nicht regelmäßig erneuern kann. Durch diese periodische Regeneration bleibt das Gewebe gesund und frei von Schäden durch Umweltgifte.
Altersbedingte Fibrose
Dieses Tiermodell ohne Telomerase-Gen reproduziert gut, was bei Patienten geschieht, deren Fibrose auf Mutationen zurückzuführen ist, die die Telomere betreffen. Aber diese Menschen sind in der Minderheit. Bei der überwiegenden Mehrheit der Patienten deutet nichts auf eine bestimmte Mutation hin, aber es gibt einen Faktor, der allen gemeinsam ist: das hohe Alter.

Telomere können auch durch den bloßen Prozess des Alterns ihre Funktion verlieren. Die Untersuchung, wie dies geschieht, ist ein Gebiet, das international von Blascos Gruppe geleitet wird.
Telomere sind Proteinkappen an den Enden der Chromosomen, die bei jeder Zellteilung ein wenig kürzer werden. Nach vielen Zellteilungen im Laufe des Lebens eines Organismus werden sie daher irgendwann so kurz, dass sie ihre Fähigkeit, die Chromosomen zu schützen, verlieren. Die Zelle interpretiert dies als Fehler und stellt ihre Teilung ein, so dass sich das Gewebe nicht regeneriert.
In der jetzt veröffentlichten Arbeit haben die Forscher gezeigt, dass diese altersbedingte Telomerdysfunktion tatsächlich in den regenerativen Zellen des Lungengewebes, den Typ-II-Pneumozyten, auftritt. Auf diese Weise finden sie die molekulare Ursache für die Verbindung zwischen Alterung und Lungenfibrose, die in der Klinik so deutlich ist.
Verlust des Lungenschmierstoffs
Die Autoren erklären, dass „eine der Errungenschaften der neuen Arbeit darin besteht, die Auswirkungen der Alterung auf das Lungengewebe in allen Einzelheiten zu beschreiben“. „Eine davon ergibt sich direkt aus der Tatsache, dass die Typ-II-Pneumozyten ihre Arbeit einstellen“, sagt Sergio Piñeiro, Erstautor der Studie.
Diese Zellen regenerieren nicht nur Gewebe, sondern stellen auch eine Flüssigkeit her und geben sie ab, die die mechanische Arbeit der Lunge erleichtert, das so genannte pulmonale Surfactant.
„Das Lungengewebe muss sich bei jedem Atemzug öffnen, sechs- bis zehnmal pro Minute, was aus physikalischer Sicht eine große Anstrengung bedeutet“, erklärt Jesús Pérez-Gil, Experte an der Complutense-Universität Madrid.
Gil, der an der Studie mitgewirkt hat und dessen Team Experte auf diesem Gebiet ist, weist darauf hin, dass „das Lungensurfactant wichtig ist, um das Gewebe zu schmieren, damit es sich mit minimalem Aufwand öffnen und schließen kann und elastisch bleibt“.
„Wenn sich die Typ-II-Pneumozyten nicht regenerieren, regeneriert sich auch das Surfactant nicht, und das trägt dazu bei, dass die Lunge zunehmend starr und fibrotisch wird“
Universität Complutense Madrid, Jesús Pérez-Gil
In dieser Arbeit „haben wir einen sehr klaren Zusammenhang zwischen dem Telomer-Status der Typ-II-Pneumozyten, der Surfactant-Produktion in der Lunge und der Entwicklung der Fibrose bei Tieren beobachtet“, fügt Pérez-Gil hinzu. „In dieser Zusammenarbeit befassen wir uns auf kombinierte Weise mit den Auswirkungen auf molekularer Ebene, auf die Telomere, mit den biologischen und physikalischen Veränderungen in Zellen und Geweben und mit den Folgen für die Gesundheit des Tieres, des gesamten Organismus.“
Eine Therapie für alle Arten von Fibrose
Im Jahr 2018 entwickelte die CNIO-Gruppe eine Gentherapie, die in der Lage ist, die Fibrose zu heilen, die ihre Mäuse ohne das Telomerase-Gen entwickelten. Die Behandlung basiert darauf, diese genetische Veränderung rückgängig zu machen und die Telomerase-Synthese in den Mäusen vorübergehend zu aktivieren.

Mäusen wird intravenös ein Virus verabreicht, dessen einzige Funktion darin besteht, das Telomerase-Gen in die Gewebe zu tragen. Die Wirkung ist nur von kurzer Dauer, reicht aber aus, um bei den Typ-II-Pneumozyten lange Telomere nachwachsen zu lassen und das Lungengewebe zu regenerieren.
Jetzt haben sie die gleiche Therapie bei Mäusen angewandt, die einfach nur altern. Und es funktioniert auch. „Die Behandlung mit Telomerase-aktivierender Gentherapie verhinderte den Beginn der Fibrose bei allen Mäusen, auch bei denen, die keine genetische Veränderung aufwiesen, aber physiologisch alterten“, erklärt Blasco.
Damit wird die Möglichkeit einer Heilung der Lungenfibrose auf fast alle Fälle von Fibrose ausgedehnt, wie die Forscher in ihrem Artikel schlussfolgern: „Diese Ergebnisse helfen, die Bedeutung der Telomerase für künftige therapeutische Strategien gegen idiopathische Lungenfibrose zu erklären.
Die Studie wurde vom spanischen Ministerium für Wissenschaft, Innovation und Universitäten, dem Carlos III Institut für Gesundheit, der Gemeinschaft Madrid, der Botín Stiftung und Banco Santander über Santander Universitäten und World Cancer Research finanziert.
Die Studie wurde vom spanischen Ministerium für Wissenschaft, Innovation und Universitäten, dem Carlos III Institut für Gesundheit, der Gemeinschaft Madrid, der Botín Stiftung und Banco Santander über Santander Universitäten und World Cancer Research finanziert.




