Metformine-geïnduceerde melk acidose: nut van het meten van niveaus en therapie met hoge-flux hemodialyse | Nefrología
To the Editor,
Lactische acidose bij metformine behandelde diabetes mellitus patiënten is een zeer zeldzame complicatie, met een hoog sterftecijfer en is vaak geassocieerd met een onderliggende aandoening, die op zichzelf deze zeer ernstige hydro-elektrolytische onevenwichtigheid zou kunnen veroorzaken. Metformine is een veelgebruikt oraal antidiabeticum, dat door actieve tubulaire secretie wordt geëlimineerd, maar zich bij patiënten met nierfalen ophoopt.1 Klinisch ontwikkelt metforminegeassocieerde melkzuurocidose (MALA) zich abrupt en gaat gepaard met overademing, buikpijn, sufheid en coma. Abnormale laboratoriumindicatoren voor MALA zijn een hoge anion gap, base-overmaat in het arteriële bloedgas en hoge plasma lactaatspiegels (prognostische waarde) en metformine plasmaspiegels. Het monitoren van de lactaat- en metforminespiegels is een zeer nuttige manier om de evolutie en de mogelijke wijzigingen in de behandeling te evalueren. De behandeling van MALA is omstreden; het gebruik van bicarbonaat is gebruikelijk, hoewel er geen wetenschappelijk bewijs is dat dit met een betere prognose in verband brengt. De geringe binding van metformine aan plasma-eiwitten maakt het mogelijk hemodialyse-technieken met bicarbonaatoplossingen toe te passen wanneer een overdosis is toegediend. Deze techniek is doeltreffend gebleken om plasma-metformine te elimineren en maakt het tevens mogelijk de acidose te corrigeren.2,3 Dialyse lijkt een belangrijke bijdrage te leveren aan de behandeling van deze ernstige pathologie en de resultaten te verbeteren wanneer MALA gepaard gaat met acuut nierfalen.4 Als we MALA zouden vergelijken met ernstige melkzuurvergiftiging die elders is gelokaliseerd, is de prognose van MALA aanzienlijk beter. De diagnose ervan moet worden overwogen bij alle metformine behandelde patiënten die zich presenteren met melkzuurocidose.5
Eenentachtigjarige patiënt met hoge bloeddruk, dyslipidemie, diabetes type 2 en gedilateerde myocardiopathie (ejectiefractie 30%). Gebruikelijke behandeling: telmisartan, torsemide, metformine 850mg/8hrs, atorvastatine, carvedilol en omeprazol. Ze kwam op de spoedeisende hulp met diarree met slijm en bloed, en braken, dat al een week aanhield, evenals oligoanurie gedurende 24 uur.
Lichamelijk onderzoek: bloeddruk: 120/70mm Hg, hartslag (HR): 95bpm, temperatuur (T): 36ºC.
Neurologisch onderzoek: Glasgow score 12, tijd/ruimte desoriëntatie en bradypsychia, zonder tekenen van focussering. Ritmische hartslag, geen geruis, gekraak tot in het middenveld. Geen tekenen in de buik en onderste ledematen.
Biochemische tests toonden aan: hemoglobine: 11,7g/dl; leukocyten: 18 030 (78,9% neutrofielen); bloedplaatjes: 307 000; glucose: 68mg/dl; ureum: 133mg/dl; creatinine: 6,89mg/dl; natrium: 134mEq/l; kalium: 4.4mEq/l; pH: 6.89; pCO2: 29mm Hg; bicarbonaat: 6,9mmol/l; ionisch calcium: 3,85mg/dl; anion gap: 28. Normale stolling. Urine: pH: 6; creatinine: 71mg/dl; proteïnurie: 400mg/dl; 100 rode bloedcellen/veld; 60 leukocyten/veld; positieve ketonlichamen en negatieve drugs (benzodiazepinen, barbituraten). Normale abdominale echografie met symmetrische nieren (12cm); goede corticomedullary delimitatie.
Electrocardiogram: linker bundeltakblok (LBBB) bij 93bpm. Röntgenfoto van de borst: cardiomegalie en normale craniale computergestuurde tomografie (CT). Ze werd gediagnosticeerd met stadium 2 chronisch nierfalen secundair aan acute prerenale hypertensieve en diabetische nefropathie in een tubulaire necrose fase en hoge anion gap lactische metabole acidose. Repletiebehandeling met fysiologische zoutoplossing (PSS) van 0,9%, en dextroseoplossing van 5%, lusdiuretica en 1M natriumbicarbonaat. Ondanks deze behandeling bleef ze anurie houden en ging haar cognitieve functie verder achteruit. Daarom besloten wij haar eerste hemodialyse-sessie van 2 uur zonder ultrafiltratie uit te voeren. Na bevestiging van hyperlactacidemie (10,7mmol/l), hoge metforminespiegels (34,4mg/l; therapeutische niveaus 1,3-5) en symptomen van hartoverbelasting met hemodynamische stoornis, besloten wij dialyse uit te voeren gedurende vier dagen en vervolgens om de 48 uur totdat een constante lactaatdaling en niet-toxische metforminespiegels werden bereikt (tabel 1). Ze kreeg in totaal 7 sessies. Ze kreeg empirische antibiotische therapie met cefalosporine van de derde generatie; de urine- en feceskweken waren negatief.
Ze werd ontslagen zonder neurologische en renale symptomen, met creatinine op 1,6mg/dl en de volgende behandeling: carvedilol in een dosering van 6.25mg/24uur, repaglinide in een dosering van 1,5mg/8uur, telmisartan, atorvastatine, torsemide in een dosering van 10mg/24uur en omeprazol in een dosering van 20mg/24uur.
Ze presenteert zich momenteel met 1,26mg/dl creatinine en is neurologisch stabiel.
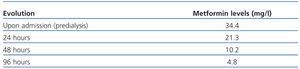
Tabel 1. Ontwikkeling van de metforminespiegels




