Hemoglobina e sua medida
A função celular normal depende de um suprimento contínuo de oxigênio. Como o oxigênio é consumido durante o metabolismo celular, o dióxido de carbono é produzido.
Uma função principal do sangue é o fornecimento de oxigénio (O2), presente no ar inspirado, dos pulmões para cada célula do corpo e fornecimento de dióxido de carbono (CO2) das células para os pulmões, para eliminação do corpo em ar expirado.
Estas funções vitais de transporte de gases dependem da hemoglobina proteica contida nos eritrócitos (glóbulos vermelhos do sangue). Cada um dos 5 × 1010 eritrócitos normalmente presentes em 1 mL de sangue contém cerca de 280 milhões de moléculas de hemoglobina.
1. ESTRUTURA E FUNÇÃO HEMOGLOBINA
A molécula de hemoglobina (Hb) é aproximadamente esférica e compreende dois pares de subunidades diferentes (FIGURA 1).
Cada uma das subunidades é uma cadeia de polipeptídeos dobrada (a porção globina) com um grupo heme (derivado da porfirina) ligado.
No centro de cada grupo heme está um único átomo de ferro no estado ferroso (Fe2+). Assim, heme é um metallo-porfirina, incidentalmente responsável pela cor vermelha do sangue.
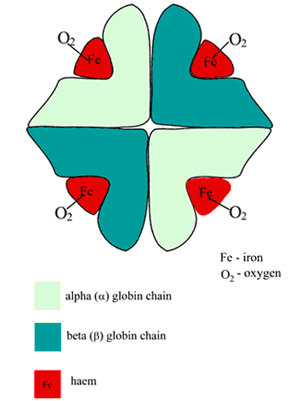
FIGURA 1: Esquema da estrutura da hemoglobina oxigenada (HbA)
O local de ligação do Hb ao oxigénio é a bolsa de heme presente em cada uma das quatro cadeias de polipeptídeos; um único átomo de oxigénio forma uma ligação reversível com o ferro ferroso em cada um destes locais, pelo que uma molécula de Hb liga quatro moléculas de oxigénio; o produto é a oxihemoglobina (O2Hb).
A função de fornecimento de oxigênio da Hb, ou seja, sua capacidade de “pegar” oxigênio nos pulmões e “liberá-lo” para as células teciduais é possibilitada por pequenas mudanças conformacionais na estrutura quaternária que ocorrem na molécula de hemoglobina e que alteram a afinidade da bolsa de heme para oxigênio. Hb tem dois estados estruturais quaternários: o estado de deoxia (baixa afinidade com o oxigênio) e o estado oxigenado (alta afinidade com o oxigênio).
Uma gama de factores ambientais determinam o estado quaternário de Hb e portanto a sua relativa afinidade com o oxigénio. O microambiente nos pulmões favorece o estado oxiquaternário e, portanto, a Hb tem alta afinidade com o oxigênio aqui.
Por contraste, o microambiente dos tecidos induz a mudança conformacional na estrutura da hemoglobina que reduz sua afinidade com o oxigênio, permitindo assim que o oxigênio seja liberado para as células dos tecidos.
1.1. ELIMINAÇÃO DE HEMOGLOBINA E DIÓXIDO DE CARBONO
Uma pequena quantidade (até 20%) de CO2 é transportada dos tecidos para os pulmões soltamente ligada ao aminoácido N-terminal das quatro unidades de polipeptídeos de globina da hemoglobina; o produto desta combinação é a carbaminohemoglobina. No entanto, a maioria do CO2 é transportada como bicarbonato no plasma sanguíneo.
A conversão eritrócita de CO2 em bicarbonato, necessária para este modo de transporte de CO2, resulta na produção de iões de hidrogénio (H+). Estes íons de hidrogênio são tamponados pela hemoglobina desoxigenada.
O papel da hemoglobina no transporte de oxigênio e dióxido de carbono está resumido em FIGURAS 2a e 2b.
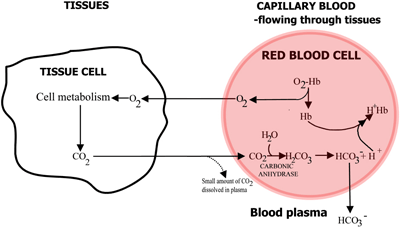
FIGURA 2a: TISSOS O2 difunde-se do sangue para os tecidos, CO2 difunde-se dos tecidos para o sangue
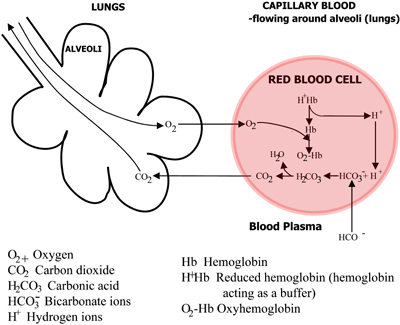
FIGURA 2b: LUNGS O CO2 difunde-se do sangue para os pulmões, o O2 difunde-se dos pulmões para o sangue
>Em sangue capilar que flui através dos tecidos, o oxigénio é libertado da hemoglobina e passa para as células tecidulares. O dióxido de carbono difunde-se das células tecidulares para os eritrócitos, onde a enzima anidrase carbónica de células vermelhas permite a sua reacção com a água para formar ácido carbónico.
O ácido carbónico dissocia-se do bicarbonato (que passa para o plasma sanguíneo) e dos iões de hidrogénio, que se combinam com a agora desoxigenada hemoglobina. O sangue flui para os pulmões, e nos capilares dos alvéolos pulmonares as vias acima são invertidas. O bicarbonato entra nos eritrócitos e aqui combina-se com íons hidrogênio, liberados da hemoglobina, para formar ácido carbônico.
>
Isso dissocia-se do dióxido de carbono e da água. O dióxido de carbono se difunde do sangue para os alvéolos dos pulmões e é eliminado no ar expirado. Entretanto, o oxigênio se difunde dos alvéolos para o sangue capilar e combina com a hemoglobina.
1.2. HEMOGLOBINA QUE NÃO PODE ACOMPANHAR OXIGÉNIO
Embora normalmente presente apenas em quantidades vestigiais, existem três espécies de hemoglobina: metemoglobina (MetHb ou Hi), sulfhemoglobina (SHb) e carboxihemoglobina (COHb) que não consegue ligar o oxigénio.
São, portanto, funcionalmente deficientes, e quantidades aumentadas de qualquer uma dessas espécies de hemoglobina, geralmente resultado da exposição a drogas específicas ou toxinas ambientais, podem comprometer seriamente o fornecimento de oxigênio.
Uma descrição abrangente da estrutura e função da hemoglobina é fornecida na referência .
ctHb, a concentração total de hemoglobina é tipicamente definida como a soma de hemoglobina oxigenada, hemoglobina desoxigenada, carboxihemoglobina e metemoglobina.
UTILIDADE CLÍNICA DA MEDIÇÃO da ctHb
A principal razão para medir a ctHb é a detecção de anemia e avaliação de sua gravidade.
Anemia pode ser definida como uma redução na capacidade de transporte de oxigênio do sangue devido a uma redução no número de eritrócitos e/ou uma redução na ctHb, de modo que a anemia é estabelecida se a ctHb estiver abaixo do limite inferior da faixa de referência (normal) (TABELA I). Quanto menor a ctHb, mais grave é a anemia.
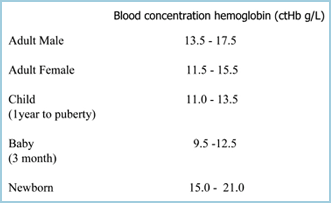
>TABLE I: faixas de referência da ctHb (Ref 2)
Anemia não é uma entidade da doença, mas uma consequência ou sinal da doença. A razão pela qual a ctHb é um exame de sangue tão frequentemente solicitado é que a anemia é uma característica de uma série de patologias, muitas das quais são relativamente comuns (Tabela II).
Sintomas comuns, a maioria dos quais não específicos, incluem: palidez, cansaço e letargia, falta de ar – particularmente em esforço, tonturas e desmaios, dores de cabeça, constipação e aumento da frequência cardíaca, palpitações, taquicardia.

TÁBULO II: Algumas das condições clínicas associadas à anemia
A ausência desses sintomas não impede a anemia; muitos indivíduos levemente anêmicos permanecem assintomáticos, principalmente se a anemia se desenvolveu lentamente.
2.2. POLICITEMIA
Apesar de a anemia ser caracterizada por ctHb reduzida, uma ctHb elevada indica policitemia. A policitemia surge como uma resposta a qualquer condição fisiológica ou patológica na qual o sangue contém menos oxigénio do que o normal (hipoxemia).
A resposta do corpo à hipoxemia inclui o aumento da produção de eritrócitos para aumentar o fornecimento de oxigénio, e como consequência a ctHb é elevada. Essa chamada policitemia secundária é parte da adaptação fisiológica à altitude elevada e pode ser uma característica da doença pulmonar crônica.
Polícitemia primária é uma malignidade muito menos comum da medula óssea chamada policitemia vera, que é caracterizada pela produção descontrolada de todas as células sanguíneas, incluindo eritrócitos. A policitemia, seja secundária ou primária, é geralmente muito menos comum que a anemia.
3,1. PERSPECTIVO HISTÓRICO
O primeiro teste clínico de medição de Hb concebido há mais de um século envolveu a adição de gotas de água destilada a um volume de sangue medido até que a sua cor correspondesse à de um padrão de cor artificial.
Uma modificação posterior envolveu primeiro saturar o sangue com gás de carvão (monóxido de carbono) para converter a hemoglobina para a carboxihemoglobina mais estável. A hemoglobinometria moderna data dos anos 50, seguindo o desenvolvimento da espectrofotometria e do método de hemiglobincianeto (cynamethemoglobina).
Adaptação deste método e outros para uso em analisadores automatizados de hematologia seguidos. Nas últimas duas décadas, os avanços se concentraram no desenvolvimento de métodos que permitem o teste de ponto de tratamento (POCT) da hemoglobina.
Esta seção trata primeiro da consideração de alguns dos métodos atualmente utilizados no laboratório e, em seguida, com os métodos POCT utilizados fora do laboratório.
3.2. HEMIGLOBINCYANIDE – UM MÉTODO ESPECTROFOTOMÉTRICO
Inicialmente 40 anos após ter sido adotado como método de referência para medir a hemoglobina pelo International Committee for Standardization in Hematology (ICSH) , o teste de hemiglobincianeto (HiCN) continua sendo o método recomendado do ICSH contra o qual todos os novos métodos ctHb são julgados e padronizados.
A consideração detalhada que se segue reflete sua importância contínua tanto como método laboratorial de referência quanto como método de rotina.
3.2.1. Princípio do teste
Blood é diluído numa solução contendo ferricianeto de potássio e cianeto de potássio. O ferricianeto de potássio oxida o ferro em heme ao estado férrico para formar a metemoglobina, que é convertida em hemiglobincianeto (HiCN) pelo cianeto de potássio.
HiCN é um produto de cor estável, que em solução tem uma absorvância máxima a 540 nm e obedece rigorosamente à lei de Beer-Lambert. A absorvância da amostra diluída a 540 nm é comparada com a absorvância no mesmo comprimento de onda de uma solução padrão HiCN cuja concentração equivalente de hemoglobina é conhecida.
Os derivados da maioria da hemoglobina (oxihemoglobina, metemoglobina e carboxihemoglobina, mas não sulfhemoglobina) são convertidos em HiCN e, portanto, medidos por este método.
3.2.1.1. Diluente de reagente (solução Drabkin modificada)
| Potássio ferricianeto (K3Fe(CN)6) | 200 mg |
| Cianeto de potássio (KCN) | 50 mg |
| Dihidrogenofosfato de potássio (KH2 PO4) | 140 mg |
| Não-detergente iônico (e.g. Triton X-100) | 1 mL |
| Acima diluído até 1000 mL em água destilada |
3.2.1.2. Método manual
25 µl de sangue é adicionado a 5.0 mL de reagente, misturado e deixado durante 3 minutos. A absorvância é lida a 540 nm contra um reagente em branco. A absorvância do padrão HiCN é medida da mesma forma.
3.2.1.3. ICSH HiCN standard
A grande vantagem deste método é que existe uma solução HiCN standard fabricada e atribuída a um valor de concentração de acordo com critérios muito precisos estabelecidos e revistos periodicamente pelo International Council for Standardization in Hematology (ICSH) .
Esta solução padrão internacional é o principal calibre para as soluções padrão comerciais utilizadas nos laboratórios clínicos em todo o mundo. Assim, todos aqueles que utilizam a padronização HiCN estão efetivamente utilizando o mesmo padrão, cujo valor foi escrupulosamente validado.
3.2.1.4. Interferência
Turbidez devida a proteínas, lipídios e matéria celular é um problema potencial com a estimativa espectrofotométrica de qualquer constituinte do sangue, incluindo a hemoglobina.
A grande diluição (1:251) da amostra elimina amplamente o problema, mas resultados de ctHb falsamente elevados podem ocorrer em pacientes cuja concentração de proteína plasmática é particularmente elevada .
Amostras fortemente lipémicas e aquelas que contêm números muito elevados de leucócitos (leucócitos) podem também aumentar a ctHb de forma artefactual através de um mecanismo semelhante .
3.2.1.5. Vantagens do HiCN
- Padrão internacional – preciso
- Fácilmente adaptado a analisadores automatizados de hematologia; assim reprodutíveis (baixos DP e CV – dentro do CV de lote tipicamente
- Bem estabelecido e minuciosamente investigado – ICSH recomendado
- Reagente barato
3.2.1.6. Desvantagens do HiCN
- Método manual requer pipetagem precisa e espectrofotômetro
- Reagente (cianeto) perigoso
- O acima limita seu uso fora do laboratório
- Subjeta à interferência de lipídios elevados, proteínas plasmáticas e números de leucócitos
- Não distingue os derivados de hemoglobina que não têm capacidade de transporte de oxigênio (MetHb, COHb, SHb). Assim, pode sobrestimar a capacidade de transporte de oxigênio do sangue se estes estiverem presentes em quantidades anormais (mais que vestígios).
3.3. MÉTODOS ALTERNATIVOS (SEM CICANIDE) LABORATÓRIOS
Sulfato de laurilo de sódio (SLS) é um surfactante que tanto lisa eritrócitos como rapidamente forma um complexo com a hemoglobina liberada. O produto SLS-MetHb é estável por algumas horas e tem um espectro característico com absorção máxima a 539 nm .
O complexo obedece à lei de Beer-Lambert para que haja uma correlação linear precisa entre a concentração de Hb e a absorvância de SLS-MetHb.
O método envolve simplesmente misturar 25 µL de sangue com 5.0 mL de uma solução de 2.08-mol/L de SLS (tamponado para pH de 7.2), e a absorvância de leitura a 539 nm. Os resultados da ctHb pelo método SLS-Hb demonstraram uma correlação muito estreita (r = 0,998) com o método de referência HiCN .
O método foi adaptado para analisadores hematológicos automatizados e é tão confiável em termos de precisão e precisão quanto os métodos automatizados HiCN . Uma grande vantagem é que o reagente é atóxico. Também é menos propenso à interferência por lipemia e aumento da concentração de leucócitos .
A instabilidade a longo prazo da SDS-MetHb exclui o seu uso como padrão, pelo que o método deve ser calibrado com sangue cuja ctHb foi determinada usando o método de referência HiCN.
3.3.2. Método da metemoglobina azida
Este método é baseado na conversão da hemoglobina num produto de cor estável, a metemoglobina azida, que tem um espectro de absorção quase idêntico ao do HiCN .
O reagente utilizado neste método é muito semelhante ao utilizado no método de referência HiCN com a substituição da azida de sódio pelo cianeto de potássio mais tóxico. Como no método HiCN, a hemoglobina é convertida em metemoglobina por ferricianeto de potássio; a azida forma então um complexo com metemoglobina.
ctHb resultados por este método são comparáveis aos resultados obtidos pelo método de referência HiCN; este é um método manual alternativo aceitável. O potencial explosivo da azida sódica, contudo, impede a sua utilização em analisadores hematológicos automatizados. A reacção azida-MetHb foi adaptada para hemoglobinómetros POCT.
3.4. MEDIÇÃO ctHb FORA DO LABORATÓRIO
Os métodos POCT considerados aqui são:
- Hemoglobinómetros portáteis
- CO-oximetria – um método utilizado em analisadores de gases sanguíneos POCT
- EUA escala de cor
3.4.1. Hemoglobinómetros portáteis
Os hemoglobinómetros portáteis como o HemoCue-B permitem a determinação precisa da hemoglobina à beira do leito. São essencialmente fotómetros que permitem a medição da intensidade de cor das soluções.
A microcuvette descartável na qual estas medições são feitas também actua como recipiente de reacção. Os reagentes necessários tanto para a liberação de Hb de eritrócitos como para a conversão de Hb em um produto de cor estável estão presentes na forma seca nas paredes da cubeta.
Tudo o que é necessário é a introdução de uma pequena amostra (tipicamente 10 µL) de sangue capilar, venoso ou arterial na microcuvette e a inserção da microcuvette no instrumento.
O instrumento é pré-calibrado de fábrica usando o padrão HiCN, e a absorvância da solução de teste é automaticamente convertida para ctHb. O resultado é exibido em menos de um minuto.
3.4.1.1. As vantagens dos hemoglobinômetros modernos incluem
- Portabilidade
- Bateria ou operada por rede, pode ser usado em qualquer lugar
- Pequeno volume de amostra (10 µL) obtido por picada de dedo
- Rápido (resultado em 60 segundos)
- Facilidade de uso – sem pipetagem
- Treinamento mínimo exigido por pessoal não-laboratorial
- Padrão contra HiCN – resultados comparáveis aos obtidos em laboratório
- Correção para turbidez. A este respeito, hemoglobinômetros portáteis superiores à maioria dos métodos ctHb .
>
>
>
>
Esta tecnologia tem sido extensivamente avaliada em uma gama de configurações e a maioria dos estudos tem confirmado precisão e precisão aceitáveis quando comparados com métodos laboratoriais.
3.4.1.2. Desvantagens
Alguns estudos, no entanto, levantaram a preocupação de que nas mãos de pessoal não-laboratorial os resultados possam ser menos satisfatórios. Apesar da simplicidade de operação, estes instrumentos não são imunes ao erro do operador, sendo essencial um treino eficaz.
Existem evidências que sugerem que os resultados derivados de amostras capilares (punção capilar) são menos precisos que os derivados de amostras capilares ou venosas bem misturadas coletadas em garrafas de EDTA .
3.4.2. CO-oximetria
Um CO-oxímetro é um espectrofotômetro especializado, o nome reflete a aplicação original, que era para medir COHb e MetHb.
Muitos analisadores modernos de gases do sangue possuem um oxímetro de CO incorporado, permitindo a estimativa simultânea da ctHb durante a análise dos gases do sangue.
A medição da ctHb pela CO-oximetria baseia-se no fato de que a hemoglobina e todos os seus derivados são proteínas coloridas que absorvem a luz em comprimentos de onda específicos e, portanto, têm um espectro de absorção característico (FIGURA 3).
A lei de Beer-Lambert dita que a absorvância de um único composto é proporcional à concentração desse composto. Se a característica espectral de cada substância absorvente em uma solução for conhecida, leituras de absorbância da solução em vários comprimentos de onda podem ser usadas para calcular a concentração de cada substância absorvente.
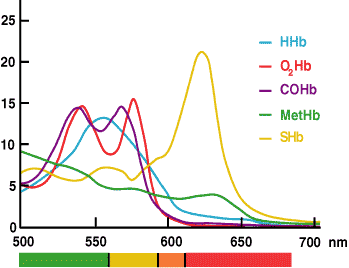
FIGURA 3.
> Nas medições de absorvância do CO-oxímetro de uma amostra de sangue hemolisado em comprimentos de onda múltiplos em toda a gama que as espécies de hemoglobina absorvem a luz (520-620 nm) são utilizadas pelo software instalado para calcular a concentração de cada um dos derivados da hemoglobina (HHb, O2Hb, MetHb e COHb). ctHb é a soma calculada desses derivados.
Tudo o que é necessário do operador é a injeção de uma amostra bem misturada de sangue arterial no analisador de gases sanguíneos/oxímetro de CO.
A amostra, ou parte dela, é bombeada automaticamente para a cubeta de medição do CO-oxímetro, onde – por ação química ou física – os eritrócitos são lisados para liberar hemoglobina, que é escaneada espectroscopicamente como descrito acima.
Resultados são mostrados juntamente com os resultados dos gases sanguíneos em um minuto ou dois.
Estudos transversais confirmaram que os resultados da ctHb obtidos pela CO-oximetria não são clinicamente significativamente diferentes daqueles derivados dos métodos laboratoriais de referência. A CO-oximetria fornece um meio aceitável de estimativa urgente da ctHb em um ambiente de cuidados críticos.
3.4.2.1. As vantagens particulares da ctHb por CO-oximetria incluem
- Velocidade da análise
- Facilidade da análise
- Velocidade da amostra
- Sem custo de capital ou consumível além do necessário para análise de gases sanguíneos
- Parâmetros adicionais (MetHb, COHb, O2Hb) medido
- Não afetado por alta contagem de células brancas
3.4.3. Escala de cor da hemoglobina da OMS (HCS)
Desenvolvido para a Organização Mundial de Saúde (OMS), este teste de baixa tecnologia tem aplicação limitada nos países desenvolvidos, mas tem enorme significado para os países economicamente desfavorecidos do mundo em desenvolvimento, onde a anemia é mais prevalente.
Em áreas onde não há instalações laboratoriais e recursos insuficientes para financiar hemoglobinômetros POCT mais sofisticados, este é praticamente o único meio de determinar a ctHb.
O teste HCS é baseado no princípio simples de que a cor do sangue é uma função da ctHb. Uma gota de sangue é absorvida no papel e sua cor comparada com um gráfico de seis tons de vermelho, cada tom representando um ctHb equivalente: o mais claro 40 g/L e o mais escuro 140 g/L. Embora, em princípio, muito simples, a pesquisa e a tecnologia foram utilizadas no desenvolvimento para garantir a máxima precisão e precisão possíveis.
Por exemplo, testes extensivos de diferentes papéis informaram a escolha final do papel para a matriz da tira de teste, e análises espectrofotométricas de sangue e misturas de corantes foram empregadas para chegar à correspondência mais próxima possível entre a cor da tabela e a cor do sangue em cada ctHb de referência.
3.4.3.1. Vantagens do teste HCS
- É fácil de usar – requer apenas 30 minutos de treinamento
- Não requer equipamento ou potência
- É rápido – resultado em 1 minuto
- Requer apenas uma amostra de punção capilar
- É muito barato (cerca de USD 0,12 por teste)
3.4.3.2. Desvantagens do teste HCS
Resultados confiáveis dependem da estrita aderência às instruções do teste .
Erros comuns incluem:
- Sangue inadequado ou excessivo na tira de teste
- Leitura do resultado demasiado tarde (depois de 2 minutos) ou demasiado cedo (menos de 30 segundos)
- Leitura do resultado em condições de iluminação deficientes
O teste HSC tem claramente limitações inerentes . Na melhor das hipóteses, pode determinar que a ctHb de uma amostra de paciente se encontra dentro de uma das seis faixas de concentração: 30-50 g/L, 50-70 g/L, 70-90 g/L, 90-110 g/L, 110-130 g/L ou 130-150 g/L. Ainda assim, isto é teoricamente suficiente para identificar todos os pacientes, exceto os mais levemente anêmicos, e dar uma indicação de gravidade.
Um estudo precoce demonstrou a capacidade do teste de identificar anemia (definida como ctHb
SUMÁRIO
ctHb é um dos dois parâmetros rotineiramente usados para avaliar a capacidade de transporte de oxigênio do sangue e, assim, estabelecer um diagnóstico de anemia e policitemia.
O teste alternativo, chamado de hematócrito (Hct) ou Volume Celular Embalado (VCP), foi o tema de um artigo companheiro anterior, onde a relação entre ctHb e Hct foi discutida. O foco deste artigo tem sido a medição do ctHb.
Foram concebidos inúmeros métodos, a maioria baseada na medição da cor da hemoglobina ou de um derivado da hemoglobina. Para esta breve revisão foi inevitavelmente necessário ser seletivo. Os métodos escolhidos para discussão estão entre os mais comumente utilizados atualmente.
Na seleção foi feita uma tentativa de transmitir a gama de tecnologias que são empregadas atualmente e como elas são aplicadas para satisfazer a demanda clínica por ctHb em ambientes que vão desde áreas empobrecidas do mundo em desenvolvimento, onde a assistência médica mal tem uma base, até o mundo de alta tecnologia da moderna unidade de terapia intensiva.




