Frontiers in Pharmacology
Introducere
Olanzapina este unul dintre cele mai utilizate antipsihotice de a doua generație (SGA) pentru schizofrenie, tulburare bipolară și simptome psihotice. Pe lângă ameliorarea principalelor simptome ale psihozei, olanzapina prezintă o mare acceptabilitate, scade întreruperea din toate cauzele și previne recăderile viitoare (Leucht et al., 2009). Multe studii clinice randomizate (RCT) și metaanalize au sugerat că olanzapina este unul dintre cele mai eficiente medicamente antipsihotice la pacienții cu schizofrenie (Leucht et al., 2013; Huhn et al., 2019).
Cele mai frecvente efecte adverse ale olanzapinei sunt creșterea în greutate (Allison et al., 1999). Olanzapina determină cea mai mare creștere în greutate dintre SGA. Studiul Comparison of Atypicals for First Episode (CAFE) a demonstrat că 80% dintre pacienții tratați cu olanzapină au câștigat mai mult de 7% din greutatea corporală inițială în săptămâna 52 (McEvoy et al., 2007). Rata de întrerupere a tratamentului cu olanzapină din cauza creșterii în greutate sau a efectelor metabolice însoțitoare a fost de 2-8 ori mai mare decât în cazul altor antipsihotice în cadrul studiului Clinical Antipsychotic Trials in Intervention Effectiveness (CATIE) (Lieberman et al., 2005). Pe lângă faptul că este asociată cu scăderea aderenței la tratamentul medicamentos, creșterea în greutate este, de asemenea, asociată cu o morbiditate și mortalitate medicală substanțială. Având în vedere rata ridicată a obezității la pacienții cu schizofrenie (42%), riscul potențial de creștere în greutate indusă de olanzapină trebuie evaluat cu atenție (Newcomer, 2006). Unele studii randomizate controlate (RCT) au constatat că pacienții cu boli mintale mor cu până la 30 de ani mai devreme decât populația generală (Das-Munshi et al., 2017). Principala cauză de deces la această populație este reprezentată de bolile de inimă. Un factor de risc major pentru bolile de inimă și decesul prematur la acești pacienți este creșterea în greutate (Fekadu et al., 2015).
Mecanismele care stau la baza creșterii în greutate induse de antipsihotice și a efectelor metabolice adverse nu sunt bine înțelese (Correll et al., 2011). Olanzapina este asociată cu creșterea apetitului și a aportului alimentar și scăderea activității sau afectarea reglării metabolice (Roerig et al., 2005; Henderson et al., 2015). Fountaine et al. au raportat că, la bărbații sănătoși, olanzapina a crescut greutatea corporală prin creșterea aportului alimentar, fără a evidenția scăderea nivelului de activitate sau de cheltuieli (Fountaine et al., 2010). Această observație este în concordanță cu observațiile efectuate la adolescenți de sex masculin internați cu schizofrenie (Gothelf et al., 2002). Pacienții au prezentat o creștere semnificativă a indicelui de masă corporală datorată creșterii aportului caloric după un tratament cu olanzapină de 4 săptămâni (Gothelf et al., 2002). Cu toate acestea, dovezile actuale privind asocierea apetitului cu creșterea în greutate nu sunt concludente (Poyurovsky et al., 2007; Case et al., 2010). Case et al. au raportat că modificările timpurii ale apetitului nu au fost corelate în mod consecvent cu modificarea generală a greutății în patru studii diferite (Case et al., 2010). Mai mult, niciun studiu nu a raportat momentul exact al creșterii apetitului, nu a comparat viteza de creștere în greutate în raport cu momentul creșterii apetitului sau nu a evaluat diferențele în ceea ce privește creșterea în greutate și efectele metabolice între pacienții cu apetit crescut sau neschimbat. Prin urmare, am evaluat asocierea dintre creșterea apetitului și modificările în greutate induse de olanzapină și efectele metabolice însoțitoare la pacienții cu schizofrenie aflați la primul episod de schizofrenie care nu au primit niciun medicament.
Materiale și metode
Participanți
Acest studiu a fost efectuat în Institutul de Sănătate Mintală al celui de-al doilea spital Xiangya, Universitatea Centrală de Sud, China, între decembrie 2016 și aprilie 2019. Participanții au fost evaluați pentru schizofrenie în conformitate cu criteriile definite de Manualul diagnostic și statistic al tulburărilor mintale – a cincea ediție (DSM-5) (A.P. Association, 2013). Deoarece pacienții naivi la antipsihotice/primul episod par să câștige mai multă greutate după tratamentul cu olanzapină (Correll et al., 2011), în acest studiu au fost incluși pacienți cu schizofrenie la primul episod cu vârste cuprinse între 18 și 50 de ani.
Criteriile de excludere au inclus (i) constatări anormale din punct de vedere clinic ale examenelor fizice, ale testelor de laborator sau rezultatele electrocardiogramei (ECG); (ii) tulburări precum dizabilitatea intelectuală, tulburări de consum de substanțe sau de alcool, un diagnostic de alte boli sistemice specifice conform criteriilor DSM-5; (iii) boli cardiovasculare și metabolice, cum ar fi diabetul zaharat, dislipidemia și hipertensiunea; (iv) antecedente de tulburări de alimentație; (v) dietă strictă în luna dinaintea screeningului sau în timpul studiului; și (vi) sarcină sau alăptare.
Intervenție
Studii anterioare au sugerat că rata de creștere în greutate indusă de olanzapină a fost cea mai rapidă în timpul primelor 12 săptămâni de tratament (Correll et al., 2009). Prin urmare, participanții au fost tratați cu olanzapină (15-20 mg/zi la ora 8:00 p.m.) timp de 12 săptămâni. Doza inițială de olanzapină a fost de 5 mg/zi și apoi ajustată la 15-20 mg/zi în prima săptămână.
Evaluare
Evaluările de bază au inclus date demografice, un istoric medical complet, măsurători antropometrice (greutate și înălțime), apetit, examinare fizică și analize de laborator. Apetitul a fost evaluat zilnic, cu 30 min înainte de prânz, cu patru întrebări standardizate: Foame, Senzație de sațietate, Gândire la mâncare și Supraalimentare. Răspunsurile au fost notate pe o scară de la 0 la 10, unde 0 = „deloc” și 10 = „extrem de”. Creșterea apetitului a fost definită ca o creștere >10% a scorurilor inițiale ale apetitului. Scăderea apetitului a fost definită ca o >10% scăderi ale scorurilor inițiale ale apetitului. Scala Sindromului Pozitiv și Negativ (PANSS) a fost utilizată pentru a evalua severitatea simptomelor schizofreniei. Efectele adverse au fost evaluate prin Scala simptomelor apărute în urma tratamentului (TESS). La fiecare vizită de urmărire, toate evaluările inițiale (inclusiv examinarea fizică, măsurătorile antropometrice, apetitul și TESS) au fost repetate, cu excepția PANSS. PANSS a fost reevaluat la săptămâna 12.
Înainte de tratament și în stare de repaus alimentar, greutatea și înălțimea au fost măsurate după ce participanții s-au descălțat cu îmbrăcăminte ușoară de interior. Apetitul a fost evaluat înainte de prânz și s-a bazat pe judecata medicului evaluator în ziua examinării. Analizele de laborator, inclusiv glucoza plasmatică, funcția hepatică și renală au fost evaluate folosind proceduri enzimatice cu analizatorul chimic automat Boehringer Mannheim/Hitachi 714. Insulina a fost măsurată cu un test imunoenzimatic în fază solidă (ELISA).
Rezultatele primare au fost procentul de pacienți care au avut o creștere a poftei de mâncare și perioada de timp dintre tratamentul cu olanzapină și creșterea poftei de mâncare. Rezultatele secundare au inclus modificări ale greutății, ale indicelui de masă corporală (IMC), ale glucozei la jeun, ale insulinei la jeun și ale indicelui de rezistență la insulină, ale profilurilor lipidice care au inclus trigliceride, colesterol, lipoproteine cu densitate mare (HDL-C) și lipoproteine cu densitate mică (LDL-C) și scorul PANSS. IMC a fost calculat în conformitate cu criteriile Grupului de lucru pentru obezitate din China: greutate sănătoasă (18,5 ≤ IMC <25 kg/m2), supraponderalitate (25 ≤ IMC ≤ 28 kg/m2) și obezitate (IMC > 28 kg/m2). Dislipidemia a fost definită ca fiind colesterol ≥ 5,18 mmolċl-1, trigliceride ≥ 1,70 mmolċl-1, HDL-C < 1,04 mmolċl-1 sau LDL-C ≥ 3,37 mmolċl-1 pe baza ghidurilor chinezești pentru dislipidemie (Hu, 2017). De asemenea, a fost inclusă o analiză a proporției de pacienți care au câștigat mai mult de 7 % din greutatea corporală inițială după 12 săptămâni, care este pragul pentru creșterea în greutate semnificativă din punct de vedere clinic (Kanders et al., 1991).
Analiză statistică
Pachetul statistic pentru științe sociale, versiunea 25.0 (SPSS v25.0) a fost utilizat pentru analiza statistică. Variabilele continue și variabilele categorice sunt descrise folosind statistici de sinteză (medii și deviații standard) sau frecvențe și, respectiv, procente. Testul t al lui Student și analizele chi pătrat au fost utilizate pentru a analiza diferențele dintre grupuri în ceea ce privește modificările greutății corporale, IMC, glucoza și insulina la post, indicele de rezistență la insulină, trigliceridele, colesterolul, HDL-C și LDL-C de la momentul inițial la fiecare punct de timp. Am investigat asocierea dintre greutate, IMC, indicele de rezistență la insulină, LDL-C și pofta de mâncare folosind analiza de regresie liniară. O valoare P (p) < 0,05 a fost considerată semnificativă din punct de vedere statistic.
Rezultate
În total, 33 de pacienți internați cu schizofrenie (vârsta medie, 23,5 ani; interval 18-36 ani) au fost înrolați în studiu. A existat o proporție mai mare de pacienți de sex feminin (63,6%, 21/33). Toți pacienții se aflau în intervalul normal de IMC (IMC mediu, 21,3 ± 1,7 kg/m2). Durata medie a schizofreniei a fost de 11,2 ± 3,7 (interval 5-18) luni. Doi pacienți de sex feminin au renunțat la studiu după 4 săptămâni din cauza apetitului crescut; restul de 31 (93,9%) de participanți au finalizat studiul (tabelul 1).
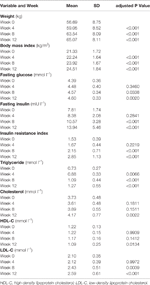
Tabel 1 Rezumat al greutății și al măsurilor metabolice în funcție de studiu.
Creșterea apetitului după tratamentul cu olanzapină
După un tratament cu olanzapină de 12 săptămâni, 77,4% (24/31) dintre pacienți au avut un apetit crescut și 22,6% (7/31) dintre pacienți au avut un apetit neschimbat. După cum se arată în figura 1, pentru cei 24 de pacienți care au avut un apetit crescut, creșterea apetitului a început în primele 8 săptămâni de tratament cu olanzapină și a durat până la sfârșitul tratamentului. Timpul mediu de la inițierea tratamentului cu olanzapină până la creșterea poftei de mâncare a fost de 20,3 zile (SD = 14,4), iar 25,0% (6/24) și 70,8% (17/24) și-au crescut pofta de mâncare în decurs de 1 săptămână și, respectiv, 4 săptămâni. Doi pacienți și-au crescut pofta de mâncare în a 3-a zi după tratamentul cu olanzapină. Nu s-a constatat nicio diferență semnificativă în ceea ce privește apetitul indus de olanzapină între diferitele sexe, utilizând analiza ANOVA în două direcții.
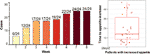
Figura 1 Numărul de pacienți cu creșterea apetitului în timpul perioadelor de tratament cu olanzapină de 8 săptămâni.
Schimbări ale greutății corporale și IMC după tratamentul cu olanzapină
S-au observat creșteri semnificative ale greutății și IMC după tratamentul cu olanzapină (tabelul 1). Creșterea medie în greutate a fost de 7,9 kg în timpul perioadei de 12 săptămâni de tratament cu olanzapină, iar pacienții au câștigat 2,4, 4,0 și 1,5 kg la prima, a doua și, respectiv, a treia perioadă de 4 săptămâni. Pacienții de sex feminin au fost mai predispuși la creșterea în greutate (P < 0,001), cu o creștere medie în greutate de 9,19 kg în timpul perioadei de studiu, comparativ cu o creștere în greutate de 5,90 kg la pacienții de sex masculin. Din totalul pacienților, 80,6% (25/31) și 61,3% (19/31) și-au crescut greutatea corporală inițială cu mai mult de 7% și, respectiv, 10%, în timpul tratamentului cu olanzapină de 12 săptămâni (tabelul suplimentar 1). După 12 săptămâni, 51,6% (16/31) dintre pacienți au devenit supraponderali (IMC>25 kg/m2).
Schimbări ale tulburărilor metabolice după tratamentul cu olanzapină
Au fost observate creșteri semnificative ale glicemiei la jeun, insulinei la jeun, indicelui de rezistență la insulină, trigliceridelor, colesterolului și LDL-C și scăderi ale HDL-C la 12 săptămâni (Tabelul 1). Niciun pacient inclus în studiu nu a prezentat dislipidemie la momentul inițial. Pe baza ghidurilor chinezești pentru dislipidemie, 38,7% (12/31) dintre pacienți aveau dislipidemie după 12 săptămâni de tratament cu olanzapină.
Creșterea apetitului și creșterea în greutate indusă de olanzapină
Pentru a detecta efectul creșterii apetitului asupra creșterii în greutate induse de olanzapină, am împărțit pacienții în două grupuri (grupul cu apetit crescut și grupul cu apetit neschimbat ) în funcție de creșterea sau nu a apetitului după 12 săptămâni de tratament cu olanzapină.
În comparație cu grupul cu apetit neschimbat, au existat creșteri semnificative ale greutății și ale nivelului IMC în grupul de creștere a apetitului după 12 săptămâni de tratament cu olanzapină (tabelul 2). Figura 2 a prezentat comparația creșterii în greutate și a rezultatelor legate de metabolism între grupurile cu apetit crescut și cele cu apetit neschimbat. Analizele detaliate au fost prezentate în Tabelul suplimentar 2. Creșterea în greutate între cele două grupuri a fost semnificativă (P = 0,01) utilizând analiza ANOVA în două direcții. Greutatea medie a crescut cu 9,1 kg (SD = 4,1) în grupul cu apetit crescut și cu 3,9 kg (SD = 2,0) în grupul cu apetit neschimbat, cu o diferență semnificativă între cele două grupuri în timpul perioadei de tratament cu olanzapină de 12 săptămâni. Un procent mai mare de pacienți (91,7%) din grupul cu apetit crescut a câștigat mai mult de 7% din greutatea corporală inițială după 12 săptămâni, în comparație cu pacienții din grupul cu apetit neschimbat (42,9%; χ2 = 8,27, df = 1, p = 0,004). În mod similar, mai mulți pacienți din grupul cu apetit crescut (19/24, 79,2%) au câștigat mai mult de 10% din greutatea corporală inițială după 12 săptămâni în comparație cu pacienții din grupul cu apetit neschimbat (0,0%; χ2 = 14,32, df = 1, p < 0,001) (Tabele suplimentare 3-5). După 12 săptămâni de tratament cu olanzapină, 58,3% dintre pacienți au devenit supraponderali în grupul cu apetit crescut, comparativ cu 28,6% dintre pacienții din grupul cu apetit neschimbat. Creșterea apetitului a mediat puternic creșterea în greutate indusă de olanzapină, cu un efect de mediere de 66,2%.

Tabel 2 Statistici descriptive ale măsurilor de rezultat între grupurile de apetit crescut și neschimbat la momentul inițial și în săptămânile 4, 8 și 12.
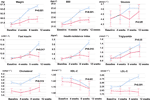
Figura 2 Compararea greutății corporale, a IMC, a glicemiei și a nivelurilor de lipide între grupurile cu apetit crescut și neschimbat. Linia albastră indică pacienții cu apetit crescut; linia roșie indică pacienții cu apetit neschimbat.
Creșterea apetitului și tulburările metabolice induse de Olanzapină
Au existat diferențe semnificative în ceea ce privește insulina (p = 0,017), indicele de rezistență la insulină (p = 0,015) și LDL-C (p = 0,001) între grupurile cu apetit crescut și cele cu apetit neschimbat după 12 săptămâni (figura 2 și tabelul 2). Patru pacienți din grupul de creștere a apetitului aveau colesterolul ≥ 5,18 mmolċl-1, nouă aveau trigliceride ≥ 1,70 mmolċl-1, șase aveau HDL-C < 1,04ċmmol l-1 și trei aveau LDL-C ≥ 3,37 mmolċl-1 la săptămâna 12. În total, 13/24 de pacienți din grupul cu apetit crescut au avut dislipidemie după 12 săptămâni, în timp ce niciunul dintre pacienții din grupul cu apetit neschimbat nu a dezvoltat dislipidemie în timpul perioadei de studiu (tabelul 3).

Tabel 3 Dislipidemia definită de fiecare măsurătoare unică de rezultat în grupurile cu apetit crescut și neschimbat.
Câștigul ponderal maxim atins la o lună după luna de creștere a apetitului
În grupul cu apetit crescut, am analizat câștigul ponderal mediu pentru fiecare pacient la patru momente de timp: înainte de luna de creștere a apetitului (-1M), luna de creștere a apetitului (0M), o lună după creșterea apetitului (+1M) și două luni după creșterea apetitului (+2M). Comparativ cu -1M, a existat o creștere a creșterii în greutate la 0M, dar această schimbare nu a fost semnificativă (-1M vs. 0M, 1,4 ± 1,2 kg vs. 3,1 ± 1,4 kg). Creșterea în greutate a intrat în creștere maximă la +1M, cu o creștere de 4,3 ± 2.Creștere de 4 kg. Creșterea în greutate a decelerat la +2M (p < 0,001) cu 1,6 ± 1,5 kg. Creșterea în greutate la +2M a încetinit și s-a stabilizat și nu au fost observate diferențe semnificative în comparație cu -1M (Figura 3 și Tabelul suplimentar 6).
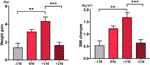
Figura 3 Viteza medie de creștere în greutate în grupul cu apetit crescut. Câștigul mediu în greutate pentru fiecare pacient pe lună în timpul perioadei de studiu a fost analizat la patru momente de timp: înainte de luna în care a crescut pofta de mâncare (-1M), luna în care a crescut pofta de mâncare (0M), la 1 lună după luna în care a crescut pofta de mâncare (+1M) și la 2 luni după luna în care a crescut pofta de mâncare (+2M). ** indică P < 0,01, *** indică P < 0,001.
Apetitul crescut mai devreme prezice o creștere mai mare în greutate în 1 lună după luna de creștere a apetitului
Am comparat în continuare viteza de creștere în greutate a participanților cu un apetit crescut în decurs de 4 săptămâni (A) și a participanților cu un apetit crescut între 4 și 8 săptămâni (B). La 0M, vitezele de creștere în greutate între participanții cu creșterea apetitului în decurs de 4 săptămâni și participanții cu un apetit crescut între 4 și 8 săptămâni nu au fost semnificativ diferite. Cu toate acestea, participanții cu apetit crescut mai devreme au prezentat o viteză de creștere în greutate semnificativ mai mare la +1M. Aceste rezultate au demonstrat că un apetit crescut mai devreme ar putea duce la o creștere în greutate mai mare în timpul perioadei de urmărire (Figura 4). Modificări similare ale IMC au fost observate în timpul celor patru puncte de timp (figurile 3 și 4).
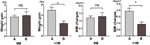
Figura 4 Comparația vitezei de creștere în greutate a participanților cu apetit crescut în diferite luni. Am comparat viteza de creștere în greutate a participanților cu apetit crescut în decurs de 4 săptămâni (A) și a participanților cu un apetit crescut între 4 și 8 săptămâni (B) în luna în care a crescut pofta de mâncare (0M) și la 1 lună după luna în care a crescut pofta de mâncare (+1M). ns, indică nesemnificativ, * indică P < 0,05.
Apetitul și viteza modificărilor tulburărilor metabolice
Datele descriptive detaliate pentru modificările în greutate, IMC, glucoza la post, insulina, indicele de rezistență la insulină, trigliceridele, colesterolul, HDL-C și LDL-C sunt rezumate în tabelul 2 Pentru a investiga asocierea dintre apetitul crescut și metabolismul glucozei și al lipidelor, am analizat modificările acestor indicatori la patru momente de timp în grupul cu apetit crescut. Nu au fost observate modificări semnificative ale vitezei pentru glucoză, trigliceride, HDL-C și LDL-C la niciun punct de timp. Creșteri semnificative ale vitezelor insulinei și ale indicelui de rezistență la insulină au fost observate doar la +2M (Figura suplimentară 1 și Tabelul suplimentar 6). Comparațiile suplimentare au sugerat că participanții cu creșterea poftei de mâncare în decurs de 4 săptămâni nu au prezentat o creștere semnificativă a vitezei insulinei și a indicelui de rezistență la insulină la 0M și +1M în comparație cu participanții cu creșterea poftei de mâncare între 4 și 8 săptămâni (Figura suplimentară 2).
Predicția apetitului asupra creșterii în greutate și a tulburărilor metabolice induse de olanzapină
Am efectuat o analiză de regresie liniară pentru a evalua efectul creșterii poftei de mâncare asupra creșterii în greutate, a glicemiei și a nivelurilor de lipide. După ce am controlat variabilele semnificative din punct de vedere statistic, cum ar fi sexul, vârsta, înălțimea și durata, am inclus creșterea în greutate, IMC, glucoza la post, insulina, indicele de rezistență la insulină, trigliceridele, colesterolul, HDL-C și LDL-C ca variabile dependente și apetitul ca variabilă independentă în analiza de regresie. Creșterea apetitului a fost asociată cu modificări ale greutății (β = 0,67, p =0,0003), IMC (β = 0,63, p = 0,0004), insulină (β = 0,49, p = 0,019), indice de rezistență la insulină (β = 0,51, p = 0,0149) și LDL-C (β = 0.61, p = 0,0035) (Tabelul suplimentar 7).
S-au observat îmbunătățiri semnificative ale simptomelor clinice (evaluate prin PANSS, p < 0,001) de la linia de bază până la punctul final după tratamentul cu olanzapină. Nu au fost observate diferențe semnificative în PANSS între grupurile cu apetit crescut și apetit neschimbat (p > 0,05).
Efecte adverse
Dintre toți cei 31 de pacienți care au finalizat studiul, nouă (29.0%) pacienți au raportat hipoactivitate, opt (25,8%) pacienți au raportat somnolență, patru (12,9%) pacienți au avut teste hepatice anormale, doi (6,5%) pacienți au raportat acatisie, patru (12,9%) pacienți au avut constipație, unul (3.2%) a avut diaree și doi (6,5%) pacienți s-au simțit amețiți, iar 80,6% (25/31) dintre pacienți și-au crescut greutatea corporală cu mai mult de 7% în timpul perioadei de studiu.
Discuție
În acest studiu prospectiv, principalele constatări au arătat că 77,4% dintre pacienți și-au crescut pofta de mâncare după tratamentul cu olanzapină, iar acești pacienți care și-au crescut pofta de mâncare au câștigat mai multă greutate decât acei pacienți cu pofta de mâncare neschimbată (9,1 kg vs. 3,9 kg). În mod similar, mai mulți pacienți din grupul de pacienți cu apetit crescut și-au crescut greutatea corporală inițială cu mai mult de 7 sau 10%, ceea ce sugerează că apetitul crescut este asociat cu o creștere substanțială în greutate la pacienții cu schizofrenie la primul episod de schizofrenie nedeplasabili tratați cu olanzapină. Mai mult, analiza de regresie liniară a susținut, de asemenea, că creșterea apetitului a fost strâns legată de creșterea în greutate indusă de olanzapină. Aceste constatări au fost în concordanță cu rapoartele anterioare (Gothelf et al., 2002; Cope et al., 2005). Murashita et al. (2005) au observat creșterea nivelului de grelină care stimulează apetitul și a procentului de grăsime corporală la pacienții cu schizofrenie tratați cu olanzapină. Rezultatele unui studiu dublu-orb randomizat au sugerat că olanzapina a indus pofta de mâncare și consumul excesiv de alimente într-o măsură mai mare decât clozapina (Murashita et al., 2005; Kluge et al., 2007). Rezultate similare au fost, de asemenea, raportate la șoarecii tratați cu olanzapină (Cope et al., 2005). Acțiunea olanzapinei asupra mai multor receptori, în special a receptorilor D2 și 5H3, care modulează apetitul, a fost, de asemenea, aplicată în tratamentul anorexiei nervoase și al grețurilor și vărsăturilor induse de chimioterapie (Kluge et al., 2007; Tan et al., 2009; Kafantaris et al., 2011).
Am constatat, de asemenea, că 70,8% dintre pacienți și-au crescut apetitul în primele 4 săptămâni de la tratamentul inițial cu olanzapină, cu o medie de 20,3 zile până la creștere. Unii pacienți chiar și-au crescut pofta de mâncare încă din a treia zi după tratamentul cu olanzapină. Interesant, pacienții al căror apetit a crescut mai devreme în timp au fost susceptibili de a câștiga mai mult în greutate decât pacienții al căror apetit a crescut mai târziu în timp, iar creșterea în greutate a atins un vârf la 1 lună după ce a avut loc creșterea apetitului. Deși nu s-a constatat nicio diferență semnificativă în ceea ce privește apetitul indus de olanzapină între bărbați și femei, pacienții de sex feminin au fost mai susceptibili de a lua în greutate (P < 0,001). Prin urmare, pofta de mâncare ar trebui să fie considerată ca un indicator pentru a prezice creșterea în greutate indusă de olanzapină, în special la pacienții de sex feminin. În mediul clinic, medicii ar trebui să acorde mai multă atenție pacienților al căror apetit crește devreme după tratamentul cu olanzapină și ar trebui să înceapă un plan de prevenire a creșterii în greutate.
Pacienții tratați cu olanzapină au prezentat o creștere de peste 7% din greutatea corporală inițială, ceea ce este în concordanță cu constatările anterioare (Gothelf et al., 2002; Wu et al., 2008). În plus față de creșterea semnificativă în greutate, pacienții cu tratament cu olanzapină au avut un metabolism al glucozei și al lipidelor perturbat semnificativ după 12 săptămâni, ceea ce este în concordanță cu observațiile publicate anterior la pacienții cu schizofrenie (Correll et al., 2011). Comparativ cu pacienții din grupul cu apetit neschimbat, grupul cu apetit crescut a prezentat anomalii lipidice semnificative. Glicemia în stare de repaus nu a fost semnificativ diferită între cele două grupuri. Participanții cu apetit crescut timpuriu nu au prezentat o creștere a vitezei insulinei și a indicelui de rezistență la insulină în următoarele luni după creșterea apetitului. Este posibil ca nivelurile de glucoză să fie independente de creșterea în greutate, deoarece apetitul nu a afectat nivelurile de glucoză.
Rezultatele adverse asupra sănătății fizice asociate cu antipsihoticele, cum ar fi creșterea în greutate, tulburările metabolice și morbiditatea asociată, au fost recunoscute de mult timp (Wu et al., 2016). Studii anterioare au sugerat că apetitul poate prezice creșterea în greutate indusă de olanzapină și efectele metabolice adverse (Gothelf et al., 2002; Poyurovsky et al., 2007; Fountaine et al., 2010). Din cunoștințele noastre, acesta este primul studiu care evaluează asocierea dintre apetit, creșterea în greutate și tulburările metabolice după tratamentul cu olanzapină la pacienții cu schizofrenie la primul episod de schizofrenie care nu au luat medicamente. Unele constatări ne oferă mai multe dovezi despre cum să alegem în mod rezonabil medicația în activitatea clinică și oferă mai multe beneficii pentru prevenirea creșterii în greutate și a tulburărilor metabolice induse de olanzapină.
Există mai multe limitări ale studiului nostru. În primul rând, acest studiu nu a măsurat aportul alimentar, cum ar fi mesele și gustările, deși tuturor pacienților incluși li s-a oferit același meniu alimentar standardizat. Un aport ridicat de grăsimi și fructoză poate scădea controlul apetitului prin afectarea reglării centrale a apetitului. Într-adevăr, dietele bogate în fructoză au efecte adverse asupra semnalizării centrale a apetitului și asupra funcției cognitive (Lowette et al., 2015; Dalvi et al., 2017). În al doilea rând, nu am examinat nivelurile de leptină și grelină în timpul perioadei de studiu. Secretate din țesutul adipos și, respectiv, din stomac, leptina și ghrelina joacă roluri cruciale în reglarea aportului alimentar și a metabolismului energetic (Cui et al., 2017). Mai multe studii au constatat o creștere a nivelului de leptină și o scădere a nivelului de grelină în primele câteva săptămâni după inițierea tratamentului cu olanzapină (Basoglu et al., 2010; Stip et al., 2012; Lu et al., 2015). Creșterea nivelului de leptină rămâne stabilă timp de câteva săptămâni, dar nivelul de ghrelin crește în perioada mai lungă (Sentissi et al., 2008). Cercetările ulterioare ar trebui să monitorizeze răspunsurile leptinei și ghrelinului la creșterea apetitului, precum și relațiile acestora cu parametrii metabolici și efectele clinice. În plus, nu am monitorizat nivelurile de activitate în timpul perioadei de studiu. Deși unele studii au raportat că olanzapina a crescut greutatea corporală numai prin creșterea apetitului și a aportului alimentar, fără diferențe semnificative în ceea ce privește cheltuielile energetice în repaus (Gothelf et al., 2002; Fountaine et al., 2010). O serie de studii au raportat reducerea activităților fizice în cazul medicației cu olanzapină (Perez-Cruzado et al., 2018). În studiul nostru, 29,0% dintre pacienți au raportat hipoactivitate și 25,8% dintre pacienți au raportat somnolență în timpul perioadei de tratament cu olanzapină de 12 săptămâni. Hillebrand și colab. (2005) au constatat că tratamentul cu olanzapină a redus activitatea fizică fizică la șobolanii expuși la anorexie bazată pe activitate. Tratamentul cu olanzapină a redus, de asemenea, nivelul de activitate al pacienților cu anorexie nervoasă, fără diferențe semnificative în ceea ce privește greutatea corporală și nivelul leptinei plasmatice, comparativ cu pacienții netratați. Studiul nostru anterior a demonstrat că intervențiile asupra stilului de viață, care au inclus programe psihoeducaționale, dietetice și de exerciții fizice, pot reduce creșterea în greutate indusă de antipsihotice (Wu et al., 2008). În plus, ar fi mai bine să se compare mai mulți pacienți cu controale sănătoase de vârstă similară, ceea ce poate ajuta la interpretarea faptului că creșterea apetitului indusă de olanzapină și modificările metabolice sunt legate în mod specific de proprietățile sale farmacologice. Studiile ulterioare ar trebui să se concentreze asupra mecanismelor de creștere a apetitului după tratamentul cu olanzapină (Koopmann et al., 2012; Sweeney et al., 2017; Mancuso et al., 2019). Sistemul de recompensă din regiunile striatale poate fi asociat cu creșterea în greutate asociată cu antipsihoticele (Nielsen et al., 2016). Activitatea modificată în cortexul cingular anterior subgenual poate, de asemenea, să stea parțial la baza creșterii apetitului după tratamentul cu olanzapină (Pawlowski et al., 2018). Ar trebui efectuate studii imagistice pentru a investiga modularea cu olanzapină a activității cerebrale profunde legate de apetit.
Concluzii
În concluzie, studiul nostru a arătat că apetitul este legat de creșterea în greutate și dislipidemia indusă de olanzapină la pacienții cu schizofrenie la primul episod de schizofrenie care nu au primit niciun medicament. Evaluarea modificărilor apetitului este o modalitate ușoară și practică de predicție a creșterii în greutate, ceea ce oferă clinicienilor mai mult timp și opțiuni pentru strategiile de intervenție. Invențiile dietetice timpurii care vizează scăderea apetitului și reducerea aportului alimentar pot fi utile pentru controlul greutății la pacienții cu schizofrenie tratați cu olanzapină.
Declarație privind disponibilitatea datelor
Seturile de date generate pentru acest studiu sunt disponibile la cerere la autorul corespondent.
Declarație de etică
Acest studiu a fost realizat în conformitate cu Declarația de la Helsinki (Asociația G.A.o.t.W.M., 2013) și a fost aprobat de Comitetul de etică al celui de-al doilea spital Xiangya, Universitatea Centrală de Sud. După o descriere completă a studiului către participanți, s-a obținut consimțământul în cunoștință de cauză înainte de participarea la studiu.
Contribuții ale autorilor
JH a analizat și a interpretat datele pacienților și a avut o contribuție majoră la redactarea manuscrisului. G-RH a conceput și realizat în principal studiul. YeY, C-CL, J-MX, Y-JL și X-JP au ajutat la recrutarea pacienților, la monitorizarea calității datelor și la documentarea evenimentelor adverse apărute în urma tratamentului. YiY a ajutat la revizuirea manuscrisului. J-PZ a îndrumat proiectarea studiului. RR-W a fost responsabil pentru conținutul general. Toți autorii au citit și aprobat manuscrisul final.
Finanțare
Această lucrare a fost susținută de Proiectele programului cheie R&D, Fundația Națională de Științe a Chinei (Grant nr. 2016YFC1306900) și Fundația Națională de Științe Naturale a Chinei (Grant nr. 81622018 și nr. 8190140101).
Conflict de interese
Autorii declară că cercetarea a fost efectuată în absența oricăror relații comerciale sau financiare care ar putea fi interpretate ca un potențial conflict de interese.
Recunoștințe
Am dori să recunoaștem contribuția valoroasă a participanților și sprijinul acordat de medicii lor de familie. De asemenea, dorim să mulțumim mai multor recenzenți anonimi pentru comentariile și sugestiile lor valoroase în vederea îmbunătățirii calității lucrării.
Material suplimentar
Materialul suplimentar pentru acest articol poate fi găsit online la adresa: https://www.frontiersin.org/articles/10.3389/fphar.2020.00739/full#supplementary-material
Supliment Figura 1 | Viteza de modificare a glicemiei și a lipidelor în sânge în grupul cu apetit crescut. Valorile medii ale modificărilor pentru fiecare pacient pe lună în timpul perioadei de studiu au fost analizate la patru momente de timp: înainte de luna în care a crescut pofta de mâncare (-1M), luna în care a crescut pofta de mâncare (0M), la 1 lună după luna în care a crescut pofta de mâncare (+1M) și la 2 luni după luna în care a crescut pofta de mâncare (+2M).
Supplement Figura 2 | Comparația vitezei de modificare a insulinei și a indicelui de rezistență la insulină la participanții cu apetit crescut în diferite luni. Am comparat viteza participanților cu un apetit crescut în decurs de 4 săptămâni (A) și a participanților cu un apetit crescut între 4-8 săptămâni (B) în luna de timp până la creșterea apetitului (0M) și la 1 lună după luna de timp până la creșterea apetitului (+1M).
Tabel suplimentar 1 | Numărul de pacienți care au avut o creștere a greutății corporale inițiale cu mai mult de 7% sau 10% la săptămânile 4, 8 și 12.
Tabel suplimentar 2 | Numărul de pacienți care au avut o creștere a greutății corporale inițiale cu mai mult de 7% sau 10% la săptămânile 4, 8 și 12 la pacienții cu apetit crescut.
Tabel suplimentar 3 | Numărul de pacienți care au avut o creștere a greutății corporale inițiale cu mai mult de 7% sau 10% la săptămânile 4, 8 și 12 la pacienții cu apetit neschimbat.
Tabel suplimentar 4 | Comparație a numărului de creșteri în greutate de 7% sau 10% între pacienții cu apetit crescut și pacienții cu apetit neschimbat la săptămânile 4, 8 și 12.
Tabel suplimentar 5 | Analiza vitezei creșterii medii în greutate, a modificărilor glicemiei și a lipidelor în grupul cu apetit crescut la patru momente de timp: înainte de luna de timp până la creșterea apetitului (-1M), luna de timp până la creșterea apetitului (0M), la 1 lună după luna de timp până la creșterea apetitului (+1M) și la 2 luni după luna de timp până la creșterea apetitului (+2M). ns indică nesemnificativ, * indică o valoare p < 0,05, ** indică o valoare p < 0,01, *** indică o valoare p < 0,001.
Tabel suplimentar 6 | Estimări ale efectelor apetitului asupra creșterii în greutate și a măsurilor de rezultat legate de metabolism din modelul general liniar mixt în timp ce se controlează vârsta, durata bolii și sexul.
Tabel suplimentar 7-1 | Modificările de greutate, IMC, Insulină, IRI și LDL-C pe pacient în timpul perioadei de tratament în diferite grupuri.
Tabel suplimentar 7-2 | Estimări ale efectelor apetitului asupra creșterii în greutate și a măsurilor de rezultat legate de metabolism.
Abbreviații
SGA, Antipsihotice de a doua generație; RCT, Studiu clinic randomizat; CAFÉ, Compararea atipicelor pentru primul episod; CATIE, Testele clinice antipsihotice în eficiența intervenției; DSM-5, Manualul de diagnostic și statistică a tulburărilor mintale-ediția a cincea; ECG, Electrocardiogramă; PANSS, The Positive and Negative Syndrome Scale; TESS, Treatment Emergent Symptom Scale; ELISA, Enzyme-linked immunosorbent assays; BMI, Indice de masă corporală; HDL-C, High-density lipoprotein; LDL-C, Low-density lipoprotein.
Allison, D. B., Mentore, J. L., Heo, M., Chandler, L. P., Cappelleri, J. C., Infante, M. C., et al. (1999). Creșterea în greutate indusă de antipsihotice: o sinteză cuprinzătoare de cercetare. Am. J. Psychiatry 156, 1686-1696. doi: 10.1176/ajp.156.11.1686
PubMed Abstract | Textul integral | Google Scholar
Association, A.P. (2013). Manualul de diagnostic și statistic al tulburărilor mintale (DSM-5®) (Arlington, VA: American Psychiatric Pub).
Google Scholar
Basoglu, C., Oner, O., Gunes, C., Semiz, U. B., Ates, A. M., Algul, A., et al. (2010). nivelurile de grelină, colecistochinină, visfatină, leptină și proteina legată de agouti în timpul tratamentului cu olanzapină de 6 săptămâni la pacienții de sex masculin cu psihoză la primul episod. Int. Clin. Psychopharmacol. 25, 165-171. doi: 10.1097/YIC.0b013e3283377850
PubMed Abstract | CrossRef Full Text | Google Scholar
Case, M., Treuer, T., Karagianis, J., Hoffmann, V. P. (2010). Rolul potențial al apetitului în prezicerea modificărilor de greutate în timpul tratamentului cu olanzapină. BMC Psychiatry 10, 72. doi: 10.1186/1471-244X-10-72
PubMed Abstract | Full CrossRef Text | Google Scholar
Cope, M., Nagy, T., Fernandez, J., Geary, N., Casey, D., Allison, D. (2005). Creșterea în greutate indusă de medicamente antipsihotice: dezvoltarea unui model animal. Int. J. Obes. 29, 607. doi: 10.1038/sj.ijo.0802928
CrossRef Full Text | Google Scholar
Correll, C. U., Manu, P., Olshanskiy, V., Napolitano, B., Kane, J. M., Malhotra, A. K. (2009). Riscul cardiometabolic al medicamentelor antipsihotice de a doua generație în timpul primei utilizări la copii și adolescenți. Jama 302, 1765-1773. doi: 10.1001/jama.2009.1549
PubMed Abstract | CrossRef Full Text | Google Scholar
Correll, C. U., Lencz, T., Malhotra, A. K. (2011). Medicamentele antipsihotice și obezitatea. Trends Mol. Med. 17, 97-107. doi: 10.1016/j.molmed.2010.10.010
PubMed Abstract | Full CrossRef Text | Google Scholar
Cui, H., Lopez, M., Rahmouni, K. (2017). Bazele celulare și moleculare ale rezistenței la leptină și ghrelin în obezitate. Nat. Rev. Endocrinol. 13, 338-351. doi: 10.1038/nrendo.2016.222
PubMed Abstract | Textul integral | Google Scholar
Dalvi, P. S., Chalmers, J. A., Luo, V., Han, D. Y., Wellhauser, L., Liu, Y., et al. (2017). Grăsimea ridicată induce o inflamație acută și cronică în hipotalamus: efectul dietei bogate în grăsimi, al palmitatului și al TNF-alfa asupra neuronilor NPY care reglează pofta de mâncare. Int. J. Obes. (Lond) 41, 149-158. doi: 10.1038/ijo.2016.183
PubMed Abstract | CrossRef Full Text | Google Scholar
Das-Munshi, J., Chang, C.-K., Dutta, R., Morgan, C., Nazroo, J., Stewart, R., et al. (2017). Etnia și mortalitatea excesivă în cazul bolilor mintale grave: un studiu de cohortă. Lancet Psychiatry 4, 389-399. doi: 10.1016/S2215-0366(17)30097-4
PubMed Abstract | CrossRef Full Text | Google Scholar
Fekadu, A., Medhin, G., Kebede, D., Alem, A., Cleare, A. J., Prince, M., et al. (2015). Excesul de mortalitate în cazul bolilor mintale severe: Studiu de cohortă bazat pe populație de 10 ani în Etiopia rurală. Br. J. Psychiatry 206, 289-296. doi: 10.1192/bjp.bp.114.149112
PubMed Abstract | CrossRef Full Text | Google Scholar
Fountaine, R. J., Taylor, A. E., Mancuso, J. P., Greenway, F. L., Byerley, L. O., Smith, S. R., et al. (2010). Creșterea aportului alimentar și a cheltuielilor energetice în urma administrării de olanzapină la bărbații sănătoși. Obesity 18, 1646-1651. doi: 10.1038/oby.2010.6
PubMed Abstract | Full CrossRef Text | Google Scholar
Asociația G.A.o.t.W.M. (2013). Declarația de la Helsinki a Asociației Medicale Mondiale: principii etice pentru cercetarea medicală care implică subiecți umani. JAMA 10 (20) 2191-2194. doi: 10.1001/jama.2013.281053
CrossRef Full Text | Google Scholar
Gothelf, D., Falk, B., Singer, P., Kairi, M., Phillip, M., Zigel, L., et al. (2002). Creșterea în greutate asociată cu un aport alimentar crescut și niveluri scăzute de activitate obișnuită la adolescenții schizofrenici internați de sex masculin tratați cu olanzapină. Am. J. Psychiatry 159, 1055-1057. doi: 10.1176/appi.ajp.159.6.1055
PubMed Abstract | Textul integral | Google Scholar
Henderson, D. C., Vincenzi, B., Andrea, N. V., Ulloa, M., Copeland, P. M. (2015). Mecanisme fiziopatologice ale riscului cardiometabolic crescut la persoanele cu schizofrenie și alte boli mintale severe. Lancet Psychiatry 2, 452-464. doi: 10.1016/S2215-0366(15)00115-7
PubMed Abstract | CrossRef Full Text | Google Scholar
Hillebrand, J. J., van Elburg, A. A., Kas, M. J., van Engeland, H., Adan, R. A. (2005). Olanzapina reduce activitatea fizică la șobolanii expuși la anorexie bazată pe activitate: posibile implicații pentru tratamentul anorexiei nervoase? Biol. Psychiatry 58, 651-657.
PubMed Abstract | Google Scholar
Hu, D.-Y. (2017). Noi orientări și dovezi pentru prevenirea și tratamentul dislipidemiei și a bolilor cardiovasculare aterosclerotice în China. Chronic Dis. Trans. Med. 3, 73. doi: 10.1016/j.cdtm.2016.11.001
CrossRef Full Text | Google Scholar
Huhn, M., Nikolakopoulou, A., Schneider-Thoma, J., Krause, M., Samara, M., Peter, N., et al. (2019). Eficacitatea și tolerabilitatea comparativă a 32 de antipsihotice orale pentru tratamentul acut al adulților cu schizofrenie multiepisodică: o revizuire sistematică și o meta-analiză de rețea. Lancet 394 (10202), 939-951. doi: 10.1016/S0140-6736(19)31135-3
PubMed Abstract | CrossRef Full Text | Google Scholar
Kafantaris, V., Leigh, E., Hertz, S., Berest, A., Schebendach, J., Sterling, W. M., et al. (2011). Un studiu pilot controlat cu placebo al olanzapinei adjuvante pentru adolescenții cu anorexie nervoasă. J. Child Adolesc. Psychopharmacol. 21, 207-212. doi: 10.1089/cap.2010.0139
PubMed Abstract | Full CrossRef Text | Google Scholar
Kanders, B., Forse, R., Blackburn, G. (1991). Metode în obezitate. Conn „s Current Therapy. Ed. Rakel, R. E. (Philadelphia: WB Saunders), 524-532.
Google Scholar
Kluge, M., Schuld, A., Himmerich, H., Dalal, M., Schacht, A., Wehmeier, P. M., et al. (2007). Clozapina și olanzapina sunt asociate cu pofta de mâncare și mâncatul compulsiv: rezultatele unui studiu dublu-orb randomizat. J. Clin. Psychopharmacol. 27, 662-666. doi: 10.1097/jcp.0b013e31815a8872
PubMed Abstract | CrossRef Full Text | Google Scholar
Koopmann, A., von der Goltz, C., Grosshans, M., Dinter, C., Vitale, M., Wiedemann, K., et al. (2012). Asocierea peptidei apetitului peptidei apetitului ghrelin acetilat cu pofta de alcool la persoanele dependente de alcool abstinente timpurii. Psychoneuroendocrinology 37, 980-986. doi: 10.1016/j.psyneuen.2011.11.005
PubMed Abstract | CrossRef Full Text | Google Scholar
Leucht, S., Corves, C., Arbter, D., Engel, R. R., Li, C., Davis, J. M. (2009). Medicamente antipsihotice de a doua generație față de cele de primă generație pentru schizofrenie: o meta-analiză. Lancet 373, 31-41. doi: 10.1016/S0140-6736(08)61764-X
PubMed Abstract | CrossRef Full Text | Google Scholar
Leucht, S., Cipriani, A., Spineli, L., Mavridis, D., Orey, D., Richter, F., et al. (2013). Eficacitatea comparativă și tolerabilitatea a 15 medicamente antipsihotice în schizofrenie: o meta-analiză cu tratamente multiple. Lancet 382, 951-962. doi: 10.1016/S0140-6736(13)60733-3
PubMed Abstract | CrossRef Full Text | Google Scholar
Lieberman, J. A., Stroup, T. S., McEvoy, J. P., Swartz, M. S., Rosenheck, R. A., Perkins, D. O., et al. (2005). Eficacitatea medicamentelor antipsihotice la pacienții cu schizofrenie cronică. New Engl. J. Med. 353, 1209-1223. doi: 10.1056/NEJMoa051688
CrossRef Full Text | Google Scholar
Lowette, K., Roosen, L., Tack, J., Vanden Berghe, P. (2015). Efectele dietelor cu conținut ridicat de fructoză asupra semnalizării apetitului central și a funcției cognitive. Front. Nutr. 2, 5. doi: 10.3389/fnut.2015.00005
PubMed Abstract | CrossRef Full Text | Google Scholar
Lu, M. L., Wang, T. N., Lin, T. Y., Shao, W. C., Chang, S. H., Chou, J. Y., et al. (2015). Efectele diferențiale ale olanzapinei și clozapinei asupra nivelurilor plasmatice ale adipocitocinelor și ale ghrelinului total. Prog. Neuropsychopharmacol. Biol. Psychiatry 58, 47-50.
PubMed Abstract | Google Scholar
Mancuso, C., Izquierdo, A., Slattery, M., Becker, K. R., Plessow, F., Thomas, J. J., et al. (2019). Modificările hormonilor de reglare a apetitului în urma consumului de alimente sunt asociate cu modificări ale apetitului raportat și o măsură a mâncării hedonice la fete și femei tinere cu anorexie nervoasă. Psychoneuroendocrinology 113, 104556. doi: 10.1016/j.psyneuen.2019.104556
PubMed Abstract | CrossRefef Full Text | Google Scholar
McEvoy, J. P., Lieberman, J. A., Perkins, D. O., Hamer, R. M., Gu, H., Lazarus, A., et al. (2007). Eficacitatea și tolerabilitatea olanzapinei, quetiapinei și risperidonei în tratamentul psihozei timpurii: o comparație randomizată, dublu-orb de 52 de săptămâni. Am. J. Psychiatry 164, 1050-1060. doi: 10.1176/ajp.2007.164.7.1050
PubMed Abstract | CrossRef Full Text | Google Scholar
Murashita, M., Kusumi, I., Inoue, T., Takahashi, Y., Hosoda, H., Kangawa, K., et al. (2005). Olanzapina crește nivelul de ghrelină plasmatică la pacienții cu schizofrenie. Psychoneuroendocrinology 30, 106-110. doi: 10.1016/j.psyneuen.2004.05.008
PubMed Abstract | CrossRef Full Text | Google Scholar
Newcomer, J. W. (2006). Riscul medical la pacienții cu tulburare bipolară și schizofrenie. J. Clin. Psychiatry 67, e16. doi: 10.4088/JCP.1106e16
PubMed Abstract | CrossRef Full Text | Google Scholar
Nielsen, M. Ø., Rostrup, E., Wulff, S., Glenthøj, B., Ebdrup, B. H. (2016). Activitatea de recompensă striatală și modificarea greutății asociată cu antipsihotice la pacienții cu schizofrenie care urmează un tratament inițial. JAMA Psychiatry 73, 121-128. doi: 10.1001/jamapsychiatry.2015.2582
PubMed Abstract | CrossRef Full Text | Google Scholar
Pawlowski, M., Abshir-Ahmed, Y., Beitinger, P., Steiger, A. (2018). S241. Investigarea mecanismului de creștere a apetitului după Olanzapină prin sLORETA în timpul somnului. Biol. Psychiatry 83, S441-S442.
Google Scholar
Perez-Cruzado, D., Cuesta-Vargas, A., Vera-Garcia, E., Mayoral-Cleries, F. (2018). Medicamente și activitate fizică și fitness fizic în boli mintale severe. Psychiatry Res. 267, 19-24. doi: 10.1016/j.psychres.2018.05.055
PubMed Abstract | Ref Full Text | Google Scholar
Poyurovsky, M., Fuchs, C., Pashinian, A., Levi, A., Faragian, S., Maayan, R., et al. (2007). Efectul atenuant al reboxetinei asupra apetitului și creșterii în greutate la pacienții cu schizofrenie tratați cu olanzapină: un studiu dublu-orb controlat cu placebo. Psychopharmacology 192, 441-448. doi: 10.1007/s00213-007-0731-1
PubMed Abstract | CrossRef Full Text | Google Scholar
Roerig, J. L., Mitchell, J. E., de Zwaan, M., Crosby, R. D., Gosnell, B. A., Steffen, K. J., et al. (2005). O comparație a efectelor olanzapinei și risperidonei versus placebo asupra comportamentelor alimentare. J. Clin. Psychopharmacol. 25, 413-418. doi: 10.1097/01.jcp.0000177549.36585.29
PubMed Abstract | CrossRef Full Text | Google Scholar
Sentissi, O., Epelbaum, J., Olie, J. P., Poirier, M. F. (2008). Nivelurile de leptină și grelină la pacienții cu schizofrenie în timpul tratamentului cu diferite antipsihotice: o revizuire. Schizophr. Bull. 34, 1189-1199. doi: 10.1093/schbul/sbm141
PubMed Abstract | Full CrossRef Text | Google Scholar
Stip, E., Lungu, O. V., Anselmo, K., Letourneau, G., Mendrek, A., Stip, B., et al. (2012). Modificări neuronale asociate cu procesarea informațiilor despre apetit la pacienții schizofrenici după 16 săptămâni de tratament cu olanzapină. Transl. Psychiatry 2, e128. doi: 10.1038/tp.2012.53
PubMed Abstract | Full Text | Google Scholar
Sweeney, P., Li, C., Yang, Y. (2017). Rolul de suprimare a apetitului al neuronilor glutamatergici septali mediali. Proc. Natl. acad. Sci. 114, 13816-13821. doi: 10.1073/pnas.1707228114
CrossRef Full Text | Google Scholar
Tan, L., Liu, J., Liu, X., Liu, X., Chen, J., Yan, Z., Yang, H., et al. (2009). Cercetarea clinică a Olanzapinei pentru prevenirea grețurilor și vărsăturilor induse de chimioterapie. J. Exp. Clin. Cancer Res. 28, 131. doi: 10.1186/1756-9966-28-131
PubMed Abstract | Full CrossRef Full Text | Google Scholar
Wu, R.-R., Zhao, J.-P., Jin, H., Shao, P., Fang, M.-S., Guo, X.-F., et al. (2008). Intervenția asupra stilului de viață și metformină pentru tratamentul creșterii în greutate induse de antipsihotice: un studiu controlat randomizat. Jama 299, 185-193. doi: 10.1001/jama.2007.56-b
PubMed Abstract | Text integral | Google Scholar
Wu, R., Zhang, F., Gao, K., Ou, J., Shao, P., Jin, H., et al. (2016). Tratamentul cu metformină al dislipidemiei induse de antipsihotice: o analiză a două studii randomizate, controlate cu placebo. Mol. Psychiatry 21, 1537. doi: 10.1038/mp.2015.221
PubMed Abstract | Text integral | Google Scholar
.




