Porušení oktetového pravidla
Výjimka 2: neúplné oktety
Druhou výjimkou z oktetového pravidla je situace, kdy je příliš málo valenčních elektronů, což vede k neúplnému oktetu. Existuje ještě více případů, kdy pravidlo oktetů neposkytuje nejsprávnější zobrazení molekuly nebo iontu. To je také případ neúplných oktetů. Druhy s neúplnými oktety jsou poměrně vzácné a obecně se vyskytují pouze v některých sloučeninách berylia, hliníku a boru včetně hydridů boru. Podívejme se na jeden takový hydrid, \(BH_3\) (boran).
Pokud bychom vytvořili Lewisovu strukturu pro \(BH_3\) podle základních strategií pro kreslení Lewisových struktur, pravděpodobně bychom dostali tuto strukturu (obrázek 3):
Problémem této struktury je, že bor má neúplný oktet; má kolem sebe pouze šest elektronů. Atomy vodíku mohou mít přirozeně pouze 2 elektrony v nejvzdálenější slupce (jejich verze oktetu), a proto nemají žádné volné elektrony pro vytvoření dvojné vazby s bórem. Lze se domnívat, že neschopnost této struktury vytvořit úplný oktet musí znamenat, že tato vazba by měla být iontová, nikoli kovalentní. Elektronegativita boru je však velmi podobná elektronegativitě vodíku, což znamená, že ve vazbě mezi vodíkem a borem je pravděpodobně jen velmi málo iontového charakteru, a proto je tato Lewisova struktura, i když nesplňuje pravidlo oktetů, pravděpodobně nejlepší možnou strukturou pro znázornění BH3 pomocí Lewisovy teorie. Jednou z věcí, která může vysvětlovat neúplný oktet BH3, je to, že se běžně jedná o přechodný druh, který vzniká dočasně v reakcích, které zahrnují více kroků.
Podívejme se na jinou situaci neúplného oktetu, která se týká boru, BF3 (bórtrifluorin). Stejně jako u BH3 vytvoří počáteční nákres Lewisovy struktury BF3 strukturu, ve které má bór kolem sebe pouze šest elektronů (obrázek 4).
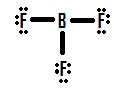
Podíváte-li se na obrázek 4, vidíte, že atomy fluoru mají další osamělé páry, které mohou využít k vytvoření dalších vazeb s bórem, a mohli byste si myslet, že stačí vytvořit jeden osamělý pár do vazby a struktura bude správná. Pokud přidáme jednu dvojnou vazbu mezi borem a jedním z fluorů, dostaneme následující Lewisovu strukturu (obrázek 5):
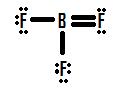
Každý fluor má osm elektronů a atom boru jich má také osm! Každý atom má dokonalý oktet, že? Ne tak rychle. Musíme prozkoumat formální náboje této struktury. Fluor, který sdílí dvojnou vazbu s bórem, má kolem sebe šest elektronů (čtyři ze svých dvou osamělých párů elektronů a po jednom ze dvou vazeb s bórem). To je o jeden elektron méně než počet valenčních elektronů, které by měl přirozeně (prvky sedmé skupiny mají sedm valenčních elektronů), takže má formální náboj +1. Dva flouriny, které sdílejí jednoduché vazby s bórem, mají kolem sebe sedm elektronů (šest ze svých tří osamělých párů a jeden z jednoduchých vazeb s bórem). To je stejné množství jako počet valenčních elektronů, které by měly samy o sobě, takže oba mají formální náboj nula. A konečně bór má kolem sebe čtyři elektrony (jeden z každé ze svých čtyř vazeb sdílených s fluorem). To je o jeden elektron více, než je počet valenčních elektronů, které by měl bór sám o sobě, a proto má bór formální náboj -1.
Tuto strukturu podporuje skutečnost, že experimentálně zjištěná délka vazby mezi bórem a fluorem v BF3 je menší, než by bylo typické pro jednoduchou vazbu (viz Řád a délky vazeb). Tato struktura však odporuje jednomu z hlavních pravidel formálních nábojů: Ve struktuře znázorněné na obrázku 5 se však kladný formální náboj nachází na fluoru, který je nejen elektronegativnějším prvkem ve struktuře, ale i elektronegativnějším prvkem v celé periodické tabulce (\(\chi=4,0\)). Naproti tomu bór s mnohem nižší elektronegativitou 2,0 má v této struktuře záporný formální náboj. Tento nesoulad formálního náboje a elektronegativity znemožňuje tuto strukturu s dvojitou vazbou.
Velký rozdíl elektronegativity zde však na rozdíl od BH3 znamená významné polární vazby mezi borem a fluorem, což znamená, že tato molekula má vysoký iontový charakter. To naznačuje možnost polojónové struktury, jak je vidět na obrázku 6:

Žádná z těchto tří struktur není v tomto případě „správnou“ strukturou. „Nejsprávnější“ strukturou je s největší pravděpodobností rezonance všech tří struktur: struktury s neúplným oktetem (obrázek 4), struktury s dvojnou vazbou (obrázek 5) a struktury s iontovou vazbou (obrázek 6). Nejvíce k tomu pravděpodobně přispívá struktura s neúplným oktetem (vzhledem k tomu, že obrázek 5 je v podstatě nemožný a obrázek 6 neodpovídá chování a vlastnostem BF3). Jak vidíte, i když existují jiné možnosti, neúplné oktety mohou nejlépe znázorňovat molekulovou strukturu.
Jako poznámku na okraj je důležité poznamenat, že BF3 se často váže s iontem F- za vzniku BF4-, místo aby zůstal jako BF3. Tato struktura doplňuje oktet boru a je v přírodě běžnější. To je příkladem skutečnosti, že neúplné oktety jsou vzácné a jiné konfigurace jsou obvykle výhodnější, včetně vazby s dalšími ionty jako v případě BF3 .
Příklad:
Nakreslete Lewisovu strukturu pro trifluorid boru (BF3).
Roztok
1. Přidejte elektrony (3*7) + 3 = 24
2. Nakreslete spojnice:
3. Přidejte oktety k vnějším atomům:
4. Přidejte další elektrony (24-24=0) k centrálnímu atomu:
5. Přidejte další elektrony (24-24=0) k centrálnímu atomu. Má centrální elektron oktet?“
- NE. Má 6 elektronů
- Přidejte násobnou vazbu (dvojnou vazbu), abyste zjistili, zda centrální atom může dosáhnout oktetu:
6. Centrální bór má nyní oktet (vznikly by tři rezonanční Lewisovy struktury)
Ještě…
- V této struktuře s dvojnou vazbou sdílí atom fluoru s bórem další elektrony.
- Fluor by měl částečný náboj „+“ a bor částečný náboj „-„, to je v rozporu s elektronegativitou fluoru a boru.
- Takže struktura BF3 s jednoduchými vazbami a 6 valenčními elektrony kolem centrálního boru je nejpravděpodobnější struktura
- BF3 silně reaguje se sloučeninami, které mají nesdílený pár elektronů, který může být využit k vytvoření vazby s borem:




