Overtrædelser af oktetreglen
Udtagelse 2: Ufuldstændige oktetter
Den anden undtagelse til oktetreglen er, når der er for få valenselektroner, hvilket resulterer i en ufuldstændig oktet. Der er endnu flere tilfælde, hvor oktetreglen ikke giver den mest korrekte afbildning af et molekyle eller en ion. Dette er også tilfældet med ufuldstændige oktetter. Arter med ufuldstændige oktetter er ret sjældne og findes generelt kun i nogle beryllium-, aluminium- og borforbindelser, herunder borhydriderne. Lad os tage et kig på et sådant hydrid, \(BH_3\) (boran).
Hvis man skulle lave en Lewis-struktur for \(BH_3\) efter de grundlæggende strategier for tegning af Lewis-strukturer, ville man sandsynligvis komme frem til denne struktur (figur 3):
Problemet med denne struktur er, at bor har en ufuldstændig oktet; det har kun seks elektroner omkring sig. Brintatomer kan naturligvis kun have kun 2 elektroner i deres yderste skal (deres version af en oktet), og som sådan er der ingen ekstra elektroner til at danne en dobbeltbinding med bor. Man kunne formode, at denne strukturs manglende evne til at danne komplette oktetter må betyde, at denne binding bør være ionisk i stedet for kovalent. Bor har imidlertid en elektronegativitet, der er meget lig brint, hvilket betyder, at der sandsynligvis er meget lidt ionisk karakter i bindingerne mellem brint og bor, og som sådan er denne Lewis-struktur, selv om den ikke opfylder oktetreglen, sandsynligvis den bedst mulige struktur til at afbilde BH3 med Lewis-teorien. En af de ting, der kan forklare BH3’s ufuldstændige oktet, er, at det almindeligvis er en overgangsart, der dannes midlertidigt i reaktioner, der involverer flere trin.
Lad os tage et kig på en anden ufuldstændig oktet-situation, der omhandler bor, BF3 (Boron trifluorine). Ligesom med BH3 vil den indledende tegning af en Lewis-struktur af BF3 danne en struktur, hvor bor kun har seks elektroner omkring sig (figur 4).
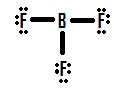
Hvis man ser på figur 4, kan man se, at fluoratomerne besidder ekstra ensomme par, som de kan bruge til at lave yderligere bindinger med bor, og man kunne tro, at man blot skal lave et enkelt ensomme par om til en binding, så vil strukturen være korrekt. Hvis vi tilføjer en dobbeltbinding mellem bor og en af fluorinerne får vi følgende Lewis-struktur (figur 5):
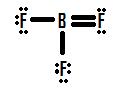
Hver fluor har otte elektroner, og boratomet har også otte! Hvert atom har en perfekt oktet, ikke sandt? Ikke så hurtigt. Vi må undersøge de formelle ladninger i denne struktur. Fluoren, der deler en dobbeltbinding med bor, har seks elektroner omkring sig (fire fra dets to ensomme elektronpar og en fra hver af dets to bindinger med bor). Det er én elektron mindre end det antal valenselektroner, det ville have naturligt (grundstoffer i gruppe 7 har syv valenselektroner), så det har en formel ladning på +1. De to flouriner, der deler enkeltbindinger med bor, har syv elektroner omkring sig (seks fra deres tre ensomme par og en fra deres enkeltbindinger med bor). Dette er det samme antal som det antal valenselektroner, de ville have hver for sig, så de har begge en formel ladning på nul. Endelig har bor fire elektroner omkring sig (en fra hver af de fire bindinger, som det deler med fluor). Dette er én elektron mere end det antal valenselektroner, som bor ville have alene, og som sådan har bor en formel ladning på -1.
Denne struktur understøttes af, at den eksperimentelt bestemte bindingslængde af bor til fluor-bindingerne i BF3 er mindre end det, der ville være typisk for en enkeltbinding (se Bindingsorden og bindingslængder). Denne struktur er imidlertid i modstrid med en af de vigtigste regler for formelle ladninger: Negative formelle ladninger skal findes på de(t) mere elektronegative atom(er) i en binding, men i den struktur, der er afbildet i figur 5, findes en positiv formel ladning på fluor, som ikke blot er det mest elektronegative element i strukturen, men også det mest elektronegative element i hele det periodiske system (\(\chi=4,0\)). Bor på den anden side, med den meget lavere elektronegativitet på 2,0, har den negative formelle ladning i denne struktur. Denne uoverensstemmelse mellem formel ladning og elektronegativitet gør denne dobbeltbindingsstruktur umulig.
Den store elektronegativitetsforskel her, i modsætning til i BH3, betyder imidlertid, at der er betydelige polære bindinger mellem bor og fluor, hvilket betyder, at der er en høj ionisk karakter i dette molekyle. Dette tyder på muligheden for en semi-ionisk struktur som den, der ses i figur 6:

Ingen af disse tre strukturer er den “rigtige” struktur i dette tilfælde. Den mest “korrekte” struktur er højst sandsynligt en resonans af alle tre strukturer: den med den ufuldstændige oktet (figur 4), den med dobbeltbindingen (figur 5) og den med ionbindingen (figur 6). Den mest bidragende struktur er sandsynligvis den ufuldstændige oktetstruktur (fordi figur 5 stort set er umulig, og fordi figur 6 ikke stemmer overens med BF3’s adfærd og egenskaber). Som man kan se, selv når der findes andre muligheder, kan ufuldstændige oktetter bedst skildre en molekylær struktur.
Som en sidebemærkning er det vigtigt at bemærke, at BF3 ofte binder sig med en F- ion for at danne BF4- i stedet for at forblive som BF3. Denne struktur fuldender borets oktet, og den er mere almindelig i naturen. Dette illustrerer det faktum, at ufuldstændige oktetter er sjældne, og at andre konfigurationer typisk er mere gunstige, herunder binding med yderligere ioner som i tilfældet BF3 .
Eksempel: \(BF_3\)
Tegn Lewis-strukturen for bor-trifluorid (BF3).
Løsning
1. Tilføj elektroner (3*7) + 3 = 24
2. Tegn forbindelsesled:
3. Tilføj oktetter til de ydre atomer:
4. Tilføj ekstra elektroner (24-24=0) til det centrale atom:
5. Har den centrale elektron oktet?
- NEJ. Det har 6 elektroner
- Føj en flerbinding (dobbeltbinding) til for at se, om det centrale atom kan opnå en oktet:
- I denne struktur med en dobbeltbinding deler fluoratomet ekstra elektroner med boret.
- Fluoren ville have en “+” partiel ladning, og boret en “-” partiel ladning, dette er uforeneligt med fluorets og borets elektronegativitet.
- Dermed er BF3’s struktur med enkeltbindinger og 6 valenselektroner omkring det centrale bor den mest sandsynlige struktur
- BF3 reagerer kraftigt med forbindelser, der har et ikke-delt elektronpar, som kan bruges til at danne en binding med boret:
6. Det centrale bor har nu en oktet (der ville være tre resonans-Lewis-strukturer)
Hvorimod…




