Hämoglobin und seine Messung
Die normale Funktion der Zellen hängt von einer kontinuierlichen Versorgung mit Sauerstoff ab. Wenn der Sauerstoff beim Zellstoffwechsel verbraucht wird, entsteht Kohlendioxid.
Eine der Hauptfunktionen des Blutes besteht darin, den in der Atemluft enthaltenen Sauerstoff (O2) von den Lungen zu jeder Zelle im Körper zu transportieren und das Kohlendioxid (CO2) von den Zellen zu den Lungen zu transportieren, damit es mit der Ausatemluft aus dem Körper ausgeschieden werden kann.
Diese lebenswichtigen Gastransportfunktionen sind von dem in den Erythrozyten (roten Blutkörperchen) enthaltenen Protein Hämoglobin abhängig. Jede der 5 × 1010 Erythrozyten, die normalerweise in 1 ml Blut vorhanden sind, enthält etwa 280 Millionen Hämoglobinmoleküle.
1. HÄMOGLOBIN STRUKTUR UND FUNKTION
Das Hämoglobinmolekül (Hb) ist ungefähr kugelförmig und besteht aus zwei Paaren ungleicher Untereinheiten (ABBILDUNG 1).
Jede der Untereinheiten ist eine gefaltete Polypeptidkette (der Globin-Teil), an die eine Häm-Gruppe (abgeleitet von Porphyrin) gebunden ist.
Im Zentrum jeder Häm-Gruppe befindet sich ein einzelnes Eisenatom im eisenhaltigen (Fe2+) Zustand. Häm ist also ein Metallo-Porphyrin, das übrigens für die rote Farbe des Blutes verantwortlich ist.
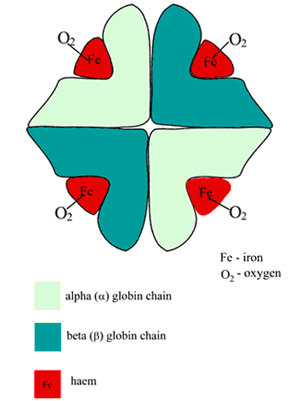
ABBILD 1: Schema der Struktur des sauerstoffhaltigen Hämoglobins (HbA)
Die sauerstoffbindende Stelle des Hb ist die Häm-Tasche, die in jeder der vier Polypeptidketten vorhanden ist; ein einzelnes Sauerstoffatom bildet an jeder dieser Stellen eine reversible Bindung mit dem Eisen, so dass ein Molekül Hb vier Sauerstoffmoleküle bindet; das Produkt ist Oxyhämoglobin (O2Hb).
Die Funktion des Hb als Sauerstofflieferant, d. h. seine Fähigkeit, Sauerstoff in der Lunge „aufzunehmen“ und an die Gewebezellen „abzugeben“, wird durch winzige Konformationsänderungen in der quaternären Struktur des Hämoglobinmoleküls ermöglicht, die die Affinität der Häm-Tasche für Sauerstoff verändern. Hb hat zwei quaternäre Strukturzustände: den Desoxy-Zustand (geringe Sauerstoffaffinität) und den Oxy-Zustand (hohe Sauerstoffaffinität).
Eine Reihe von Umweltfaktoren bestimmt den quaternären Zustand von Hb und damit seine relative Sauerstoffaffinität. Die Mikroumgebung in der Lunge begünstigt den quartären Oxy-Zustand, so dass Hb hier eine hohe Affinität zu Sauerstoff aufweist.
Im Gegensatz dazu führt die Mikroumgebung der Gewebe zu einer Konformationsänderung der Hb-Struktur, die seine Affinität für Sauerstoff verringert, so dass der Sauerstoff an die Gewebezellen abgegeben werden kann.
1.1. HÄMOGLOBIN UND KOHLENDIOXID-Eliminierung
Eine geringe Menge (bis zu 20 %) CO2 wird lose an die N-terminale Aminosäure der vier Globin-Polypeptid-Einheiten des Hämoglobins gebunden aus dem Gewebe in die Lunge transportiert; das Produkt dieser Kombination ist Carbamino-Hämoglobin. Das meiste CO2 wird jedoch als Bikarbonat im Blutplasma transportiert.
Die für diese Art des CO2-Transports notwendige Umwandlung von CO2 in Bicarbonat durch die Erythrozyten führt zur Bildung von Wasserstoffionen (H+). Diese Wasserstoffionen werden durch desoxygeniertes Hämoglobin gepuffert.
Die Rolle des Hämoglobins beim Transport von Sauerstoff und Kohlendioxid ist in den ABBILDUNGEN 2a und 2b zusammengefasst.
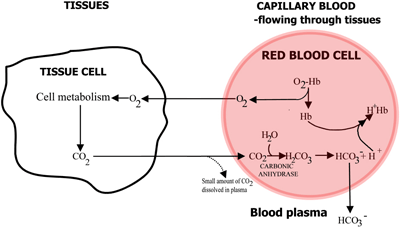
Abbildung 2a: GEWEBE O2 diffundiert vom Blut ins Gewebe, CO2 diffundiert vom Gewebe ins Blut
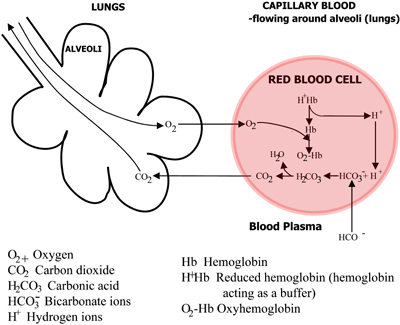
Abbildung 2b: LUNGEN CO2 diffundiert aus dem Blut in die Lungen, O2 diffundiert aus den Lungen in das Blut
Im Kapillarblut, das durch die Gewebe fließt, wird Sauerstoff aus dem Hämoglobin freigesetzt und gelangt in die Gewebezellen. Kohlendioxid diffundiert aus den Gewebezellen in die Erythrozyten, wo das Erythrozytenenzym Kohlensäureanhydrase seine Reaktion mit Wasser zu Kohlensäure ermöglicht.
Die Kohlensäure dissoziiert zu Bicarbonat (das in das Blutplasma übergeht) und Wasserstoffionen, die sich mit dem nun desoxygenierten Hämoglobin verbinden. Das Blut fließt in die Lunge, und in den Kapillaren der Lungenbläschen kehren sich die oben genannten Wege um. Bikarbonat gelangt in die Erythrozyten und verbindet sich hier mit den vom Hämoglobin freigesetzten Wasserstoffionen zu Kohlensäure.
Diese dissoziiert zu Kohlendioxid und Wasser. Das Kohlendioxid diffundiert aus dem Blut in die Alveolen der Lunge und wird mit der Ausatemluft ausgeschieden. Währenddessen diffundiert der Sauerstoff aus den Alveolen in das Kapillarblut und verbindet sich mit dem Hämoglobin.
1.2. HÄMOGLOBIN, DAS KEIN OXYGEN BINDEN KANN
Obwohl normalerweise nur in Spuren vorhanden, gibt es drei Arten von Hämoglobin: Methämoglobin (MetHb oder Hi), Sulfathämoglobin (SHb) und Carboxyhämoglobin (COHb), die keinen Sauerstoff binden können.
Sie sind daher funktionell unzureichend, und erhöhte Mengen einer dieser Hämoglobinarten, in der Regel das Ergebnis einer Exposition gegenüber bestimmten Arzneimitteln oder Umweltgiften, können die Sauerstoffversorgung ernsthaft beeinträchtigen.
Eine umfassende Darstellung der Hämoglobinstruktur und -funktion ist in der Referenz enthalten.
ctHb, die Gesamthämoglobinkonzentration wird in der Regel als die Summe von sauerstoffhaltigem Hämoglobin, desoxygeniertem Hämoglobin, Carboxyhämoglobin und Methämoglobin definiert.
KLINISCHE Nützlichkeit der ctHb-Messung
Der Hauptgrund für die Messung des ctHb ist die Erkennung einer Anämie und die Bewertung ihres Schweregrades.
Anämie kann als eine Verringerung der Sauerstofftransportkapazität des Blutes aufgrund einer Verringerung der Erythrozytenzahl und/oder einer Verringerung des ctHb-Wertes definiert werden, so dass eine Anämie vorliegt, wenn der ctHb-Wert unter der unteren Grenze des (normalen) Referenzbereichs liegt (TABELLE I). Je niedriger der ctHb-Wert ist, desto schwerer ist die Anämie.
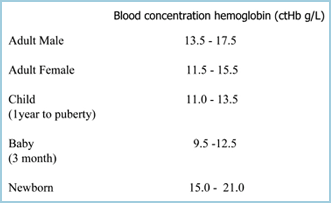
TABELLE I: ctHb-Referenzbereiche (Ref 2)
Anämie ist keine Krankheit, sondern eine Folge oder ein Zeichen einer Krankheit. Der Grund, warum der ctHb-Wert ein so häufig angeforderter Bluttest ist, liegt darin, dass Anämie ein Merkmal einer Reihe von Krankheiten ist, von denen viele relativ häufig sind (Tabelle II).
Häufige Symptome, von denen die meisten unspezifisch sind, sind: Blässe, Müdigkeit und Lethargie, Kurzatmigkeit – besonders bei Anstrengung, Schwindel und Ohnmacht, Kopfschmerzen, Verstopfung und erhöhter Pulsschlag, Herzklopfen, Tachykardie.

TABELLE II: Einige der klinischen Zustände, die mit Anämie assoziiert sind
Das Fehlen dieser Symptome schließt eine Anämie nicht aus; viele leicht anämische Personen bleiben asymptomatisch, insbesondere wenn sich die Anämie langsam entwickelt hat.
2.2. POLYZYTHEMIE
Während eine Anämie durch einen verminderten ctHb-Wert gekennzeichnet ist, weist ein erhöhter ctHb-Wert auf eine Polyzythämie hin. Polyzythämie entsteht als Reaktion auf einen physiologischen oder pathologischen Zustand, bei dem das Blut weniger Sauerstoff enthält als normal (Hypoxämie).
Der Körper reagiert auf die Hypoxämie mit einer vermehrten Produktion von Erythrozyten, um die Sauerstoffzufuhr zu erhöhen, und infolgedessen ist der ctHb-Wert erhöht. Diese so genannte sekundäre Polyzythämie ist Teil der physiologischen Anpassung an die Höhe und kann ein Merkmal einer chronischen Lungenerkrankung sein.
Primäre Polyzythämie ist eine viel seltenere bösartige Erkrankung des Knochenmarks, die so genannte Polyzythämia vera, die durch eine unkontrollierte Produktion aller Blutzellen, einschließlich der Erythrozyten, gekennzeichnet ist. Polyzythämie, ob sekundär oder primär, ist im Allgemeinen viel seltener als Anämie.
3.1. GESCHICHTLICHE PERSPEKTIVE
Der erste klinische Test zur Hb-Messung, der vor mehr als einem Jahrhundert entwickelt wurde, bestand darin, einem abgemessenen Blutvolumen Tropfen destillierten Wassers hinzuzufügen, bis dessen Farbe der eines künstlichen Farbstandards entsprach.
Eine spätere Modifikation bestand darin, das Blut zunächst mit Kohlengas (Kohlenmonoxid) zu sättigen, um das Hämoglobin in das stabilere Carboxyhämoglobin umzuwandeln. Die moderne Hämoglobinometrie stammt aus den 1950er Jahren, nachdem die Spektralphotometrie und die Hämiglobincyanid-Methode (Cynamethemoglobin) entwickelt wurden.
Diese und andere Methoden wurden für den Einsatz in automatischen Hämatologie-Analysegeräten angepasst. In den letzten zwei Jahrzehnten konzentrierten sich die Fortschritte auf die Entwicklung von Methoden, die eine Point-of-Care-Prüfung (POCT) von Hämoglobin ermöglichen.
Dieser Abschnitt befasst sich zunächst mit der Betrachtung einiger der derzeit im Labor verwendeten Methoden und dann mit den außerhalb des Labors verwendeten POCT-Methoden.
3.2. HEMIGLOBINZYANID – EINE SPECTROPHOTOMETRISCHE METHODE
Nahe 40 Jahre, nachdem sie erstmals vom Internationalen Komitee für Normung in der Hämatologie (ICSH) als Referenzmethode für die Hämoglobinmessung angenommen wurde, ist der Hämiglobin-Zyanid-Test (HiCN) nach wie vor die empfohlene Methode des ICSH, anhand derer alle neuen ctHb-Methoden beurteilt und standardisiert werden.
Die folgende ausführliche Betrachtung spiegelt seine anhaltende Bedeutung sowohl als Referenz- als auch als Routine-Labormethode wider.
3.2.1. Testprinzip
Blut wird in einer Lösung verdünnt, die Kaliumferricyanid und Kaliumcyanid enthält. Kaliumferricyanid oxidiert das Eisen im Häm in den Eisenstatus und bildet Methämoglobin, das durch Kaliumcyanid in Hämiglobincyanid (HiCN) umgewandelt wird.
HiCN ist ein stabiles farbiges Produkt, das in Lösung ein Absorptionsmaximum bei 540 nm aufweist und streng dem Beer-Lambert’schen Gesetz gehorcht. Die Absorption der verdünnten Probe bei 540 nm wird mit der Absorption bei derselben Wellenlänge einer HiCN-Standardlösung verglichen, deren äquivalente Hämoglobinkonzentration bekannt ist.
Die meisten Hämoglobinderivate (Oxyhämoglobin, Methämoglobin und Carboxyhämoglobin, aber nicht Sulfathämoglobin) werden in HiCN umgewandelt und daher mit dieser Methode gemessen.
3.2.1.1. Reagenzverdünnungsmittel (modifizierte Drabkin-Lösung)
| Kaliumferricyanid (K3Fe(CN)6) | 200 mg |
| Kaliumcyanid (KCN) | 50 mg |
| Kaliumdihydrogenphosphat (KH2 PO4) | 140 mg |
| Nichtionisches Detergenz (z.z. B. Triton X-100) | 1 mL |
| Auf 1000 mL in destilliertem Wasser verdünnt |
3.2.1.2. Manuelle Methode
25 µl Blut werden zu 5,0 mL Reagenz hinzugefügt, gemischt und 3 Minuten stehen gelassen. Die Absorption wird bei 540 nm im Vergleich zu einem Reagenzleerwert gemessen. Die Absorption des HiCN-Standards wird auf die gleiche Weise gemessen.
3.2.1.3. ICSH-HiCN-Standard
Der Hauptvorteil dieser Methode besteht darin, dass es eine HiCN-Standardlösung gibt, die nach sehr präzisen Kriterien hergestellt und einem Konzentrationswert zugeordnet wird, die vom Internationalen Rat für Standardisierung in der Hämatologie (ICSH) festgelegt und regelmäßig überprüft werden.
Diese internationale Standardlösung ist das primäre Kalibriermittel für die kommerziellen Standardlösungen, die in klinischen Labors auf der ganzen Welt verwendet werden. Somit verwenden alle, die die HiCN-Standardisierung verwenden, effektiv denselben Standard, dessen Wert genauestens validiert wurde.
3.2.1.4. Störungen
Störungen durch Proteine, Lipide und zelluläre Stoffe sind ein potenzielles Problem bei der spektralphotometrischen Bestimmung aller Blutbestandteile, einschließlich Hämoglobin.
Durch die große Verdünnung (1:251) der Probe wird das Problem weitgehend beseitigt, doch können bei Patienten, deren Plasmaproteinkonzentration besonders hoch ist, fälschlich erhöhte ctHb-Ergebnisse auftreten.
Stark lipämische Proben und solche, die sehr viele weiße Zellen (Leukozyten) enthalten, können den ctHb-Wert durch einen ähnlichen Mechanismus ebenfalls artefaktisch erhöhen.
3.2.1.5. Vorteile von HiCN
- Internationaler Standard – genau
- Einfach an automatische Hämatologie-Analysegeräte angepasst; daher reproduzierbar (geringe SD und CV – innerhalb der Charge typischerweise CV
- Gut etabliert und gründlich untersucht – ICSH empfohlen
- Ungünstiges Reagenz
3.2.1.6. Nachteile von HiCN
- Manuelle Methode erfordert genaues Pipettieren und Spektralphotometer
- Reagenz (Cyanid) gefährlich
- Das oben Genannte schränkt die Verwendung außerhalb des Labors ein
- Anfällig für Interferenzen durch erhöhte Lipide, Plasmaproteine und Leukozytenzahlen
- Unterscheidet nicht zwischen Hämoglobinderivaten, die keine Sauerstofftransportkapazität haben (MetHb, COHb, SHb). Daher kann die Sauerstofftransportkapazität des Blutes überschätzt werden, wenn diese in abnormalen (mehr als Spuren) Mengen vorhanden sind.
3.3. ALTERNATIVE (CYANID-freie) LABORMETHODEN
Natriumlaurylsulfat (SLS) ist ein Tensid, das sowohl Erythrozyten auflöst als auch schnell einen Komplex mit dem freigesetzten Hämoglobin bildet. Das Produkt SLS-MetHb ist für einige Stunden stabil und hat ein charakteristisches Spektrum mit einem Absorptionsmaximum bei 539 nm .
Der Komplex gehorcht dem Beer-Lambert’schen Gesetz, so dass eine genaue lineare Korrelation zwischen der Hb-Konzentration und der Absorption von SLS-MetHb besteht.
Bei der Methode werden einfach 25 µL Blut mit 5,0 mL einer 2,08-mmol/L-Lösung von SLS (gepuffert auf einen pH-Wert von 7,2) gemischt und die Absorption bei 539 nm gemessen. Die Ergebnisse des ctHb mit der SLS-Hb-Methode korrelieren nachweislich sehr gut (r = 0,998) mit der HiCN-Referenzmethode.
Die Methode wurde für automatisierte Hämatologie-Analysegeräte angepasst und ist in Bezug auf Genauigkeit und Präzision ebenso zuverlässig wie automatisierte HiCN-Methoden. Ein großer Vorteil ist, dass das Reagenz nicht toxisch ist. Es ist auch weniger anfällig für Störungen durch Lipämie und erhöhte Leukozytenkonzentration .
Die Langzeitinstabilität von SDS-MetHb schließt seine Verwendung als Standard aus, so dass die Methode mit Blut kalibriert werden muss, dessen ctHb mit der Referenz-HiCN-Methode bestimmt wurde.
3.3.2. Azid-Methämoglobin-Methode
Diese Methode basiert auf der Umwandlung von Hämoglobin in ein stabiles farbiges Produkt Azid-Methämoglobin, das ein nahezu identisches Absorptionsspektrum wie HiCN aufweist.
Das bei dieser Methode verwendete Reagenz ist dem bei der HiCN-Referenzmethode verwendeten sehr ähnlich, wobei das giftigere Kaliumcyanid durch Natriumazid ersetzt wird. Wie bei der HiCN-Methode wird Hämoglobin durch Kaliumferricyanid in Methämoglobin umgewandelt; Azid bildet dann einen Komplex mit Methämoglobin.
ctHb-Ergebnisse dieser Methode sind mit den Ergebnissen der HiCN-Referenzmethode vergleichbar; dies ist eine akzeptable alternative manuelle Methode. Das explosive Potenzial von Natriumazid verhindert jedoch die Verwendung auf automatischen Hämatologie-Analysegeräten. Die Azid-MetHb-Reaktion wurde für POCT-Hämoglobinometer angepasst.
3.4. MESSUNG von ctHb AUSSERHALB DES LABORS
Die hier betrachteten POCT-Methoden sind:
- Portable Hämoglobinometer
- CO-Oximetrie – eine Methode, die in POCT-Blutgasanalysatoren verwendet wird
- WHO-Farbskala
3.4.1. Tragbare Hämoglobinometer
Tragbare Hämoglobinometer wie das HemoCue-B ermöglichen eine genaue Bestimmung des Hämoglobins am Krankenbett. Sie sind im Wesentlichen Photometer, die die Messung der Farbintensität von Lösungen ermöglichen.
Die Einweg-Mikroküvette, in der diese Messungen durchgeführt werden, dient gleichzeitig als Reaktionsgefäß. Die Reagenzien, die sowohl für die Freisetzung von Hb aus den Erythrozyten als auch für die Umwandlung von Hb in ein stabiles farbiges Produkt erforderlich sind, befinden sich in getrockneter Form an den Wänden der Küvette.
Es ist lediglich erforderlich, eine kleine Probe (typischerweise 10 µl) Kapillar-, Venen- oder Arterienblut in die Mikroküvette zu geben und die Mikroküvette in das Gerät einzusetzen.
Das Gerät ist werkseitig mit dem HiCN-Standard vorkalibriert, und die Absorption der Testlösung wird automatisch in ctHb umgerechnet. Das Ergebnis wird in weniger als einer Minute angezeigt.
3.4.1.1. Vorteile moderner Hämoglobinometer sind
- Handlichkeit
- Batterie- oder Netzbetrieb, kann überall eingesetzt werden
- Kleines Probenvolumen (10 µL), das durch einen Stich in den Finger gewonnen wird
- Schnell (Ergebnis in 60 Sekunden)
- Bedienungsfreundlichkeit – kein Pipettieren
- Minimaler Schulungsaufwand für Nicht-Laborpersonal
- Standardisiert gegen HiCN – Ergebnisse vergleichbar mit denen aus dem Labor
- Korrektur der Trübung. In dieser Hinsicht sind die tragbaren Hämoglobinometer den meisten ctHb-Methoden überlegen.
Diese Technologie wurde in einer Reihe von Umgebungen umfassend evaluiert und die meisten Studien haben eine akzeptable Genauigkeit und Präzision im Vergleich zu Labormethoden bestätigt.
3.4.1.2. Nachteile
Einige Studien haben jedoch die Besorgnis geäußert, dass die Ergebnisse in den Händen von Nicht-Laborpersonal weniger zufriedenstellend sein könnten. Trotz der Einfachheit der Bedienung sind diese Geräte nicht vor Bedienungsfehlern gefeit, und eine wirksame Schulung ist unerlässlich.
Es gibt Hinweise darauf, dass die Ergebnisse aus Kapillarproben (Fingerprick) weniger genau sind als die Ergebnisse aus gut gemischten Kapillar- oder Venenproben, die in EDTA-Flaschen gesammelt wurden.
3.4.2. CO-Oximetrie
Ein CO-Oximeter ist ein spezialisiertes Spektralphotometer, dessen Name die ursprüngliche Anwendung widerspiegelt, nämlich die Messung von COHb und MetHb.
Viele moderne Blutgasanalysatoren verfügen über ein eingebautes CO-Oximeter, das die gleichzeitige Schätzung von ctHb während der Blutgasanalyse ermöglicht.
Die Messung von ctHb durch CO-Oximetrie beruht auf der Tatsache, dass Hämoglobin und alle seine Derivate farbige Proteine sind, die Licht bei bestimmten Wellenlängen absorbieren und somit ein charakteristisches Absorptionsspektrum aufweisen (ABBILDUNG 3).
Das Gesetz von Beer-Lambert besagt, dass die Absorption einer einzelnen Verbindung proportional zur Konzentration dieser Verbindung ist. Wenn die spektrale Charakteristik jeder absorbierenden Substanz in einer Lösung bekannt ist, können die Absorptionswerte der Lösung bei mehreren Wellenlängen verwendet werden, um die Konzentration jeder absorbierenden Substanz zu berechnen.
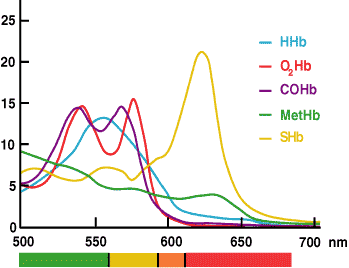
Abbildung 3.
Im CO-Oximeter werden Absorptionsmessungen einer hämolysierten Blutprobe bei mehreren Wellenlängen in dem Bereich, in dem Hämoglobinarten Licht absorbieren (520-620 nm), von der installierten Software zur Berechnung der Konzentration jedes der Hämoglobinderivate (HHb, O2Hb, MetHb und COHb) verwendet. ctHb ist die berechnete Summe dieser Derivate.
Der Bediener muss lediglich eine gut gemischte arterielle Blutprobe in das Blutgasanalysegerät/CO-Oximeter injizieren.
Die Probe oder ein Teil davon wird automatisch in die Messküvette des CO-Oximeters gepumpt, wo – entweder durch chemische oder physikalische Einwirkung – Erythrozyten lysiert werden, um Hämoglobin freizusetzen, das wie oben beschrieben spektroskopisch untersucht wird.
Die Ergebnisse werden zusammen mit den Blutgaswerten innerhalb von ein oder zwei Minuten angezeigt.
Verschiedene Studien haben bestätigt, dass die mit der CO-Oximetrie erzielten ctHb-Ergebnisse sich klinisch nicht signifikant von denen unterscheiden, die mit Referenzlaborverfahren ermittelt wurden. Die CO-Oximetrie stellt ein akzeptables Mittel zur dringenden Schätzung des ctHb in der Intensivpflege dar.
3.4.2.1. Zu den besonderen Vorteilen der CO-Oximetrie gehören
- Geschwindigkeit der Analyse
- Einfache Analyse
- Kleines Probenvolumen
- Keine Investitions- oder Verbrauchskosten, die über die für die Blutgasanalyse erforderlichen hinausgehen
- Zusätzliche Parameter (MetHb, COHb, O2Hb) gemessen
- Nicht beeinträchtigt durch hohe Anzahl weißer Blutkörperchen
3.4.3. WHO-Hämoglobin-Farbskala (HCS)
Dieser für die Weltgesundheitsorganisation (WHO) entwickelte Test mit geringem technischem Aufwand ist in den Industrieländern nur begrenzt anwendbar, hat aber große Bedeutung für die wirtschaftlich benachteiligten Länder der Dritten Welt, in denen Anämie am häufigsten vorkommt.
In Gebieten, in denen es keine Laboreinrichtungen und keine ausreichenden Mittel für die Finanzierung anspruchsvollerer POCT-Hämoglobinometer gibt, ist er praktisch die einzige Möglichkeit zur Bestimmung des ctHb-Wertes.
Der HCS-Test beruht auf dem einfachen Prinzip, dass die Farbe des Blutes eine Funktion des ctHb-Wertes ist. Ein Tropfen Blut wird auf Papier aufgesaugt und seine Farbe mit einer Tabelle mit sechs Rottönen verglichen, wobei jeder Farbton einem entsprechenden ctHb-Wert entspricht: der hellste 40 g/L und der dunkelste 140 g/L. Obwohl es im Prinzip sehr einfach ist, wurde bei der Entwicklung ein beträchtlicher Forschungs- und Technologieaufwand betrieben, um größtmögliche Genauigkeit und Präzision zu gewährleisten.
Ausführliche Versuche mit verschiedenen Papieren bildeten beispielsweise die Grundlage für die endgültige Wahl des Papiers für die Teststreifenmatrix, und die spektralphotometrische Analyse von Blut und Farbstoffmischungen wurde eingesetzt, um die bestmögliche Übereinstimmung zwischen der Farbe der Karte und der Farbe des Blutes bei jedem Referenz-ctHb-Wert zu erzielen.
3.4.3.1. Vorteile des HCS-Tests
- Ist einfach in der Anwendung – erfordert nur 30 Minuten Schulung
- Braucht keine Ausrüstung oder Strom
- Ist schnell – Ergebnis innerhalb von 1 Minute
- Erfordert nur eine Fingerstichprobe (Kapillarprobe)
- Ist sehr billig (etwa 0,12 USD pro Test)
3.4.3.2. Nachteile des HCS-Tests
Zuverlässige Ergebnisse hängen von der strikten Befolgung der Testanweisungen ab.
Häufige Fehler sind:
- Unzureichende oder zu viel Blut auf dem Teststreifen
- Ablesen des Ergebnisses zu spät (über 2 Minuten) oder zu früh (weniger als 30 Sekunden)
- Ablesen des Ergebnisses unter schlechten Lichtverhältnissen
Der HSC-Test hat eindeutig seine Grenzen. Im besten Fall kann er feststellen, dass der ctHb-Wert einer Patientenprobe innerhalb eines von sechs Konzentrationsbereichen liegt: 30-50 g/L, 50-70 g/L, 70-90 g/L, 90-110 g/L, 110-130 g/L oder 130-150 g/L. Dies reicht theoretisch aus, um alle Patienten mit Ausnahme der leichtesten Anämie zu identifizieren und einen Hinweis auf den Schweregrad zu geben.
Eine frühe Studie hat gezeigt, dass der Test in der Lage ist, eine Anämie zu erkennen (definiert als ctHb
ZUSAMMENFASSUNG
ctHb ist einer von zwei Parametern, die routinemäßig verwendet werden, um die Sauerstofftransportkapazität des Blutes zu beurteilen und damit die Diagnose einer Anämie und Polyzythämie zu stellen.
Der alternative Test, der Hämatokrit (Hct) oder das gepackte Zellvolumen (PCV), war Gegenstand eines früheren Artikels, in dem die Beziehung zwischen ctHb und Hct erörtert wurde. Der Schwerpunkt dieses Artikels liegt auf der Messung des ctHb.
Es wurden zahlreiche Methoden entwickelt, von denen die meisten auf der Messung der Farbe des Hämoglobins oder eines Hämoglobinderivats basieren. Für diesen kurzen Überblick war es unumgänglich, eine Auswahl zu treffen. Die zur Diskussion gestellten Methoden gehören zu den heute am häufigsten verwendeten.
Bei der Auswahl wurde versucht, die Bandbreite der gegenwärtig eingesetzten Technologien zu vermitteln und darzustellen, wie diese angewandt werden, um den klinischen Bedarf an ctHb in Umgebungen zu decken, die von verarmten Gebieten der Entwicklungsländer, in denen die medizinische Versorgung kaum Fuß fassen kann, bis hin zur High-Tech-Welt der modernen Intensivstation reichen.




