Hemoglobiini ja sen mittaaminen
Solujen normaali toiminta riippuu jatkuvasta hapen saannista. Kun happea kuluu solujen aineenvaihdunnassa, syntyy hiilidioksidia.
Veren pääasiallinen tehtävä on hengitysilmassa olevan hapen (O2) kuljettaminen keuhkoista elimistön jokaiseen soluun ja hiilidioksidin (CO2) kuljettaminen soluista keuhkoihin poistettavaksi elimistöstä uloshengitysilman mukana.
Nämä elintärkeät kaasunkuljetustoiminnot ovat riippuvaisia erytrosyyttien (punasolujen) sisältämästä proteiinista hemoglobiinista. Kukin 5 × 1010 erytrosyytistä, joita normaalisti on 1 ml:ssa verta, sisältää noin 280 miljoonaa hemoglobiinimolekyyliä.
1. HEMOGLOBIININ RAKENNE JA TOIMINTA
Hemoglobiinimolekyyli (Hb) on suurin piirtein pallomainen, ja se muodostuu kahdesta parista toisistaan poikkeavia alayksiköitä (KUVA 1).
Kumpikin alayksikkö on taitettu polypeptidiketju (globiinin osa), johon on kiinnittynyt (porfyriinistä peräisin oleva) hemiryhmä.
Kunkin heemiryhmän keskellä on yksi rauta-atomi rautatilassa (Fe2+). Näin ollen hemi on metallo-porfyriini, joka on muuten vastuussa veren punaisesta väristä.
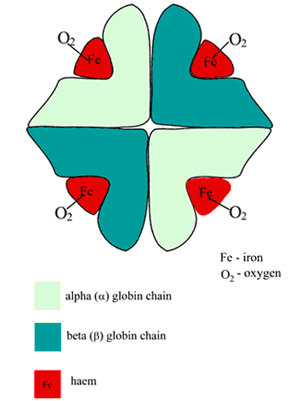
KUVA 1: Kaavio hapettuneen hemoglobiinin (HbA) rakenteesta
Hb:n happea sitova paikka on jokaisessa neljässä polypeptidiketjussa esiintyvä hemätasku; yksittäinen happiatomi muodostaa jokaisessa näissä paikoissa reversiibelin sidoksen rautapitoisen rauta-aineksen kanssa, joten Hb-molekyyli sitoo neljää happea sisältävää happimolekyyliä; tuotteena saadaan oksyhemoglobiiniä (oxyhemoglobin, O2Hb).
Hb:n hapen luovutustehtävä eli sen kyky ”hakea” happea keuhkoista ja ”luovuttaa” sitä kudossoluihin mahdollistuu hemoglobiinimolekyylissä tapahtuvien kvaternäärirakenteen pienien konformaatiomuutosten ansiosta, jotka muuttavat hemitaskun affiniteettia happea kohtaan. Hb:llä on kaksi kvaternääristä rakennetilaa: deoksitila (alhainen happiaffiniteetti) ja oksitila (korkea happiaffiniteetti).
Erilaiset ympäristötekijät määräävät Hb:n kvaternaarisen tilan ja siten sen suhteellisen happiaffiniteetin. Keuhkojen mikroympäristö suosii oksikvaternääristä tilaa, joten Hb:llä on täällä korkea affiniteetti happea kohtaan.
Kudosten mikroympäristö sen sijaan saa aikaan Hb:n rakenteessa konformaatiomuutoksen, joka vähentää sen affiniteettia happea kohtaan, jolloin happi pääsee vapautumaan kudossoluihin.
1.1. HEMOGLOBIINI JA HIILIDIOKSIDIN POISTO
Pieni määrä (jopa 20 %) hiilidioksidia kulkeutuu kudoksista keuhkoihin löyhästi sitoutuneena hemoglobiinin neljän globiinipolypeptidiyksikön N-terminaaliseen aminohappoon; tämän yhdistymisen tuotteena syntyy karbaminohemoglobiini. Suurin osa hiilidioksidista kulkeutuu kuitenkin bikarbonaattina veriplasmassa.
Tämän CO2-kuljetustavan edellyttämä CO2:n muuttaminen bikarbonaatiksi erytrosyytteissä johtaa vetyionien (H+) tuotantoon. Näitä vetyioneja puskuroi hapeton hemoglobiini.
Hemoglobiinin rooli hapen ja hiilidioksidin kuljetuksessa on esitetty yhteenvetona KUVIOISSA 2a ja 2b.
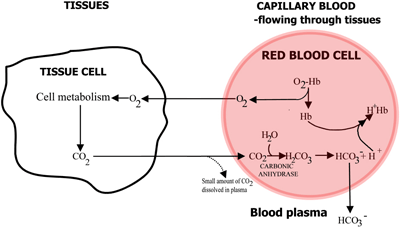
KUVIO 2a: KUDOKSET O2 diffundoituu verestä kudoksiin, CO2 diffundoituu kudoksista vereen
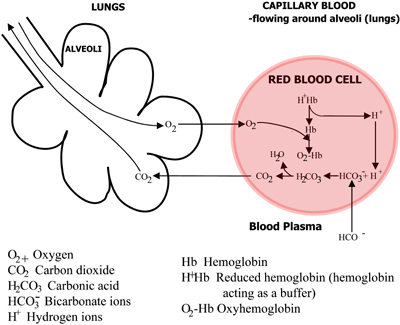
KUVIO 2b: Keuhkot CO2 diffundoituu verestä keuhkoihin, O2 diffundoituu keuhkoista vereen
Kudosten läpi virtaavassa kapillaariveressä happi irtoaa hemoglobiinista ja kulkeutuu kudossoluihin. Hiilidioksidi diffundoituu kudossoluista erytrosyytteihin, joissa punasolujen entsyymi hiilihappoanhydraasi mahdollistaa sen reaktion veden kanssa hiilihapoksi.
Hiilihappo dissosioituu bikarbonaatiksi (joka siirtyy veriplasmaan) ja vetyioneiksi, jotka yhdistyvät nyt hapettomaan hemoglobiiniin. Veri virtaa keuhkoihin, ja keuhkorakkuloiden kapillaareissa edellä mainitut reitit ovat päinvastaiset. Bikarbonaatti pääsee erytrosyytteihin, joissa se yhdistyy hemoglobiinista vapautuvien vetyionien kanssa hiilihapoksi.
Tämä dissosioituu hiilidioksidiksi ja vedeksi. Hiilidioksidi diffundoituu verestä keuhkojen alveoleihin ja poistuu uloshengitysilman mukana. Samaan aikaan happi diffundoituu keuhkorakkuloista kapillaariveriin ja yhdistyy hemoglobiiniin.
1.2. Happi diffundoituu keuhkorakkuloihin. HEMOGLOBIINI, JOTKA EIVÄT VOI SITOA HAPPIA
Normaalisti hemoglobiinia esiintyy vain pieniä määriä, mutta on olemassa kolme hemoglobiinilajia: methemoglobiini (MetHb tai Hi), sulfhemoglobiini (SHb) ja karboksihemoglobiini (COHb), jotka eivät pysty sitomaan happea.
Siten ne ovat toiminnallisesti puutteellisia, ja minkä tahansa näistä hemoglobiinilajeista lisääntyneet määrät, jotka ovat yleensä seurausta altistumisesta tietyille lääkkeille tai ympäristömyrkyille, voivat vakavasti heikentää hapen saantia.
Kattava selvitys hemoglobiinin rakenteesta ja toiminnasta on esitetty viitteessä.
ctHb, hemoglobiinin kokonaispitoisuus määritellään tavallisesti happeutuneen hemoglobiinin, hapenpoistohemboglobiinin, hiilihappohemoglobiinin ja methemoglobiinin summana.
CtHb:n MITTAUKSEN KLIININEN HYÖTY
CtHb:n mittauksen pääasiallinen syy on anemian toteaminen ja sen vaikeusasteen arviointi.
Anemia voidaan määritellä veren hapenkuljetuskyvyn vähenemisenä, joka johtuu erytrosyyttien määrän vähenemisestä ja/tai ctHb:n vähenemisestä, joten anemia todetaan, jos ctHb on alle viitealueen (normaalin) alarajan (TAULUKKO I). Mitä alhaisempi ctHb on, sitä vaikeampi anemia on.
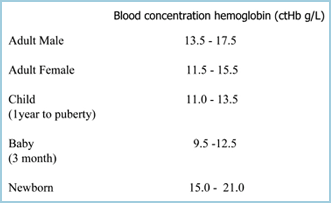
TAULUKKO I: ctHb:n viitealueet (Viitattu 2)
Anemia ei ole sairauskokonaisuus, vaan pikemminkin sairauden seuraus tai merkki. Syynä siihen, että ctHb on niin usein pyydetty verikoe, on se, että anemia on monien sairauksien piirre, joista monet ovat suhteellisen yleisiä (taulukko II).
Yleisiä oireita, joista useimmat ovat epäspesifisiä, ovat: kalpeus, väsymys ja letargia, hengenahdistus – erityisesti rasituksessa, huimaus ja pyörtyminen, päänsärky, ummetus ja kohonnut pulssi, sydämentykytys, takykardia.

TAULUKKO II: Eräitä anemiaan liittyviä kliinisiä tiloja
Tämä oireiden puuttuminen ei sulje pois anemiaa; monet lievästi aneemiset henkilöt jäävät oireettomiksi, varsinkin jos anemia on kehittynyt hitaasti.
2.2. POLYKYTEEMIA
Vaikka anemialle on ominaista alentunut ctHb, kohonnut ctHb viittaa polysytemiaan. Polysytemia syntyy vasteena mihin tahansa fysiologiseen tai patologiseen tilaan, jossa veri sisältää normaalia vähemmän happea (hypoksemia).
Kehon vasteena hypoksemiaan on lisääntynyt erytrosyyttituotanto hapen saannin lisäämiseksi, minkä seurauksena ctHb kohoaa. Tämä niin sanottu sekundaarinen polysytemia on osa fysiologista sopeutumista suuriin korkeuksiin, ja se voi olla kroonisen keuhkosairauden piirre.
Primäärinen polysytemia on paljon harvinaisempi luuytimen pahanlaatuinen sairaus nimeltä polycythemia vera, jolle on ominaista kaikkien verisolujen, myös erytrosyyttien, hallitsematon tuotanto. Sekundaarinen tai primaarinen polysytemia on yleensä paljon harvinaisempaa kuin anemia.
3.1. HISTORIALLINEN NÄKÖKULMA
Ensimmäisessä kliinisessä Hb:n mittauskokeessa, joka kehitettiin yli sata vuotta sitten, lisättiin pisaroita tislattua vettä mitattuun verimäärään, kunnes sen väri vastasi keinotekoisen väristandardin väriä.
Myöhemmässä muunnoksessa veri kyllästettiin ensin hiilikaasulla (hiilimonoksidilla) hemoglobiinin muuttamiseksi vakaammaksi karboksihemoglobiiniksi. Nykyaikainen hemoglobinometria on peräisin 1950-luvulta, jolloin kehitettiin spektrofotometria ja hemiglobiinisyanidimenetelmä (kyynamethemoglobiini).
Tämän ja muiden menetelmien mukauttaminen automaattisten hematologisten analysaattoreiden käyttöön seurasi. Kahden viime vuosikymmenen aikana kehitys on keskittynyt sellaisten menetelmien kehittämiseen, jotka mahdollistavat hemoglobiinin testaamisen hoitopaikassa (POCT).
Tässä jaksossa tarkastellaan ensin joitakin nykyisin laboratoriossa käytettäviä menetelmiä ja sitten laboratorion ulkopuolella käytettäviä POCT-menetelmiä.
3.2. HEMIGLOBINSKYANIDI – SPEKTROFOTOMETRINEN MENETELMÄ
Lähes 40 vuotta sen jälkeen, kun Kansainvälinen hematologian standardointikomitea (ICSH) hyväksyi sen ensimmäisen kerran hemoglobiinin mittausvertailumenetelmäksi, hemiglobinsyaniditesti (HiCN) on edelleen ICSH:n suosittelema menetelmä, jota vasten kaikkia uusia ctHb-menetelmiä arvioidaan ja standardoidaan.
Seuraava yksityiskohtainen tarkastelu kuvastaa sen jatkuvaa merkitystä sekä viite- että rutiinilaboratoriomenetelmänä.
3.2.1. Testin periaate
Veri laimennetaan liuokseen, joka sisältää kaliumferrisyanidia ja kaliumsyanidia. Kaliumferrisyanidi hapettaa hemin sisältämän raudan rautaiseen tilaan muodostaen methemoglobiinia, jonka kaliumsyanidi muuttaa hemiglobiinisyanidiksi (HiCN).
HiCN on stabiili värillinen tuote, jonka absorbanssimaksimi on liuoksessa 540 nm:ssä ja joka noudattaa tiukasti Beer-Lambertin lakia. Laimennetun näytteen absorbanssia 540 nm:ssä verrataan samalla aallonpituudella tapahtuvaan absorbanssiin HiCN-standardiliuoksessa, jonka ekvivalentti hemoglobiinipitoisuus tunnetaan.
Useimmat hemoglobiinijohdannaiset (oksihemoglobiini, methemoglobiini ja karboksihemoglobiini, mutta ei sulfhemoglobiini) muuntuvat HiCN:ksi ja siten mitataan tällä menetelmällä.
3.2.1.1. Reagenssilaimennin (modifioitu Drabkin-liuos)
| Kaliumferrisyanidi (K3Fe(CN)6) | 200 mg |
| Kaliumsyanidi (KCN) | 50 mg |
| Dihydrogeenikaliumfosfaatti (KH2 PO4) | 140 mg |
| Non-ioninen pesuaine (esim.esim. Triton X-100) | 1 ml |
| Edellä mainittu laimennetaan 1000 ml:ksi tislatulla vedellä |
3.2.1.2. Tislattu vesi. Manuaalinen menetelmä
25 µl verta lisätään 5,0 ml:aan reagenssia, sekoitetaan ja annetaan vaikuttaa 3 minuuttia. Absorbanssi luetaan 540 nm:ssä reagenssin nollaa vastaan. HiCN-standardin absorbanssi mitataan samalla tavalla.
3.2.1.3. ICSH:n HiCN-standardi
Tämän menetelmän suurimpana etuna on se, että käytössä on HiCN-standardiliuos, joka on valmistettu ja jolle on annettu pitoisuusarvo hyvin tarkkojen kriteerien mukaisesti, jotka kansainvälinen hematologian standardointineuvosto (ICSH) on määritellyt ja tarkistanut säännöllisesti.
Tämä kansainvälinen standardiliuos on ensisijainen kalibrointiaine kaupallisille standardiliuoksille, joita käytetään kliinisissä laboratorioissa kaikkialla maailmassa. Näin ollen kaikki HiCN-standardointia käyttävät käyttävät käytännössä samaa standardia, jonka arvo on tunnollisesti validoitu.
3.2.1.4. HiCN:n standardisointi. Häiriöt
Proteiinien, lipidien ja soluväliaineen aiheuttama häiriö on potentiaalinen ongelma kaikkien veren ainesosien, myös hemoglobiinin, spektrofotometrisessä arvioinnissa.
Näytteen suuri laimennus (1:251) poistaa ongelman suurelta osin, mutta virheellisesti kohonneita ctHb-tuloksia voi esiintyä potilailla, joiden plasman proteiinipitoisuus on erityisen korkea .
Kovasti lipeemiset näytteet ja näytteet, jotka sisältävät erittäin paljon valkosoluja (leukosyyttejä), voivat myös keinotekoisesti nostaa ctHb:tä vastaavalla mekanismilla .
3.2.1.5. HiCN:n edut
- Kansainvälinen standardi – tarkka
- Helppo sovittaa automatisoituihin hematologisiin analysaattoreihin; näin ollen toistettavissa (alhainen SD ja CV – erän sisäinen CV tyypillisesti
- Hyvin vakiintunut ja perusteellisesti tutkittu – ICSH:n suosittelema
- Hinnaltaan edullinen reagenssi
3.2.1.6. HiCN:n haitat
- Manuaalinen menetelmä edellyttää tarkkaa pipetointia ja spektrofotometriä
- Reagenssi (syanidi) on vaarallinen
- Edellä mainitut seikat rajoittavat sen käyttöä laboratorion ulkopuolella
- Häiritsevät kohonneet lipidit, plasman valkuaisaineet ja leukosyyttien lukumäärän nousuasteet
- Ei pysty erottamaan niitä hemoglobiinijohdannaisia, joilla ei ole hapensietokapasiteettia (MetHb, COHb, SHb). Saattaa siten yliarvioida veren hapenkuljetuskapasiteetin, jos näitä esiintyy epänormaaleja (enemmän kuin pieniä) määriä.
3.3. Vaihtoehtoiset (SYANIDIVAPAAT) LABORATORIOMENETELMÄT
Natriumlauryylisulfaatti (SLS) on pinta-aktiivinen aine, joka sekä lysoi erytrosyyttejä että muodostaa nopeasti kompleksin vapautuneen hemoglobiinin kanssa. Tuote SLS-MetHb on stabiili muutaman tunnin ajan, ja sillä on tyypillinen spektri, jonka suurin absorbanssi on 539 nm:ssä.
Kompleksi noudattaa Beer-Lambertin lakia, joten Hb-konsentraation ja SLS-MetHb:n absorbanssin välillä on tarkka lineaarinen korrelaatio.
Menetelmässä yksinkertaisesti sekoitetaan 25 µl verta 5,0 ml:aan 2,08 mmol/l:n SLS-liuosta (joka on puskuroitu pH:n 7,2:een) ja mitataan absorbanssi 539 nm:ssä. SLS-Hb-menetelmällä saadut ctHb-tulokset korreloivat erittäin hyvin (r = 0,998) HiCN-vertailumenetelmän kanssa.
Menetelmä on sovitettu automatisoituja hematologisia analysaattoreita varten, ja se on yhtä luotettava sekä tarkkuuden että täsmällisyyden suhteen kuin automatisoidut HiCN-menetelmät . Merkittävä etu on, että reagenssi on myrkytön. Se on myös vähemmän altis lipemian ja lisääntyneen leukosyyttikonsentraation aiheuttamille häiriöille .
SDS-MetHb:n pitkäaikainen epävakaus estää sen käytön standardina, joten menetelmä on kalibroitava verellä, jonka ctHb on määritetty HiCN-referenssimenetelmällä.
3.3.2 . Atsidimethemoglobiinimenetelmä
Tämä menetelmä perustuu hemoglobiinin muuntamiseen stabiiliksi värilliseksi tuotteeksi atsidimethemoglobiiniksi, jonka absorptiospektri on lähes identtinen HiCN:n kanssa.
Tässä menetelmässä käytetty reagenssi on hyvin samanlainen kuin HiCN-vertailumenetelmässä käytetty reagenssi, mutta myrkyllisempi kaliumsyanidi on korvattu natriumatsidilla. Kuten HiCN-menetelmässä, hemoglobiini muutetaan methemoglobiiniksi kaliumferrisyanidin avulla; atsidi muodostaa sitten kompleksin methemoglobiinin kanssa.
ctHb-tulokset tällä menetelmällä ovat vertailukelpoisia HiCN-viitemenetelmällä saatuihin tuloksiin; tämä on hyväksyttävä vaihtoehtoinen manuaalinen menetelmä. Natriumatsidin räjähdysalttius estää kuitenkin sen käytön automaattisissa hematologisissa analysaattoreissa. Azidi-MetHb-reaktio on sovitettu POCT-hemoglobinometreihin.
3.4. ctHb:n MITTAAMINEN LABORATORION ULKOPUOLELLA
Tässä tarkasteltavat POCT-menetelmät ovat:
- Kannettavat hemoglobinometrit
- CO-oksimetria – menetelmä, jota hyödynnetään POCT-verikaasuanalysaattoreissa
- WHO:n värisävyasteikko
3.4.1 . Kannettavat hemoglobinometrit
Kannettavat hemoglobinometrit, kuten HemoCue-B, mahdollistavat hemoglobiinin tarkan määrityksen vuodeosastolla. Ne ovat pohjimmiltaan fotometrejä, joilla voidaan mitata liuosten värin voimakkuutta.
Kertakäyttöinen mikrokyvetti, jossa nämä mittaukset tehdään, toimii myös reaktioastiana. Reagenssit, joita tarvitaan sekä Hb:n vapautumiseen erytrosyyteistä että Hb:n muuntamiseen stabiiliksi värilliseksi tuotteeksi, ovat kuivatussa muodossa kyvettien seinämillä.
Tarvitaan vain pieni näyte (tyypillisesti 10 µl) kapillaari-, laskimo- tai valtimoverta mikrokyvettiin ja mikrokyvetti asetetaan laitteeseen.
Laite on esikalibroitu tehtaalla käyttäen HiCN-standardia, ja testiliuoksen absorbanssi muunnetaan automaattisesti ctHb:ksi. Tulos näytetään alle minuutissa.
3.4.1.1. Testausmenetelmät Nykyaikaisten hemoglobinometrien etuja ovat
- Kannettavuus
- Akku- tai verkkokäyttöinen, voidaan käyttää missä tahansa
- Pieni näytemäärä (10 µl), joka saadaan sormenpistolla
- Nopea (tulos 60 sekunnissa)
- Käytön helppous – ei pipetointia
- Minimaalinen koulutustarve muulta kuin laboratoriohenkilökunnalta
- Vakiinnutettu HiCN:ää vasten – tulokset ovat vertailukelpoisia laboratoriossa saatuihin tuloksiin nähden
- Turbiditeettien korjaaminen. Tässä suhteessa kannettavat hemoglobinometrit ovat parempia kuin useimmat ctHb-menetelmät .
Tekniikkaa on arvioitu laajalti eri ympäristöissä, ja useimmat tutkimukset ovat vahvistaneet hyväksyttävän tarkkuuden ja täsmällisyyden laboratoriomenetelmiin verrattuna.
3.4.1.2 . Haitat
Joissain tutkimuksissa on kuitenkin esitetty huoli siitä, että muiden kuin laboratoriohenkilöstön käsissä tulokset voivat olla vähemmän tyydyttäviä. Käytön yksinkertaisuudesta huolimatta nämä laitteet eivät ole immuuneja käyttäjävirheille, ja tehokas koulutus on välttämätöntä.
On näyttöä siitä, että kapillaarinäytteistä (sormenpistonäytteistä) saadut tulokset ovat epätarkempia kuin hyvin sekoitetuista kapillaari- tai laskimonäytteistä saadut tulokset, jotka on kerätty EDTA-pulloihin .
3.4.2. Tulokset. CO-oksimetria
CO-oksimetri on erikoistunut spektrofotometri, jonka nimi kuvastaa alkuperäistä käyttötarkoitusta, joka oli COHb:n ja MetHb:n mittaaminen.
Monissa nykyaikaisissa verikaasuanalysaattoreissa on sisäänrakennettu CO-oksimetri, joka mahdollistaa ctHb:n samanaikaisen arvioinnin verikaasuanalyysin aikana.
CtHb:n mittaaminen CO-oksimetrialla perustuu siihen tosiasiaan, että hemoglobiini ja kaikki sen johdannaiset ovat värjättyjä valkuaisaineita, jotka absorboivat valoa tietyillä aallonpituuksilla ja joilla on näin ollen niille ominainen absorptiospektri (KUVA 3).
Beer-Lambertin lain mukaan yksittäisen yhdisteen absorbanssi on verrannollinen kyseisen yhdisteen pitoisuuteen. Jos liuoksen kunkin absorboivan aineen spektriominaisuus tunnetaan, liuoksen absorptiolukemia useilla aallonpituuksilla voidaan käyttää kunkin absorboivan aineen konsentraation laskemiseen.
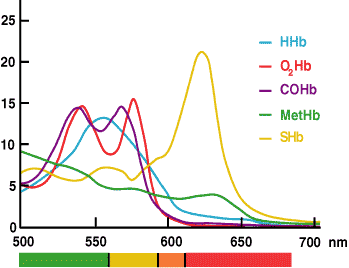
KAAVIO 3.
CO-oksimetrissä asennettu ohjelmisto käyttää hemolysoidun verinäytteen absorbanssimittauksia useilla aallonpituuksilla alueella, jolla hemoglobiinilajit absorboivat valoa (520-620 nm), kunkin hemoglobiinijohdannaisen (HHb, O2Hb, MetHb ja COHb) pitoisuuden laskemiseen. ctHb on näiden johdannaisten laskettu summa.
Käyttäjältä vaaditaan vain hyvin sekoitetun valtimoverinäytteen ruiskuttaminen verikaasuanalysaattoriin/CO-oksimetriin.
Näyte tai osa siitä pumpataan automaattisesti CO-oksimetrin mittauskyvettiin, jossa – joko kemiallisella tai fysikaalisella vaikutuksella – erytrosyytit lysoituvat vapauttaen hemoglobiinia, joka skannataan spektroskooppisesti edellä kuvatulla tavalla.
Tulokset näytetään yhdessä verikaasutulosten kanssa minuutissa tai kahdessa.
Monissa tutkimuksissa on vahvistettu, että CO-oksimetrialla saadut ctHb-tulokset eivät eroa kliinisesti merkittävästi vertailulaboratoriomenetelmillä saaduista tuloksista. CO-oksimetria tarjoaa hyväksyttävän keinon ctHb:n kiireelliseen arviointiin tehohoitoympäristössä.
3.4.2.1. CO-oksimetria ja CO-oksimetria. CO-oksimetrisen ctHb:n erityiset edut ovat
- Analyysin nopeus
- Analyysin helppous
- Pieni näytemäärä
- Ei pääoma- tai tarvikekustannuksia, jotka olisivat suuremmat kuin verikaasuanalyysiin vaadittavat kustannukset
- Lisäparametrit (MetHb, COHb, O2Hb) mitataan
- Valkosolujen suuri määrä ei vaikuta
3.4.3. WHO:n hemoglobiinin väriasteikko (HCS)
Tämä Maailman terveysjärjestöä (WHO) varten kehitetty matalan teknologian testi soveltuu vain rajoitetusti kehittyneissä maissa, mutta sillä on valtava merkitys kehitysmaiden taloudellisesti heikossa asemassa olevissa maissa, joissa anemia on yleisintä.
Alueilla, joilla ei ole laboratoriotiloja eikä riittäviä resursseja rahoittaa kehittyneempiä POCT-hemoglobinometrejä, se on käytännössä ainoa keino määrittää ctHb.
HCS-testi perustuu siihen yksinkertaiseen periaatteeseen, että veren väri on ctHb:n funktio. Veripisara imeytetään paperille ja sen väriä verrataan kuuden punaisen sävyn taulukkoon, jossa kukin sävy vastaa vastaavaa ctHb:tä: vaalein 40 g/l ja tummin 140 g/l. Veripisara imeytetään paperille ja sen väriä verrataan kuuteen punaisen sävyyn, joista kukin vastaa vastaavaa ctHb:tä. Vaikka menetelmä on periaatteessa hyvin yksinkertainen, sitä kehitettäessä on käytetty paljon tutkimusta ja tekniikkaa, jotta voidaan varmistaa mahdollisimman suuri tarkkuus ja täsmällisyys.
Esimerkiksi testiliuskojen matriisin paperin lopullinen valinta perustui laajoihin kokeiluihin eri papereilla, ja veren ja väriainesekoitusten spektrofotometristä analyysia käytettiin, jotta saatiin aikaan mahdollisimman tarkka vastaavuus taulukon värin ja veren värin välillä kullakin ctHb:n viitearvolla.
3.4.3.1. Veren ja väriainesekoitusten spektrofotometrinen analyysi. HCS-testin edut
- On helppokäyttöinen – vaatii vain 30 minuutin koulutuksen
- Ei vaadi laitteita tai sähköä
- On nopea – tulos 1 minuutissa
- Tarvitsee vain sormenpistonäytteen (kapillaarinäytteen)
- On erittäin halpa (noin 0,12 Yhdysvaltain dollaria testiä kohti)
3.4.3.2. Testaustulokset 3.4.3.1. Testauksen edut HCS-testin haitat
Luotettavat tulokset riippuvat testiohjeiden tarkasta noudattamisesta .
Yleisiä virheitä ovat:
- Eriittävästi tai liikaa verta testiliuskalla
- Tuloksen lukeminen liian myöhään (yli 2 minuuttia) tai liian aikaisin (alle 30 sekuntia)
- Tuloksen lukeminen huonoissa valaistusolosuhteissa
HSC-testillä on selvästikin luontaisia rajoituksia . Parhaimmillaan sillä voidaan määrittää, että potilasnäytteen ctHb on jollakin kuudesta pitoisuusalueesta: 30-50 g/l, 50-70 g/l, 70-90 g/l, 90-110 g/l, 110-130 g/l tai 130-150 g/l. Silti tämä riittää teoriassa tunnistamaan kaikki muut paitsi lievimmin aneemiset potilaat ja antamaan viitteitä anemian vaikeusasteesta.
Varhainen tutkimus osoitti testin kyvyn tunnistaa anemia (määritelty ctHb
YHTEENVETO
ctHb on toinen kahdesta parametrista, joita käytetään rutiininomaisesti verenkierron hapenottokyvyn arvioimiseen ja sitä kautta anemian ja polysytemian diagnoosin määrittämiseen.
Vaihtoehtoinen testi, jota kutsutaan hematokriitiksi (Hct) tai pakatuksi soluvolyymiksi (PCV), oli aiheena aiemmassa liitännäisartikkelissa, jossa käsiteltiin ctHb:n ja Hct:n välistä suhdetta . Tässä artikkelissa on keskitytty ctHb:n mittaamiseen.
Lukuisia menetelmiä on kehitetty, joista suurin osa perustuu hemoglobiinin tai sen johdannaisen värin mittaamiseen. Tässä lyhyessä katsauksessa on väistämättä jouduttu tekemään valintoja. Keskusteluun valitut menetelmät ovat nykyisin yleisimmin käytettyjä.
Valintaa tehtäessä on pyritty välittämään nykyisin käytössä olevien tekniikoiden kirjo ja se, miten niitä sovelletaan ctHb:n kliinisen kysynnän tyydyttämiseksi tilanteissa, jotka vaihtelevat kehitysmaiden köyhtyneistä alueista, joissa lääkehoito tuskin saa jalansijaa, nykyaikaisen tehohoitoyksikön huipputekniikan maailmaan.




