Perfect Scorer Test Prep : Chimie : Que signifie le mot » saturé » ?
En chimie, le mot saturé peut être utilisé pour décrire des molécules individuelles ou des mélanges soluté/solvant entiers, et il a une signification différente dans chacune de ces situations.
Généralement, quelque chose qui est saturé est complètement plein, comme dans une éponge saturée (une éponge remplie d’eau) ou un bombardement par saturation (utiliser des centaines de bombes pour détruire une zone entière).
Molécules saturées et insaturées
Lorsque le mot est appliqué à une molécule individuelle, cela signifie que la molécule n’a pas de doubles liaisons carbone-carbone ou de cycles. Dans les molécules ci-dessous, remarquez comment le fait de changer une simple liaison en une double liaison signifie que vous devez retirer deux atomes d’hydrogène :
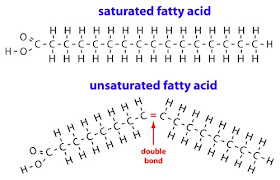
Parce que le carbone ne peut avoir que quatre liaisons, l’ajout d’une double liaison C=C utilise deux endroits où des hydrogènes auraient pu être liés à la place.
La première molécule a autant d’atomes d’hydrogène qu’elle peut en contenir (pas de double liaison), elle est donc saturée, ou pleine d’hydrogènes. Parce que la deuxième molécule a une double liaison, elle n’a pas tous les hydrogènes qu’elle pourrait potentiellement contenir, et elle est insaturée.
Important : Les acides gras sont considérés comme saturés si la partie de la chaîne hydrocarbonée de la molécule ne contient aucune double liaison. Le C=O du groupe COOH à l’extrémité gauche de la molécule n’est pas pris en compte.
Notez que la présence d’un cycle rendra également une molécule insaturée. Le pentane à chaîne droite et le pentane ramifié ont tous deux la formule C5H12, tandis que la molécule en forme d’anneau, le cyclopentane, a la formule C5H10:
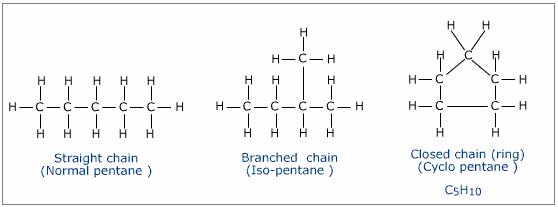
La formation de l’anneau implique de joindre les deux carbones aux extrémités de la chaîne, en utilisant deux endroits pour se lier là où les atomes d’hydrogène auraient été. Les hydrocarbures à chaîne droite et à chaîne ramifiée sont saturés, tandis que les hydrocarbures en forme d’anneau sont insaturés.
A propos, il n’existe pas de molécule sursaturée. Si vous voyez cette option sur un test, vous êtes face à une question piège.
Solutions saturées, insaturées et sursaturées
Le mot saturé a un sens différent lorsqu’il est utilisé pour décrire des solutions.
Pour les définitions ci-dessous, rappelez-vous que le solvant est le produit chimique dans lequel le soluté se dissout. Il y a toujours plus de solvant que de soluté.
Par exemple, l’eau salée est une solution de chlorure de sodium (le soluté) dans l’eau (le solvant).
Le solvant est généralement un liquide, mais il n’est pas obligé de l’être : l’air est une solution d’oxygène, de dioxyde de carbone et de vapeur d’eau (solutés) dans l’azote (le solvant). L’acier est une solution de carbone (le soluté) dans le fer (le solvant).

Les solutions saturées contiennent autant de soluté que le solvant peut en contenir.
La mer Morte est saturée : elle contient tout le sel et les minéraux qu’elle peut contenir. Elle contient tellement de sel que l’eau est plus dense que le corps humain, et les gens peuvent y flotter facilement. Dans l’image de droite, les morceaux solides blancs sont les morceaux de sel qui ne peuvent pas se dissoudre parce que l’eau est déjà saturée.
Les solutions non saturées contiennent moins de soluté que le solvant ne peut en contenir.
Contrairement à la mer Morte, l’eau normale de l’océan est non saturée. Même si elle est vraiment salée, elle ne contient pas autant de sel qu’elle peut en contenir.

Les solutions sursaturées contiennent plus de soluté que le solvant est censé pouvoir en contenir.
On peut faire du sucre candi en faisant bouillir de l’eau sucrée puis en la refroidissant, ce qui conduit à une sursaturation : le sucre est censé sortir de la solution, mais il ne le fera pas tant que vous n’y aurez pas déposé un cristal de semence. (L’absence de cristal de semence est également l’une des raisons pour lesquelles les arbres ne gèlent pas en hiver.)
La vidéo ci-dessous montre comment vous pouvez faire votre propre solution sursaturée d’acétate de sodium et l’utiliser pour faire des sculptures de « glace chaude »:
Vous devrez également connaître les termes ci-dessous:
Les solutions diluées contiennent très peu de soluté par rapport à la quantité de solvant.
Les solutions concentrées contiennent beaucoup de soluté par rapport à la quantité de solvant.
Questions pièges
Une question piège courante consiste à vous demander de faire les distinctions correctes entre les termes saturé, insaturé, sursaturé, dilué et concentré.
Une solution peut être à la fois saturée et diluée : lorsque la solubilité est faible, comme lorsque des cristaux d’iode sont ajoutés à l’eau d’un lac pour tuer les germes, la solution est à la fois saturée (pleine de soluté) et diluée (pas très concentrée). C’est une bonne chose que I2 soit non polaire et peu soluble dans l’eau : si la solution était concentrée, vous boiriez de grandes quantités d’un halogène élémentaire !
L’eau de mer, en revanche, est à la fois insaturée et concentrée.
La mer Morte est à la fois saturée et concentrée.




