Hemoglobine en de meting ervan
Normale celfunctie is afhankelijk van een voortdurende toevoer van zuurstof. Wanneer tijdens de celstofwisseling zuurstof wordt verbruikt, ontstaat kooldioxide.
Een van de belangrijkste functies van bloed is het afgeven van zuurstof (O2), aanwezig in geïnspireerde lucht, vanuit de longen aan elke cel in het lichaam en het afgeven van kooldioxide (CO2) vanuit de cellen aan de longen, voor eliminatie uit het lichaam in uitgeademde lucht.
Deze vitale gastransportfuncties zijn afhankelijk van het eiwit hemoglobine dat aanwezig is in erytrocyten (rode bloedcellen). Elk van de 5 × 1010 erytrocyten die normaal aanwezig zijn in 1 ml bloed bevat ongeveer 280 miljoen hemoglobinemoleculen.
1. HEMOGLOBINE STRUCTUUR EN FUNCTIE
De hemoglobinemolecule (Hb) is ruwweg bolvormig en bestaat uit twee paren van ongelijke subeenheden (FIGUUR 1).
Elk van de subeenheden is een gevouwen polypeptideketen (het globbinegedeelte) met een heemgroep (afgeleid van porfyrine) eraan vast.
In het centrum van elke heemgroep bevindt zich een enkel ijzeratoom in de ijzerhoudende (Fe2+) toestand. Zo is heem een metallo-porfyrine, dat overigens verantwoordelijk is voor de rode kleur van bloed.
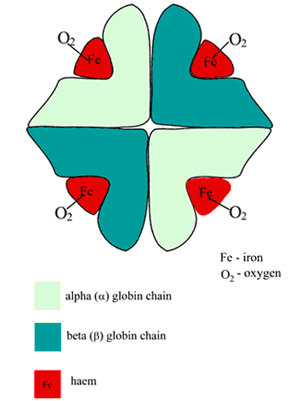
FIGUUR 1: Schema van de structuur van zuurstofhoudend hemoglobine (HbA)
De zuurstofbindingsplaats van Hb is de heemzak die aanwezig is in elk van de vier polypeptideketens; een enkel zuurstofatoom vormt een omkeerbare binding met het ijzerijzer op elk van deze plaatsen, zodat een molecule Hb vier zuurstofmoleculen bindt; het product is oxyhemoglobine (O2Hb).
De zuurstoftransportfunctie van Hb, dat wil zeggen zijn vermogen om zuurstof in de longen “op te nemen” en aan weefselcellen “af te geven”, wordt mogelijk gemaakt door minieme conformatieveranderingen in de quaternaire structuur die in het hemoglobinemolecuul optreden en die de affiniteit van de heemzak voor zuurstof veranderen. Hb heeft twee quaternaire structurele toestanden: de deoxy-toestand (lage zuurstofaffiniteit) en de oxy-toestand (hoge zuurstofaffiniteit).
Een reeks omgevingsfactoren bepaalt de quaternaire toestand van Hb en derhalve zijn relatieve zuurstofaffiniteit. De micro-omgeving in de longen begunstigt de oxy-quaternaire toestand, en dus heeft Hb hier een hoge affiniteit voor zuurstof.
De micro-omgeving van de weefsels daarentegen induceert de conformatieverandering in de Hb-structuur die zijn affiniteit voor zuurstof vermindert, zodat zuurstof aan de weefselcellen kan worden afgegeven.
1.1. HEMOGLOBINE EN CARBON DIOXIDE ELIMINATIE
Een kleine hoeveelheid (tot 20%) CO2 wordt van de weefsels naar de longen getransporteerd losjes gebonden aan het N-terminale aminozuur van de vier globine polypeptide eenheden van hemoglobine; het produkt van deze combinatie is carbaminohemoglobine. Het meeste CO2 wordt echter als bicarbonaat in het bloedplasma getransporteerd.
De omzetting van CO2 in bicarbonaat door de erytrocyten, noodzakelijk voor deze wijze van CO2-transport, resulteert in de produktie van waterstofionen (H+). Deze waterstofionen worden gebufferd door zuurstofarme hemoglobine.
De rol van hemoglobine bij het transport van zuurstof en kooldioxide is samengevat in FIGUREN 2a en 2b.
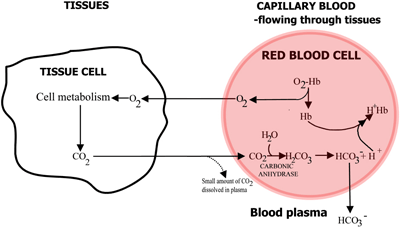
FIGUUR 2a: O2 diffundeert van bloed naar weefsels, CO2 diffundeert van weefsels naar bloed
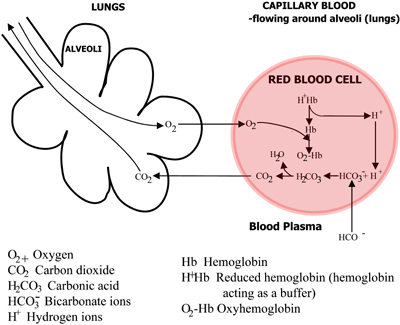
FIGUUR 2b: LUNGS CO2 diffundeert van bloed naar longen, O2 diffundeert van longen naar bloed
In capillair bloed dat door de weefsels stroomt, komt zuurstof vrij uit hemoglobine en gaat de weefselcellen binnen. Kooldioxide diffundeert uit de weefselcellen naar de erytrocyten, waar het rode-cellenenzym koolzuuranhydrase de reactie met water tot koolzuur mogelijk maakt.
Het koolzuur valt uiteen in bicarbonaat (dat in het bloedplasma terechtkomt) en waterstofionen, die zich verbinden met het nu zuurstofloze hemoglobine. Het bloed stroomt naar de longen, en in de haarvaten van de longblaasjes worden de bovengenoemde routes omgekeerd. Bicarbonaat komt in de erytrocyten en verbindt zich hier met waterstofionen, vrijgekomen uit hemoglobine, tot koolzuur.
Dit dissocieert tot kooldioxide en water. Het kooldioxide diffundeert uit het bloed in de longblaasjes en wordt afgevoerd in de uitgeademde lucht. Ondertussen diffundeert de zuurstof uit de longblaasjes naar de haarvaten en verbindt zich met hemoglobine.
1.2. HEMOGLOBINE DAT GEEN OXYGEN KAN BINDEN
Hoewel er normaal slechts sporen aanwezig zijn, zijn er drie soorten hemoglobine: methemoglobine (MetHb of Hi), sulfhemoglobine (SHb) en carboxyhemoglobine (COHb) die geen zuurstof kunnen binden.
Zij zijn dus functioneel deficiënt, en verhoogde hoeveelheden van een van deze hemoglobinesoorten, gewoonlijk het resultaat van blootstelling aan specifieke geneesmiddelen of milieutoxinen, kunnen de zuurstoftoevoer ernstig in gevaar brengen.
Een uitvoerige beschrijving van de structuur en functie van hemoglobine wordt gegeven in referentie .
ctHb, de totale hemoglobineconcentratie wordt typisch gedefinieerd als de som van zuurstofhoudend hemoglobine, zuurstofarme hemoglobine, carboxyhemoglobine en methemoglobine.
CLINISCHE GEVOLGEN VAN DE METING VAN ctHb
De voornaamste reden voor het meten van ctHb is het opsporen van anemie en het beoordelen van de ernst ervan.
Anemie kan worden gedefinieerd als een vermindering van het zuurstofdragend vermogen van bloed als gevolg van een vermindering van het aantal erytrocyten en/of een vermindering van het ctHb, zodat anemie is vastgesteld als het ctHb onder de ondergrens van het (normale) referentiebereik ligt (TABEL I). Hoe lager het ctHb, hoe ernstiger de anemie.
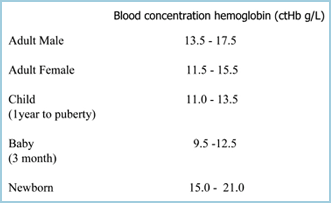
TABEL I: ctHb-referentiebereiken (Ref 2)
Anemie is geen ziekte-entiteit, maar eerder een gevolg of teken van ziekte. De reden waarom ctHb zo’n veel gevraagd bloedonderzoek is, is dat bloedarmoede een kenmerk is van een reeks ziektebeelden, waarvan vele relatief vaak voorkomen (tabel II).
Gemeenschappelijke symptomen, waarvan de meeste niet-specifiek zijn, zijn: bleekheid, vermoeidheid en lethargie, kortademigheid – vooral bij inspanning, duizeligheid en flauwvallen, hoofdpijn, constipatie en verhoogde polsslag, hartkloppingen, tachycardie.

TABEL II: Enkele klinische aandoeningen die met anemie in verband worden gebracht
Het ontbreken van deze symptomen sluit anemie niet uit; veel personen met lichte anemie blijven asymptomatisch, vooral als de anemie zich langzaam heeft ontwikkeld.
2.2. POLYCYTHEMIE
Terwijl anemie wordt gekenmerkt door een verlaagd ctHb, wijst een verhoogd ctHb op polycythemie. Polycythemie ontstaat als reactie op elke fysiologische of pathologische toestand waarbij het bloed minder zuurstof bevat dan normaal (hypoxemie).
De reactie van het lichaam op hypoxemie omvat een verhoogde productie van erytrocyten om de zuurstoftoevoer te verhogen, en als gevolg daarvan wordt het ctHb verhoogd. Deze zogenaamde secundaire polycythemie maakt deel uit van de fysiologische aanpassing aan grote hoogte en kan een kenmerk zijn van chronische longaandoeningen.
Primaire polycythemie is een veel minder vaak voorkomende maligniteit van het beenmerg, polycythemia vera genaamd, die wordt gekenmerkt door ongecontroleerde productie van alle bloedcellen, inclusief erytrocyten. Polycythemie, secundair of primair, komt in het algemeen veel minder vaak voor dan anemie.
3.1. HISTORISCHE VOORUITZICHTEN
De eerste klinische test van Hb-meting die meer dan een eeuw geleden werd bedacht, bestond uit het toevoegen van druppels gedestilleerd water aan een gemeten volume bloed totdat de kleur overeenkwam met die van een kunstmatig gekleurde standaard.
Bij een latere wijziging werd het bloed eerst verzadigd met kolengas (koolmonoxide) om hemoglobine om te zetten in het stabielere carboxyhemoglobine. Moderne hemoglobinometrie dateert uit de jaren 1950, na de ontwikkeling van spectrofotometrie en de hemiglobincyanide (cynamethemoglobine) methode.
Aanpassing van deze methode en andere voor gebruik in geautomatiseerde hematologie-analysatoren volgde. In de afgelopen twee decennia heeft de vooruitgang zich geconcentreerd op de ontwikkeling van methoden die point-of-care testen (POCT) van hemoglobine mogelijk maken.
In dit deel wordt eerst aandacht besteed aan enkele van de methoden die momenteel in het laboratorium worden gebruikt en vervolgens aan de POCT-methoden die buiten het laboratorium worden gebruikt.
3.2. HEMIGLOBINCYANIDE – EEN SPECTROPHOTOMETRISCHE METHODE
Nauwelijks 40 jaar nadat de hemiglobine-test (HiCN) voor het eerst door het International Committee for Standardization in Hematology (ICSH) als referentiemethode voor het meten van hemoglobine werd aangenomen, blijft deze test de door het ICSH aanbevolen methode, waaraan alle nieuwe ctHb-methoden worden getoetst en gestandaardiseerd.
De gedetailleerde beschouwing die volgt weerspiegelt zijn blijvend belang zowel als referentie als routine laboratoriummethode.
3.2.1. Principe van de test
Bloed wordt verdund in een oplossing die kaliumferricyanide en kaliumcyanide bevat. Kaliumferricyanide oxideert het ijzer in heem tot de ferrische toestand om methemoglobine te vormen, dat door kaliumcyanide wordt omgezet in hemiglobinecyanide (HiCN).
HiCN is een stabiel gekleurd product, dat in oplossing een absorptiemaximum heeft bij 540 nm en strikt gehoorzaamt aan de wet van Beer-Lambert. De extinctie van het verdunde monster bij 540 nm wordt vergeleken met de extinctie bij dezelfde golflengte van een standaard-HiCN-oplossing waarvan de equivalente hemoglobineconcentratie bekend is.
De meeste hemoglobine-derivaten (oxyhemoglobine, methemoglobine en carboxyhemoglobine, maar niet sulfhemoglobine) worden omgezet in HiCN en dus met deze methode gemeten.
3.2.1.1. Reagensverdunningsmiddel (gemodificeerde Drabkin-oplossing)
| Kaliumferricyanide (K3Fe(CN)6) | 200 mg |
| Kaliumcyanide (KCN) | 50 mg |
| Dihydrogeen kaliumfosfaat (KH2 PO4) | 140 mg |
| Niet-ionisch detergens (bijv.b.v. Triton X-100) | 1 mL |
| Hierboven verdund tot 1000 mL in gedestilleerd water |
3.2.1.2. Handmatige methode
25 µl bloed wordt toegevoegd aan 5,0 mL reagens, gemengd en 3 minuten laten staan. De absorptie wordt afgelezen bij 540 nm tegen een reagensblanco. De extinctie van de HiCN-standaard wordt op dezelfde wijze gemeten.
3.2.1.3. ICSH HiCN-standaard
Het grote voordeel van deze methode is dat er een standaard HiCN-oplossing is die wordt vervaardigd en waaraan een concentratiewaarde wordt toegekend volgens zeer nauwkeurige criteria die periodiek door de International Council for Standardization in Hematology (ICSH) worden vastgesteld en herzien.
Deze internationale standaardoplossing is de primaire ijkstof voor de commerciële standaardoplossingen die in klinische laboratoria over de hele wereld worden gebruikt. Al degenen die HiCN-standaardisatie gebruiken, gebruiken dus in feite dezelfde standaard, waarvan de waarde nauwgezet is gevalideerd.
3.2.1.4. Storing
Storing door proteïnen, lipiden en cellulaire materie is een potentieel probleem bij spectrofotometrische schattingen van elk bloedbestanddeel, met inbegrip van hemoglobine.
De grote verdunning (1:251) van het monster elimineert het probleem grotendeels, maar foutief verhoogde ctHb-resultaten kunnen voorkomen bij patiënten met een bijzonder hoge plasma-eiwitconcentratie.
Zwaar lipemische monsters en monsters die zeer veel witte bloedcellen (leukocyten) bevatten, kunnen het ctHb ook artefactief verhogen door een soortgelijk mechanisme
3.2.1.5. Voordelen van HiCN
- Internationale standaard – nauwkeurig
- Gemakkelijk aan te passen aan geautomatiseerde hematologieanalysatoren; dus reproduceerbaar (lage SD en CV – binnen batch CV typisch
- Goed ingeburgerd en grondig onderzocht – ICSH aanbevolen
- Ingoedkoop reagens
3.2.1.6. Nadelen van HiCN
- Handmatige methode vereist nauwkeurig pipetteren en spectrofotometer
- Reagens (cyanide) gevaarlijk
- Het bovenstaande beperkt het gebruik buiten het laboratorium
- Ongevoelig voor interferentie door verhoogde lipiden, plasma-eiwitten en leukocytenaantallen
- Maakt geen onderscheid tussen de hemoglobinederivaten die geen zuurstofdragend vermogen hebben (MetHb, COHb, SHb). Kan dus het zuurstofdragend vermogen van bloed overschatten indien deze in abnormale (meer dan sporen) hoeveelheden aanwezig zijn.
3.3. ALTERNATIEVE (CYANIDE-VRIJE) LABORATORIUMMETHODEN
Natrium Lauryl Sulfaat (SLS) is een oppervlakte-actieve stof die zowel erytrocyten afbreekt als snel een complex vormt met de vrijgekomen hemoglobine. Het produkt SLS-MetHb is enkele uren stabiel en heeft een karakteristiek spectrum met een maximale absorptie bij 539 nm .
Het complex gehoorzaamt aan de wet van Beer-Lambert, zodat er een nauwkeurige lineaire correlatie is tussen de Hb-concentratie en de absorptie van SLS-MetHb.
De methode bestaat eenvoudig uit het mengen van 25 µL bloed met 5,0 mL van een 2,08-mmol/L-oplossing van SLS (gebufferd tot pH van 7,2), en het aflezen van de absorptie bij 539 nm. De resultaten van ctHb met de SLS-Hb-methode blijken zeer nauw te correleren (r = 0,998) met de referentie-HiCN-methode.
De methode is aangepast voor geautomatiseerde hematologie-analysatoren en is even betrouwbaar in termen van zowel nauwkeurigheid als precisie als geautomatiseerde HiCN-methoden . Een groot voordeel is dat het reagens niet-toxisch is. Het is ook minder gevoelig voor interferentie door lipemie en verhoogde concentratie van leukocyten .
De instabiliteit op lange termijn van SDS-MetHb sluit het gebruik ervan als standaard uit, zodat de methode moet worden gekalibreerd met bloed waarvan het ctHb is bepaald met de referentie-HiCN-methode.
3.3.2. Azide-methemoglobine-methode
Deze methode is gebaseerd op de omzetting van hemoglobine in een stabiel gekleurd produkt azide-methemoglobine, dat een vrijwel identiek absorptiespectrum heeft als HiCN.
Het reagens dat bij deze methode wordt gebruikt lijkt sterk op dat van de HiCN-referentiemethode, met vervanging van natriumazide door het giftigere kaliumcyanide. Evenals bij de HiCN-methode wordt hemoglobine door kaliumferricyanide omgezet in methemoglobine; azide vormt dan een complex met methemoglobine.
De resultaten vanctHb met deze methode zijn vergelijkbaar met de resultaten die met de HiCN-referentiemethode worden verkregen; dit is een aanvaardbare alternatieve handmatige methode. Het explosieve potentieel van natriumazide verhindert echter het gebruik ervan op geautomatiseerde hematologieanalysatoren. De azide-MetHb reactie is aangepast voor POCT hemoglobinometers.
3.4. METING VAN ctHb BUITEN HET LABORATORIUM
De hier beschouwde POCT methoden zijn:
- Draagbare hemoglobinometers
- CO-oximetrie – een methode die gebruikt wordt in POCT bloedgasanalysatoren
- WHO kleurenschaal
3.4.1. Draagbare hemoglobinometers
Draagbare hemoglobinometers zoals de HemoCue-B maken een nauwkeurige bepaling van hemoglobine aan het bed mogelijk. Het zijn in wezen fotometers waarmee de kleurintensiteit van oplossingen kan worden gemeten.
De wegwerp-microcuvette waarin deze metingen worden verricht, fungeert tevens als reactievat. De reagentia die nodig zijn voor zowel het vrijkomen van Hb uit erytrocyten als de omzetting van Hb in een stabiel gekleurd product zijn in gedroogde vorm aanwezig op de wanden van de cuvette.
Het enige dat nodig is, is het inbrengen van een klein monster (gewoonlijk 10 µL) capillair, veneus of arterieel bloed in de microcuvette en het inbrengen van de microcuvette in het instrument.
Het instrument is in de fabriek voorgekalibreerd met HiCN-standaard, en de extinctie van de testoplossing wordt automatisch omgezet in ctHb. Het resultaat wordt in minder dan een minuut weergegeven.
3.4.1.1. Voordelen van moderne hemoglobinometers zijn
- Draagbaarheid
- Batterij of netvoeding, kan overal worden gebruikt
- Klein monstervolume (10 µL) verkregen door vingerprik
- Snel (resultaat in 60 seconden)
- Gemakelijk in gebruik – geen pipetteren
- Minimale opleiding vereist voor niet-laboratoriumpersoneel
- Gestandaardiseerd ten opzichte van HiCN – resultaten vergelijkbaar met die verkregen in laboratorium
- Correctie voor troebelheid. In dit opzicht zijn draagbare hemoglobinometers superieur aan de meeste ctHb-methoden.
Deze technologie is uitvoerig geëvalueerd in een reeks settings en de meeste studies hebben een aanvaardbare nauwkeurigheid en precisie bevestigd in vergelijking met laboratoriummethoden.
3.4.1.2. Nadelen
Enkele studies hebben echter de vrees geuit dat de resultaten in handen van niet-laboratoriumpersoneel minder bevredigend kunnen zijn. Ondanks de eenvoud van de bediening zijn deze instrumenten niet ongevoelig voor fouten van de bediener, en een doeltreffende opleiding is van essentieel belang.
Er zijn aanwijzingen dat de resultaten van capillaire (vingerprik-) monsters minder nauwkeurig zijn dan die van goed gemengde capillaire of veneuze monsters die in EDTA-flesjes zijn verzameld
3.4.2. CO-oximetrie
Een CO-oximeter is een gespecialiseerde spectrofotometer, waarvan de naam de oorspronkelijke toepassing weergeeft, namelijk het meten van COHb en MetHb.
Veel moderne bloedgasanalysatoren hebben een ingebouwde CO-oximeter, die de gelijktijdige schatting van ctHb tijdens de bloedgasanalyse mogelijk maakt.
De meting van ctHb door CO-oximetrie is gebaseerd op het feit dat hemoglobine en al zijn derivaten gekleurde eiwitten zijn die licht absorberen bij specifieke golflengten en daardoor een karakteristiek absorptiespectrum hebben (FIGUUR 3).
De wet van Beer-Lambert dicteert dat de absorptie van een enkele verbinding evenredig is met de concentratie van die verbinding. Als de spectrale karakteristiek van elke absorberende stof in een oplossing bekend is, kunnen absorptiewaarden van de oplossing bij meerdere golflengten worden gebruikt om de concentratie van elke absorberende stof te berekenen.
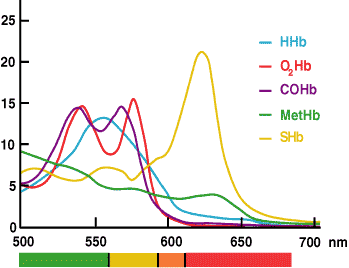
FIGUUR 3.
In de CO-oximeter worden extinctiemetingen van een hemolysebloedmonster bij meerdere golflengten in het bereik waarin hemoglobinesoorten licht absorberen (520-620 nm), door de geïnstalleerde software gebruikt om de concentratie van elk van de hemoglobinederivaten (HHb, O2Hb, MetHb en COHb) te berekenen. ctHb is de berekende som van deze derivaten.
Het enige dat van de bediener wordt verlangd is injectie van een goed gemengd arterieel bloedmonster in de bloedgasanalysator/CO-oximeter.
Het monster, of een gedeelte daarvan, wordt automatisch naar de meetcuvet van de CO-oximeter gepompt, waar – door chemische of fysische werking – de erytrocyten worden gelyseerd om hemoglobine vrij te maken, dat spectroscopisch wordt gescand zoals hierboven beschreven.
Resultaten worden samen met bloedgasresultaten binnen een minuut of twee weergegeven.
Verschillende studies hebben bevestigd dat ctHb-resultaten verkregen met CO-oximetrie klinisch niet significant verschillen van die verkregen met referentielaboratoriummethoden. CO-oximetrie biedt een aanvaardbaar middel voor dringende schatting van ctHb in een kritieke zorgsetting.
3.4.2.1. De bijzondere voordelen van ctHb door middel van CO-oximetrie zijn
- Snelheid van de analyse
- Gemak van de analyse
- Klein monstervolume
- Geen hogere kapitaal- of verbruikskosten dan die voor bloedgasanalyse
- Extra parameters (MetHb, COHb, O2Hb) gemeten
- Niet beïnvloed door hoog aantal witte bloedcellen
3.4.3. WHO hemoglobin color scale (HCS)
Ontwikkeld voor de Wereldgezondheidsorganisatie (WHO), heeft deze laagtechnologische test een beperkte toepassing in ontwikkelde landen, maar is van enorm belang voor de economisch achtergestelde landen van de ontwikkelingswereld, waar anemie het meest voorkomt.
In gebieden waar geen laboratoriumfaciliteiten zijn en onvoldoende middelen om meer geavanceerde POCT hemoglobinometers te financieren, is het vrijwel de enige manier om ctHb te bepalen.
De HCS-test is gebaseerd op het eenvoudige principe dat de kleur van bloed een functie is van ctHb. Een druppel bloed wordt op papier geabsorbeerd en de kleur wordt vergeleken met een grafiek van zes tinten rood, waarbij elke kleur overeenkomt met een equivalent ctHb: de lichtste 40 g/L en de donkerste 140 g/L. Hoewel in principe zeer eenvoudig, werd bij de ontwikkeling veel onderzoek en technologie gebruikt om een zo groot mogelijke nauwkeurigheid en precisie te waarborgen.
Bij voorbeeld: uitgebreide proeven met verschillende papiersoorten hebben geleid tot de uiteindelijke keuze van het papier voor de matrix van de teststrook, en spectrofotometrische analyse van bloed en kleurstofmengsels werden toegepast om de kleur van de teststrook zo goed mogelijk te doen overeenstemmen met de kleur van het bloed bij elk referentiectHb.
3.4.3.1. Voordelen van de HCS-test
- Is gemakkelijk te gebruiken – vereist slechts 30 minuten opleiding
- Vraagt geen apparatuur of vermogen
- Is snel – resultaat binnen 1 minuut
- Vraagt slechts een vingerprik (capillair) monster
- Is zeer goedkoop (ongeveer 0,12 USD per test)
3.4.3.2. Nadelen van de HCS-test
Betrouwbare resultaten hangen af van een strikte naleving van de testinstructies .
Gemeenschappelijke fouten zijn:
- Onvoldoende of te veel bloed op de teststrip
- Het resultaat te laat (meer dan 2 minuten) of te vroeg (minder dan 30 seconden)
- Het resultaat aflezen bij slechte lichtomstandigheden
De HCS-test heeft duidelijk inherente beperkingen. Op zijn best kan hij bepalen dat het ctHb van een patiëntenmonster binnen een van zes concentratiebereiken ligt: 30-50 g/L, 50-70 g/L, 70-90 g/L, 90-110 g/L, 110-130 g/L of 130-150 g/L. Nog steeds is dit theoretisch voldoende om alle, behalve de meest mild anemische patiënten te identificeren en een indicatie van de ernst te geven.
Een vroege studie toonde het vermogen van de test aan om anemie te identificeren (gedefinieerd als ctHb
SUMMARY
ctHb is een van de twee parameters die routinematig worden gebruikt om het zuurstofdragend vermogen van bloed te beoordelen en daardoor een diagnose van anemie en polycythemie vast te stellen.
De alternatieve test, hematocriet (Hct) of Packed Cell Volume (PCV) genoemd, was het onderwerp van een eerder begeleidend artikel, waarin de relatie tussen ctHb en Hct werd besproken. De focus van dit artikel is de meting van ctHb.
Er zijn talrijke methoden ontwikkeld, waarvan de meeste gebaseerd zijn op het meten van de kleur van hemoglobine of een derivaat van hemoglobine. Voor dit korte overzicht was het onvermijdelijk selectief te werk te gaan. De voor bespreking gekozen methoden behoren tot de tegenwoordig meest gebruikte.
Bij het maken van de selectie is getracht een beeld te geven van het scala aan technologieën dat momenteel wordt gebruikt en hoe deze worden toegepast om te voldoen aan de klinische vraag naar ctHb in settings die variëren van verarmde gebieden in de derde wereld, waar medische zorg nauwelijks voet aan de grond heeft, tot de high-tech wereld van de moderne intensive care unit.




