KÉM 245 – Enzimgátlás
Biokémiai témakörök
Enzimgátlás
Az inhibitorok és a gátlás típusai.Reversibilis és irreverzibilis inhibitorok és gátlás. A kompetitív és nem kompetitív gátlás modelljei és kinetikai hatásai. Vegyes gátlás.Példák az enzimgátlásra.
Az enzimek specifitása nem korlátozódik szigorúan a szubsztrátokra. Gyakran előfordul, hogy egy enzim aktivitását az inhibitoroknak nevezett molekulákkal való specifikus kölcsönhatások csökkentik. Az enzimgátlás a biokémia egyik legfontosabb jelensége. Például számos gyógyszer, antibiotikum és toxin úgy fejti ki hatását, hogy képes gátolni egy enzimet. A szubsztráthoz szerkezetileg hasonló inhibitorok gyakran kompetitív inhibitorok, mivel versenyeznek az aktív helyhez való kötődésért. Az enzimgátlás lehet reverzibilis (mint általában, amikor az inhibitor nemkovalens kölcsönhatásokon keresztül kötődik az enzimhez) vagy irreverzibilis (mint számos olyan esetben, amikor az inhibitorok az enzim kovalens módosításán keresztül hatnak, esetleg a katalízis szempontjából kritikus maradékot célozva).
A reverzibilis gátlásra több egyszerű modellt is elképzelhetünk. Ezek közül a legegyszerűbb az aktív centrum közvetlen elzárása az inhibitor által. Ez egy olyan molekula esetében lenne látható, amely bizonyos szerkezeti hasonlóságot mutat a szubsztráttal. A kompetitív gátlás e modelljében a szubsztrát és az inhibitor kötődése kölcsönösen kizárja egymást.
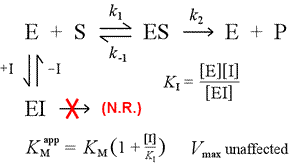
Jobbra látható a kompetitív gátlás egyszerű mechanisztikus modellje. Az inhibitor, I, csak a szabad enzimhez E kötődik, KI disszociációs állandóval, és blokkolja a szubsztrát (S) kötődését. Azáltal, hogy az enzim egy részét leköti az inaktív EI-komplexben, adott szubsztrátkoncentráció mellett kevesebb enzim áll rendelkezésre ahhoz, hogy a szubsztráttal egyesülve ES-t képezzen, majd potenciálisan termékké alakuljon. Az ½Vmax eléréséhez szükséges mennyiség növekedése figyelhető meg, ezért a KM látszólagos értéke nő.
Az egyre nagyobb szintre való emelkedéssel a szubsztrát elnyomhatja az inhibitort, túlkompetálva azt a szabad enzimmel olyan mértékben, hogy a valódi Vmax még megközelíthető legyen.
Egyszerűen elképzelhető, hogy egy olyan molekula, amely bizonyos kulcsfontosságú szerkezeti jellemzőiben hasonlít a szubsztrátra, versenyezhet a szubsztráttal az aktív centrumban való kötődésért. Ezt nevezzük szubsztrátanalógnak, és ezek szolgáltatnak gyakori példákat az enzimek kompetitív inhibitoraira. Ha az enzimek a reakció sebességét a reakció átmeneti állapotának szelektív stabilizálásával fokozzák, akkor ha találunk egy olyan molekulát, amely hasonlít az átmeneti állapotra (szerkezetében és polaritásában vagy töltésében), akkor egy ilyen átmeneti állapot analógnak nagyon jó kompetitív inhibitornak kell lennie.
A kompetitív gátlás modelljét szembeállítjuk a nem kompetitív gátlással, amelyben az inhibitor csak az enzim-szubsztrát komplexhez kötődik. Ezt egy indukált-illeszkedés típusú enzim-szubsztrát kölcsönhatás eredményeként képzelhetjük el, amelyben az inhibitor számára kizárólag az ES indukált konformációjában áll rendelkezésre kötőhely.
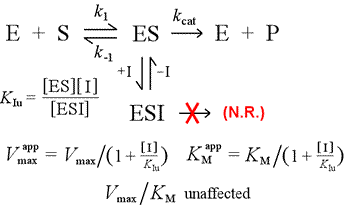
Balra: A nem kompetitív gátlás mechanisztikus modellje. Ebben a modellben az inhibitor csak az ES-komplexhez kötődik, a szabad enzimhez nem. A terner komplex, az ESI, nem megy át termékekké. Ennek hatására csökken a látszólagos Vmax. Az ESI inhibitor disszociációs állandóját KIu-val jelöljük. A Le Châtelier-elvvel magyarázott hatás szerint a látszólagos KM alacsonyabb, mivel az inhibitor megkötése eltávolítja az ES képződési “egyensúly” termékének (ES) egy részét.
A gátlás olyan modellje, amelyben az inhibitor a szabad enzimet és az enzim-szubsztrát komplexet is megköti, a kevert gátlás. Az inhibitor disszociációs állandója E és ES között eltérhet (azaz KI ≠ KIu). Azt a speciális esetet, amikor KI = KIu, nemkompetitív gátlásnak nevezzük. Megjegyzendő, hogy ebben az esetben a KM nem változik, míg a Vmax csökken.
A reverzibilis enzimgátlás típusai – összefoglaló
Láttuk, hogy a reverzibilis gátlás különböző modelljeit a kinetikai paraméterekre gyakorolt hatások alapján különböztethetjük meg. Az alábbi táblázat összefoglalja a gátlás típusait és azok hatásait ezekre a paraméterekre.

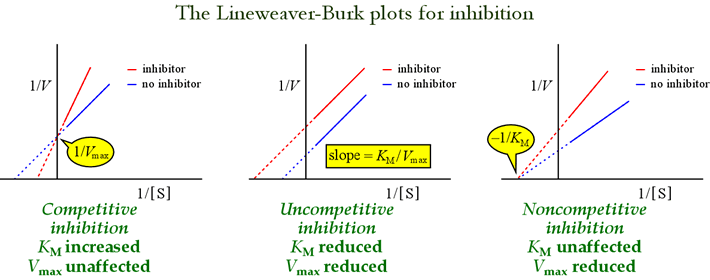
A Lineweaver-Burk, vagy kettős-reciprokális ábrák hasznosak a gátlási minták azonosítására. Az alábbi ábra mutatjahogy a gátlás különböző típusai hogyan hatnak a plotra.
Példák az enzimgátlásra
Az első és legszélesebb körben használt gyógyszer, az acetilszalicilát (szalicilát = ortohidroxibenzoát), közismert nevén az aszpirin, hatékony fájdalomcsillapító (fájdalomcsillapító), lázcsillapító (lázcsillapító) és gyulladáscsökkentő szer. A fűzfakéreg gyógyhatását egyes kultúrákban már évszázadok óta ismerték. A 19. században megállapították, hogy a hatóanyag a és a szalicilalkohol kombinációja. Ezekre és más megfigyelésekre, valamint a kémiai szintézis terén elért eredményekre alapozva az aszpirin a század közepén vált elérhetővé, amelyet Hoffman, a Bayer alkalmazásában álló vegyész állított elő. A modernebb vizsgálatok megállapították, hogy az aszpirin gyógyhatása nagyrészt abból a képességéből ered, hogy irreverzibilisen gátolja a ciklooxigenáz nevű enzimet, amely a prosztaglandinokés tromboxánok szintéziséhez szükséges.
A ciklooxigenázok katalizálják az arachidonátnak a prosztaglandinok és tromboxánok előanyagává, prosztaglandin G2-vé (PGG2, szerkezet és reakció) történő átalakításának első lépését. A reakció két O2-molekulát használ fel, és a C20:4 zsírsavat egy ciklopentángyűrűt tartalmazó peroxidált molekulává alakítja át (PGG2 – a PG a “prosztaglandin” rövidítése). A ciklooxigenáz enzim hidroperoxidáz aktivitással is rendelkezik, amely a PGG2-t PGH2-vé alakítja. Így a “ciklooxigenáz” (COX) pontosabb lenne a prosztaglandin endoperoxid H szintáz (PGHS) elnevezés. A ciklooxigenáz aktivitásának aszpirin általi gátlása annak köszönhető, hogy képes kémiailag módosítani az enzim egy szerin-maradékát (Ser530). A szerin-maradék acetilcsoportot kap az aszpirintől, ami irreverzibilis módosítás. Így az aszpirin egy irreverzibilis inhibitor példája. Valójában két COX izoenzim létezik: egy konstitutív forma, a COX-1 (PGHS-1), és egy indukált forma (gyulladásos körülmények között), a COX-2 (PGHS-2). A nem-szteroid gyulladáscsökkentők (NSAID-ok), mint az aszpirin, az ibuprofén és a naproxen általában mindkét izoformát gátolják. Következésképpen ezek a gyógyszerek nemkívánatos mellékhatásokat, pl. gyomor-bélrendszeri irritációt okoznak. Ezért a farmakológiai kutatások jelenlegi célja a COX-2 specifikus gátlók kifejlesztése, amelyről úgy gondolják, hogy az NSAID-ok fájdalomcsillapító és gyulladáscsökkentő hatásainak nagy részét közvetíti.
Kapcsolódó témájú oldalak:
- bevezető kémiai kinetika
- bevezető enzimológia
- enzimkinetika
- Michaelis-Menten-egyenlet




