L’emoglobina e la sua misurazione
La funzione cellulare normale dipende da un apporto continuo di ossigeno. Quando l’ossigeno viene consumato durante il metabolismo cellulare, viene prodotta anidride carbonica.
Una funzione principale del sangue è la consegna dell’ossigeno (O2), presente nell’aria ispirata, dai polmoni ad ogni cellula del corpo e la consegna dell’anidride carbonica (CO2) dalle cellule ai polmoni, per l’eliminazione dal corpo nell’aria espirata.
Queste funzioni vitali di trasporto dei gas dipendono dalla proteina emoglobina contenuta negli eritrociti (globuli rossi). Ognuno dei 5 × 1010 eritrociti normalmente presenti in 1 mL di sangue contiene circa 280 milioni di molecole di emoglobina.
1. STRUTTURA E FUNZIONE DELL’EMOGLOBINA
La molecola di emoglobina (Hb) è approssimativamente sferica e comprende due coppie di subunità dissimili (FIGURA 1).
Ognuna delle subunità è una catena polipeptidica ripiegata (la porzione di globina) con un gruppo eme (derivato dalla porfirina) attaccato.
Al centro di ogni gruppo eme c’è un singolo atomo di ferro nello stato ferroso (Fe2+). Così l’eme è una metallo-porfirina, incidentalmente responsabile del colore rosso del sangue.
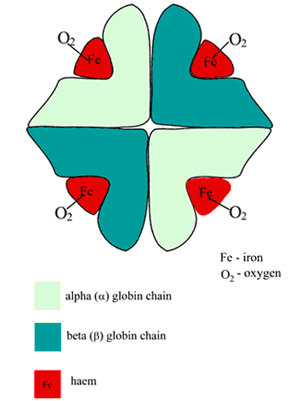
FIGURA 1: Schema della struttura dell’emoglobina ossigenata (HbA)
Il sito di legame all’ossigeno dell’Hb è la tasca eme presente in ciascuna delle quattro catene polipeptidiche; un singolo atomo di ossigeno forma un legame reversibile con il ferro ferro in ciascuno di questi siti, così una molecola di Hb lega quattro molecole di ossigeno; il prodotto è l’ossiemoglobina (O2Hb).
La funzione di consegna dell’ossigeno dell’Hb, cioè la sua capacità di “raccogliere” l’ossigeno nei polmoni e di “rilasciarlo” alle cellule dei tessuti, è resa possibile da minuscoli cambiamenti conformazionali nella struttura quaternaria che avvengono nella molecola di emoglobina e che alterano l’affinità della tasca eme per l’ossigeno. L’Hb ha due stati strutturali quaternari: lo stato deoxy (bassa affinità di ossigeno) e lo stato oxy (alta affinità di ossigeno).
Una serie di fattori ambientali determina lo stato quaternario dell’Hb e quindi la sua affinità relativa all’ossigeno. Il microambiente nei polmoni favorisce lo stato oxy-quaternario e quindi l’Hb ha qui un’alta affinità per l’ossigeno.
Al contrario, il microambiente dei tessuti induce il cambiamento conformazionale nella struttura di Hb che riduce la sua affinità per l’ossigeno, permettendo così all’ossigeno di essere rilasciato alle cellule dei tessuti.
1.1. EMOGLOBINA ED ELIMINAZIONE DEL DIOSSIDO DI CARBONIO
Una piccola quantità (fino al 20%) di CO2 viene trasportata dai tessuti ai polmoni, legata in modo lasco all’aminoacido N-terminale delle quattro unità polipeptidiche della globina dell’emoglobina; il prodotto di questa combinazione è la carbamminoemoglobina. Tuttavia, la maggior parte della CO2 è trasportata come bicarbonato nel plasma sanguigno.
La conversione eritrocitaria di CO2 in bicarbonato, necessaria per questa modalità di trasporto della CO2, comporta la produzione di ioni idrogeno (H+). Questi ioni idrogeno sono tamponati dall’emoglobina deossigenata.
Il ruolo dell’emoglobina nel trasporto di ossigeno e anidride carbonica è riassunto nelle FIGURE 2a e 2b.
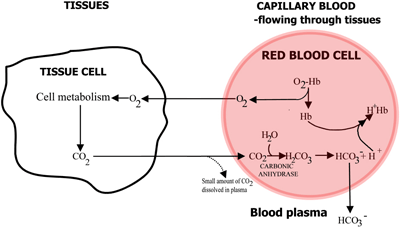
FIGURA 2a: TESSUTI O2 diffonde dal sangue ai tessuti, CO2 diffonde dai tessuti al sangue
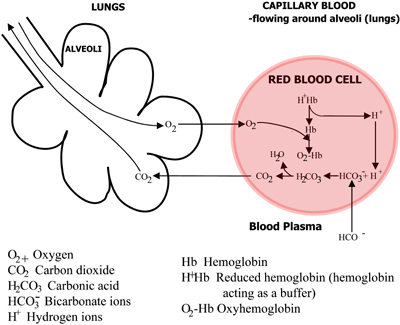
FIGURA 2b: LUNAGGI La CO2 diffonde dal sangue ai polmoni, l’O2 diffonde dai polmoni al sangue
Nel sangue capillare che scorre attraverso i tessuti l’ossigeno viene rilasciato dall’emoglobina e passa nelle cellule dei tessuti. L’anidride carbonica si diffonde dalle cellule dei tessuti negli eritrociti, dove l’enzima carbonico delle cellule rosse permette la sua reazione con l’acqua per formare acido carbonico.
L’acido carbonico si dissocia in bicarbonato (che passa nel plasma sanguigno) e ioni idrogeno, che si combinano con l’emoglobina ora deossigenata. Il sangue scorre verso i polmoni, e nei capillari degli alveoli polmonari i percorsi di cui sopra sono invertiti. Il bicarbonato entra negli eritrociti e qui si combina con gli ioni idrogeno, rilasciati dall’emoglobina, per formare acido carbonico.
Questo si dissocia in anidride carbonica e acqua. L’anidride carbonica si diffonde dal sangue negli alveoli dei polmoni e viene eliminata nell’aria espirata. Nel frattempo, l’ossigeno si diffonde dagli alveoli al sangue capillare e si combina con l’emoglobina.
1.2. EMOGLOBINA CHE NON PUÒ LEGARE L’OSSIGENO
Anche se normalmente presente solo in tracce, ci sono tre specie di emoglobina: la metemoglobina (MetHb o Hi), la solfemoglobina (SHb) e la carbossiemoglobina (COHb) che non possono legare l’ossigeno.
Sono quindi funzionalmente carenti, e l’aumento delle quantità di una qualsiasi di queste specie di emoglobina, di solito il risultato dell’esposizione a farmaci specifici o tossine ambientali, può compromettere seriamente la consegna di ossigeno.
Un resoconto completo della struttura e della funzione dell’emoglobina è fornito in riferimento.
ctHb, la concentrazione di emoglobina totale è tipicamente definita come la somma di emoglobina ossigenata, emoglobina deossigenata, carbossiemoglobina e metemoglobina.
UTILITÀ CLINICA DELLA MISURAZIONE della ctHb
La ragione principale per misurare la ctHb è il rilevamento dell’anemia e la valutazione della sua gravità.
L’anemia può essere definita come una riduzione della capacità del sangue di trasportare ossigeno dovuta a una riduzione del numero di eritrociti e/o una riduzione del ctHb, in modo che l’anemia è stabilita se il ctHb è al di sotto del limite inferiore dell’intervallo di riferimento (normale) (TABELLA I). Più basso è il ctHb, più grave è l’anemia.
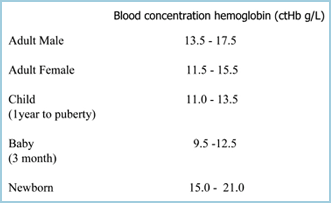
Tabella I: intervalli di riferimento ctHb (Rif 2)
L’anemia non è un’entità di malattia, piuttosto una conseguenza o un segno di malattia. La ragione per cui il ctHb è un esame del sangue così frequentemente richiesto è che l’anemia è una caratteristica di una serie di patologie, molte delle quali sono relativamente comuni (Tabella II).
Sintomi comuni, la maggior parte dei quali sono aspecifici, includono: pallore, stanchezza e letargia, mancanza di respiro – in particolare sullo sforzo, vertigini e svenimenti, mal di testa, stipsi e aumento della frequenza del polso, palpitazioni, tachicardia.

Tabella II: Alcune delle condizioni cliniche associate all’anemia
L’assenza di questi sintomi non esclude l’anemia; molti individui lievemente anemici rimangono asintomatici, soprattutto se l’anemia si è sviluppata lentamente.
2.2. POLICITEMIA
Mentre l’anemia è caratterizzata da una ctHb ridotta, una ctHb elevata indica policitemia. La policitemia nasce come risposta a qualsiasi condizione fisiologica o patologica in cui il sangue contiene meno ossigeno del normale (ipossiemia).
La risposta del corpo all’ipossiemia include un aumento della produzione di eritrociti per aumentare la consegna di ossigeno, e di conseguenza la ctHb si alza. Questa cosiddetta policitemia secondaria fa parte dell’adattamento fisiologico all’alta quota e può essere una caratteristica della malattia polmonare cronica.
La policitemia primaria è una neoplasia molto meno comune del midollo osseo chiamata policitemia vera, che è caratterizzata dalla produzione incontrollata di tutte le cellule del sangue, compresi gli eritrociti. La policitemia, secondaria o primaria, è generalmente molto meno comune dell’anemia.
3.1. PROSPETTIVA STORICA
Il primo test clinico di misurazione dell’Hb ideato più di un secolo fa prevedeva l’aggiunta di gocce di acqua distillata a un volume di sangue misurato fino a quando il suo colore corrispondeva a quello di uno standard artificiale colorato.
Una modifica successiva prevedeva la saturazione del sangue con gas di carbone (monossido di carbonio) per convertire l’emoglobina nella più stabile carbossiemoglobina. L’emoglobinometria moderna risale agli anni 50, dopo lo sviluppo della spettrofotometria e del metodo dell’emiglobincianuro (cinametemoglobina).
Seguì l’adattamento di questo metodo e di altri per l’uso in analizzatori ematologici automatizzati. Negli ultimi due decenni i progressi si sono concentrati sullo sviluppo di metodi che permettono il test point-of-care (POCT) dell’emoglobina.
Questa sezione si occupa prima della considerazione di alcuni dei metodi attualmente utilizzati in laboratorio e poi dei metodi POCT utilizzati fuori dal laboratorio.
3.2. HEMIGLOBINCYANIDE – UN METODO SPETTROFOTOMETRICO
Quasi 40 anni dopo essere stato adottato come metodo di riferimento per la misurazione dell’emoglobina dall’International Committee for Standardization in Hematology (ICSH), il test dell’emiglobincianuro (HiCN) rimane il metodo raccomandato dall’ICSH rispetto al quale vengono giudicati e standardizzati tutti i nuovi metodi ctHb.
La considerazione dettagliata che segue riflette la sua continua importanza sia come metodo di riferimento che di routine di laboratorio.
3.2.1. Principio del test
Il sangue viene diluito in una soluzione contenente ferricianuro di potassio e cianuro di potassio. Il ferricianuro di potassio ossida il ferro nell’eme allo stato ferrico per formare la metaemoglobina, che viene convertita in emiglobincianuro (HiCN) dal cianuro di potassio.
HiCN è un prodotto colorato stabile, che in soluzione ha un massimo di assorbanza a 540 nm e obbedisce strettamente alla legge di Beer-Lambert. L’assorbanza del campione diluito a 540 nm viene confrontata con l’assorbanza alla stessa lunghezza d’onda di una soluzione standard di HiCN la cui concentrazione di emoglobina equivalente è nota.
La maggior parte dei derivati dell’emoglobina (ossiemoglobina, metemoglobina e carbossiemoglobina, ma non la solfoemoglobina) vengono convertiti in HiCN e quindi misurati con questo metodo.
3.2.1.1. Diluente reagente (soluzione di Drabkin modificata)
| Ferricianuro di potassio (K3Fe(CN)6) | 200 mg |
| Cianuro di potassio (KCN) | 50 mg |
| Diidrogeno fosfato di potassio (KH2 PO4) | 140 mg |
| Non-detergente ionico (ad es.Triton X-100) | 1 mL |
| Sopra diluito a 1000 mL in acqua distillata |
3.2.1.2. Metodo manuale
25 µl di sangue vengono aggiunti a 5,0 mL di reagente, mescolati e lasciati per 3 minuti. L’assorbanza viene letta a 540 nm contro un bianco di reagente. L’assorbanza dello standard HiCN viene misurata nello stesso modo.
3.2.1.3. ICSH HiCN standard
Il vantaggio principale di questo metodo è che esiste una soluzione standard di HiCN prodotta e a cui viene assegnato un valore di concentrazione secondo criteri molto precisi stabiliti e rivisti periodicamente dall’International Council for Standardization in Hematology (ICSH).
Questa soluzione standard internazionale è il calibratore primario per le soluzioni standard commerciali utilizzate nei laboratori clinici di tutto il mondo. Pertanto, tutti coloro che utilizzano la standardizzazione HiCN stanno effettivamente utilizzando lo stesso standard, il cui valore è stato scrupolosamente convalidato.
3.2.1.4. Interferenza
La turbolenza dovuta a proteine, lipidi e materia cellulare è un problema potenziale nella stima spettrofotometrica di qualsiasi costituente del sangue, compresa l’emoglobina.
La grande diluizione (1:251) del campione elimina in gran parte il problema, ma risultati ctHb falsamente elevati possono verificarsi in pazienti la cui concentrazione di proteine plasmatiche è particolarmente elevata.
Anche i campioni fortemente lipemici e quelli contenenti un numero molto elevato di globuli bianchi (leucociti) possono aumentare artificialmente la ctHb con un meccanismo simile
3.2.1.5. Vantaggi dell’HiCN
- Standard internazionale – accurato
- Facilmente adattabile agli analizzatori ematologici automatizzati; quindi riproducibile (bassa SD e CV – entro il lotto CV tipicamente
- Ben stabilito e studiato a fondo – ICSH raccomandato
- Reagente poco costoso
3.2.1.6. Svantaggi di HiCN
- Il metodo manuale richiede un pipettaggio accurato e uno spettrofotometro
- Il reagente (cianuro) è pericoloso
- Il suddetto limita il suo uso fuori dal laboratorio
- Soggetto a interferenze da lipidi, proteine del plasma e numero di leucociti in aumento
- Non distingue i derivati dell’emoglobina che non hanno capacità di trasportare ossigeno (MetHb, COHb, SHb). Quindi può sovrastimare la capacità di trasporto di ossigeno del sangue se questi sono presenti in quantità anormali (più che tracce).
3.3. METODI DI LABORATORIO ALTERNATIVI (SENZA CIANURO)
Il laurilsolfato di sodio (SLS) è un tensioattivo che liscia gli eritrociti e forma rapidamente un complesso con l’emoglobina liberata. Il prodotto SLS-MetHb è stabile per alcune ore e ha uno spettro caratteristico con assorbimento massimo a 539 nm.
Il complesso obbedisce alla legge di Beer-Lambert, per cui esiste una precisa correlazione lineare tra la concentrazione di Hb e l’assorbanza di SLS-MetHb.
Il metodo consiste semplicemente nel mescolare 25 µL di sangue con 5,0 mL di una soluzione di SLS da 2,08 mmol/L (tamponata a pH 7,2), e leggere l’assorbanza a 539 nm. I risultati di ctHb con il metodo SLS-Hb hanno dimostrato di correlare molto strettamente (r = 0,998) con il metodo HiCN di riferimento.
Il metodo è stato adattato per gli analizzatori ematologici automatizzati ed è affidabile in termini di accuratezza e precisione come i metodi automatizzati HiCN. Un grande vantaggio è che il reagente non è tossico. È anche meno incline alle interferenze della lipemia e all’aumento della concentrazione di leucociti.
L’instabilità a lungo termine di SDS-MetHb preclude il suo uso come standard, quindi il metodo deve essere calibrato con sangue la cui ctHb è stata determinata utilizzando il metodo HiCN di riferimento.
3.3.2. Metodo dell’azide-metemoglobina
Questo metodo si basa sulla conversione dell’emoglobina in un prodotto colorato stabile azide-metemoglobina che ha uno spettro di assorbanza quasi identico a quello di HiCN .
Il reagente utilizzato in questo metodo è molto simile a quello utilizzato nel metodo di riferimento HiCN con la sostituzione dell’azoturo di sodio con il più tossico cianuro di potassio. Come nel metodo HiCN, l’emoglobina viene convertita in metaemoglobina dal ferricianuro di potassio; l’azide forma quindi un complesso con la metaemoglobina.
I risultati dictHb con questo metodo sono comparabili ai risultati ottenuti con il metodo HiCN di riferimento; questo è un metodo manuale alternativo accettabile. Il potenziale esplosivo della sodio azide, tuttavia, impedisce il suo utilizzo su analizzatori ematologici automatizzati. La reazione azide-MetHb è stata adattata agli emoglobinometri POCT.
3.4. I metodi POCT qui considerati sono:
- Emoglobinometri portatili
- CO-ossimetria – un metodo utilizzato negli analizzatori di gas sanguigni POCT
- Scala dei colori WHO
3.4.1. Emoglobinometri portatili
Gli emoglobinometri portatili come l’HemoCue-B permettono una determinazione accurata dell’emoglobina al letto del paziente. Sono essenzialmente fotometri che permettono di misurare l’intensità del colore delle soluzioni.
La microcuvetta monouso in cui vengono effettuate queste misurazioni funge anche da recipiente di reazione. I reagenti necessari sia per il rilascio di Hb dagli eritrociti che per la conversione di Hb in un prodotto colorato stabile sono presenti in forma essiccata sulle pareti della cuvetta.
Basta introdurre un piccolo campione (tipicamente 10 µL) di sangue capillare, venoso o arterioso nella microcuvetta e inserire la microcuvetta nello strumento.
Lo strumento è precalibrato in fabbrica utilizzando lo standard HiCN, e l’assorbanza della soluzione del test viene automaticamente convertita in ctHb. Il risultato viene visualizzato in meno di un minuto.
3.4.1.1. I vantaggi dei moderni emoglobinometri includono
- Portabilità
- Funzionamento a batteria o a rete, può essere usato ovunque
- Piccolo volume di campione (10 µL) ottenuto tramite puntura del dito
- Veloce (risultato in 60 secondi)
- Facilità d’uso – nessun pipettaggio
- Minima formazione richiesta dal personale non di laboratorio
- Standardizzato contro HiCN – risultati comparabili a quelli ottenuti in laboratorio
- Correzione della torbidità. In questo senso gli emoglobinometri portatili sono superiori alla maggior parte dei metodi ctHb.
Questa tecnologia è stata ampiamente valutata in una serie di impostazioni e la maggior parte degli studi ha confermato un’accuratezza e una precisione accettabili rispetto ai metodi di laboratorio.
3.4.1.2. Svantaggi
Alcuni studi, tuttavia, hanno sollevato la preoccupazione che nelle mani di personale non di laboratorio i risultati possano essere meno soddisfacenti. Nonostante la semplicità di funzionamento, questi strumenti non sono immuni da errori dell’operatore, e una formazione efficace è essenziale.
Ci sono prove che suggeriscono che i risultati derivati da campioni capillari (puntura del dito) sono meno precisi di quelli derivati da campioni capillari o venosi ben miscelati raccolti in bottiglie EDTA. CO-ossimetria
Un CO-ossimetro è uno spettrofotometro specializzato, il nome riflette l’applicazione originale, che era di misurare COHb e MetHb.
Molti moderni analizzatori di gas sanguigni hanno un CO-ossimetro incorporato, permettendo la stima simultanea della ctHb durante l’analisi dei gas sanguigni.
La misurazione della ctHb tramite CO-ossimetria si basa sul fatto che l’emoglobina e tutti i suoi derivati sono proteine colorate che assorbono la luce a lunghezze d’onda specifiche e quindi hanno uno spettro di assorbanza caratteristico (FIGURA 3).
La legge di Beer-Lambert detta che l’assorbanza di un singolo composto è proporzionale alla concentrazione di quel composto. Se la caratteristica spettrale di ogni sostanza assorbente in una soluzione è nota, le letture di assorbanza della soluzione a lunghezze d’onda multiple possono essere utilizzate per calcolare la concentrazione di ogni sostanza assorbente.
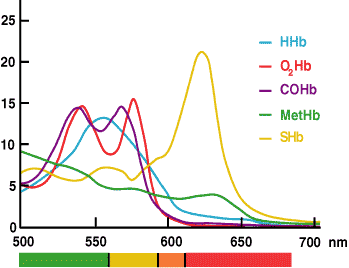
FIGURA 3.
Nel CO-ossimetro le misure di assorbanza di un campione di sangue emolizzato a lunghezze d’onda multiple attraverso l’intervallo in cui le specie di emoglobina assorbono la luce (520-620 nm) sono utilizzate dal software installato per calcolare la concentrazione di ciascuno dei derivati dell’emoglobina (HHb, O2Hb, MetHb e COHb). Il ctHb è la somma calcolata di questi derivati.
Tutto ciò che è richiesto all’operatore è l’iniezione di un campione di sangue arterioso ben miscelato nell’analizzatore di gas sanguigni/CO-ossimetro.
Il campione, o una parte di esso, viene automaticamente pompato nella cuvetta di misurazione del CO-ossimetro, dove – per azione chimica o fisica – gli eritrociti vengono lisati per rilasciare l’emoglobina, che viene analizzata spettroscopicamente come descritto sopra.
I risultati vengono visualizzati insieme ai risultati dei gas sanguigni entro uno o due minuti.
Diversi studi hanno confermato che i risultati ctHb ottenuti con la CO-ossimetria non sono clinicamente molto diversi da quelli derivati dai metodi di laboratorio di riferimento. La CO-ossimetria fornisce un mezzo accettabile per la stima urgente della ctHb in un contesto di assistenza critica.
3.4.2.1. I particolari vantaggi della ctHb tramite CO-ossimetria includono
- Velocità di analisi
- Facilità di analisi
- Piccolo volume di campione
- Nessun costo di capitale o di consumo oltre a quello richiesto per l’analisi dei gas sanguigni
- Parametri aggiuntivi (MetHb, COHb, O2Hb) misurati
- Non influenzati da un alto numero di globuli bianchi
3.4.3. WHO hemoglobin color scale (HCS)
Sviluppato per l’Organizzazione Mondiale della Sanità (OMS), questo test a bassa tecnologia ha un’applicazione limitata nei paesi sviluppati ma ha un’enorme importanza per i paesi economicamente deprivati del mondo in via di sviluppo, dove l’anemia è più diffusa.
Nelle aree in cui non ci sono strutture di laboratorio e risorse insufficienti per finanziare emoglobinometri POCT più sofisticati, è praticamente l’unico mezzo per determinare il ctHb.
Il test HCS si basa sul semplice principio che il colore del sangue è una funzione del ctHb. Una goccia di sangue viene assorbita su carta e il suo colore viene confrontato con una tabella di sei tonalità di rosso, ogni tonalità rappresenta una ctHb equivalente: la più chiara 40 g/L e la più scura 140 g/L. Anche se in linea di principio è molto semplice, nello sviluppo sono state utilizzate notevoli ricerche e tecnologie per garantire la massima accuratezza e precisione possibile.
Per esempio, la scelta finale della carta per la matrice della striscia reattiva è stata basata su prove approfondite di diverse carte e sull’analisi spettrofotometrica del sangue e delle miscele di coloranti per arrivare alla corrispondenza più vicina possibile tra il colore della carta e il colore del sangue ad ogni ctHb di riferimento.
3.4.3.1. Vantaggi del test HCS
- È facile da usare – richiede solo 30 minuti di addestramento
- Non richiede attrezzature o energia
- È veloce – risultato entro 1 minuto
- Richiede solo un campione (capillare) dal dito
- È molto economico (circa 0,12 dollari per test)
3.4.3.2. Svantaggi del test HCS
I risultati affidabili dipendono dalla stretta osservanza delle istruzioni del test.
Gli errori comuni includono:
- Sangue inadeguato o eccessivo sulla striscia reattiva
- Lettura del risultato troppo tardi (oltre 2 minuti) o troppo presto (meno di 30 secondi)
- Lettura del risultato in condizioni di scarsa illuminazione
Il test HSC ha chiaramente dei limiti intrinseci. Al massimo può determinare che il ctHb di un campione del paziente si trova all’interno di uno dei sei intervalli di concentrazione: 30-50 g/L, 50-70 g/L, 70-90 g/L, 90-110 g/L, 110-130 g/L o 130-150 g/L. Ancora questo è teoricamente sufficiente per identificare tutti, ma i pazienti più lievemente anemici e dare un’indicazione della gravità.
Un primo studio ha dimostrato la capacità del test di identificare l’anemia (definito come ctHb
SUMMARIO
ctHb è uno dei due parametri abitualmente utilizzati per valutare la capacità di trasporto di ossigeno del sangue e quindi stabilire una diagnosi di anemia e policitemia.
Il test alternativo, chiamato ematocrito (Hct) o Packed Cell Volume (PCV), è stato oggetto di un precedente articolo di accompagnamento, dove è stata discussa la relazione tra ctHb e Hct. L’obiettivo di questo articolo è la misurazione della ctHb.
Sono stati ideati numerosi metodi, la maggior parte basati sulla misurazione del colore dell’emoglobina o di un suo derivato. Per questa breve rassegna è stato inevitabilmente necessario essere selettivi. I metodi scelti per la discussione sono tra i più comunemente usati oggi.
Nel fare la selezione è stato fatto un tentativo di trasmettere la gamma di tecnologie che sono attualmente impiegati e come questi sono applicati per soddisfare la domanda clinica di ctHb in ambienti che vanno dalle aree povere del mondo in via di sviluppo, dove l’assistenza medica ha appena un punto d’appoggio, al mondo high-tech della moderna unità di terapia intensiva.




