パーフェクトスコアラー試験対策 化学 飽和」という言葉の意味とは?
化学では、飽和という言葉は個々の分子や溶質・溶媒の混合物全体を表すのに使われ、それぞれの状況で異なる意味を持ちます。
一般的には、飽和スポンジ(水で満たされたもの)や飽和爆撃(数百個の爆弾を使って地域全体を破壊)のように、何かが完全に満ちていることを意味します。
飽和分子と不飽和分子
この言葉が個々の分子に適用される場合、その分子は炭素-炭素二重結合や環を持っていないことを意味します。 下の分子では、単結合を二重結合に変えるということは、2 つの水素原子を取り除かなければならないことに注目してください。
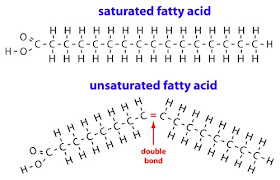
炭素には 4 つの結合しかないので、C=C 二重結合を追加すると、代わりに水素を結合させることができた 2 箇所を使います。 2番目の分子は二重結合を持っているので、それは潜在的に保持することができるすべての水素を持っていない、とそれはunsaturated.
Important.Importantです。 脂肪酸は、分子の炭化水素鎖部分が二重結合を含んでいない場合、飽和とみなされます。 分子の左端にあるCOOH基のC=Oは考慮されません。
また、環の存在も分子を不飽和にすることに注意してください。 直鎖と分岐のペンタンはどちらも式C5H12で、環状の分子であるシクロペンタンは式C5H10です。 直鎖や分岐鎖の炭化水素は飽和、環状の炭化水素は不飽和です。
ちなみに、過飽和の分子というのはありません。
ところで、過飽和分子というものはありません。テストでその選択肢があったら、それはひっかけ問題です。
飽和、不飽和、および過飽和溶液
飽和という言葉は、溶液について述べるときに別の意味を持ちます。
以下の定義について、溶媒とは溶質が溶ける化学物質であると覚えておいてください。 例えば、食塩水は水(溶媒)中の塩化ナトリウム(溶質)の溶液です。
溶媒は通常液体ですが、液体である必要はありません:空気は窒素(溶媒)中の酸素、二酸化炭素、水蒸気(溶質)の溶液です。

飽和溶液は、溶媒が保持できる限り多くの溶質を含んでいます。 死海は飽和状態であり、持てる限りの塩分とミネラルを含んでいる。塩分が多いため、水の密度は人間の体よりも高く、人は簡単に水に浮かぶことができる。 右の写真で、白い固まりは、水がすでに飽和しているために溶けることができない塩のかけらです。
不飽和溶液は、溶媒が保持できる量より少ない溶質を含みます。
死海とは異なり、通常の海水は不飽和です。
死海とは異なり、通常の海水は不飽和です。塩分が非常に高いにもかかわらず、保持できる量の塩を含んでいません。
過飽和溶液は、溶媒が保持できるはずの量より多くの溶質を含みます。
砂糖水を煮てから冷却すると、過飽和になって氷菓ができます:砂糖は溶液から出るはずですが、種の結晶を落とすまでそうなりません。 (種結晶がないことも、冬に木が凍らない理由の1つです。)
以下のビデオでは、酢酸ナトリウムの過飽和溶液を自分で作り、それを使って「熱い氷」の彫刻を作る方法を紹介しています:
また、以下の用語も知る必要があるでしょう:
希釈溶液には溶質の量に対して非常に少ない溶質が含まれている。
濃縮溶液は、溶媒の量に対して多くの溶質を含んでいます。
トリック問題
よくあるトリック問題は、飽和、不飽和、過飽和、希薄、濃縮の用語を正しく区別することを問うものです。
溶液は飽和でもあり希薄でもあります。例えば、湖の水にヨウ素の結晶を加えて細菌を殺すときなど、溶解度が低い場合、溶液は飽和(溶質でいっぱい)であると同時に希薄(あまり濃くない)であることになります。 I2が非極性であまり水に溶けないのは良いことです。もし溶液が濃縮されていたら、元素状ハロゲンを大量に飲むことになります!
一方、海水は不飽和と濃縮の両方です。
死海は飽和と濃縮の両方です。




