メカニズム – イブプロフェン(アドビル、モトリン)がアスピリンの抗血栓活性を阻害する仕組み
簡単な文献検索をすれば、このテーマについて議論し、討論し、さらには論争する多くの論文に出会うことでしょう。これらの問題のすべての理由は、使用したイブプロフェンの用量と期間、アスピリン投与との関連でイブプロフェン投与のタイミング、使用したアスピリンの用量と製剤(腸溶性または非腸溶性)、研究対象患者集団(健康ボランティア vs. アスピリン)において研究間で多数の矛盾があることと関係があると我々は考えている。 また、血小板凝集を実際に評価する検査ではなく、代理検査マーカーが使用されたかどうか、最後に、研究結果を得るために研究者が使用した研究デザインも重要です1-6。 このように、互いに限界や矛盾のあるこれらの研究から現在のデータを推定し、一般集団に適用可能な臨床的に意味のあるエンドポイントに実際に変換できる決定的な答えを出すことは非常に難しく、ほぼ不可能と言えます。 文献上の矛盾のいくつかは、非ステロイド性抗炎症薬(NSAIDs)の濃度が低いときと、濃度が高い投与後初期とで、血小板が凝集しやすいことに起因しているかもしれません7。
米国食品医薬品局(FDA)の医療関係者への警告では、「即時型アスピリン(腸溶性でない)を使用している患者がイブプロフェン400mgを単回投与する場合は、アスピリンの効果の減衰を避けるために、アスピリン摂取後少なくとも30分以上、あるいはアスピリン摂取の8時間以上前にイブプロフェンを投与すること」と述べられています。 この勧告に基づき、本号では、このテーマで発表されたすべての研究を批判するのではなく、薬物相互作用のメカニズムについて説明し、医学文献との関連でその解釈の問題点を明らかにすることを目的としています。
正常な血小板凝集では何が起こっているのか
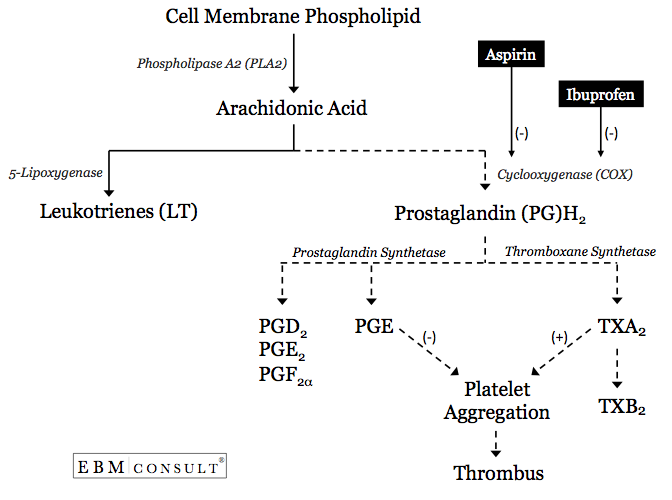
- 血小板凝集の増加プロセスは、血小板の細胞膜からアラキドン酸(AA)が放出されることから始まります6。
- TXA2が形成されると、血小板凝集が促進または助長されます。10 これは、AAが疎水性チャネルを移動して、COX-1酵素内の触媒部位と接触できる場合に特に起こります。 このチャネルまたは触媒部位の周囲がブロックされると、AAがPGH2、さらにTXA2へと代謝されなくなり、血小板凝集の可能性が低下します6、9、11。
それでは、アスピリンはどのように血小板凝集を阻害するのでしょうか?
- アスピリンを投与すると、疎水性チャネル内の529位のセリン残基が不可逆的にアセチル化され、COX-1酵素によってAAから血小板由来のTXA2へと代謝できる触媒部位と近接した場所になります6, 9,11. この部分がアセチル化されると、COX-1内の触媒部位にAAがアクセスできなくなるブロックが形成される。
- アスピリンは不可逆的にこれを行うので、AAを代謝するCOX-1酵素内のその触媒部位の能力は、その血小板の寿命(通常約7〜12日)の間、ブロックまたは阻害されます。 これは、アスピリンが主に二次予防に使用される場合、心血管イベントに対して心臓保護効果をもたらす主な理由の1つです。
- したがって、他の何かがアスピリンがCOX-1酵素内のこのセリン残基をアセチル化するのを競合またはブロックすると、心臓保護効果が減少する可能性があります。
イブプロフェンはどのようにアスピリンの薬理活性を妨げるのか?
- すべてのNSAIDsと同様に、イブプロフェンはCOX-1酵素の疎水チャネル内のAA代謝の触媒部位に対して可逆的で競合的な阻害剤である7,12。
- この疎水性チャネル内にイブプロフェンが存在すると、アスピリンがAAの触媒部位に近接するセリン残基をアセチル化するのを競合的にブロックする。
- イブプロフェンがアスピリンの薬理効果を発揮するのをどの程度抑制するかは、多くの要因によって影響を受けそうである。
まず最も明白な要因は、アスピリンとイブプロフェンが互いに関連して投与される順序に関係している。 アスピリンが先に投与されると、COX-1酵素内のセリン残基を不可逆的にアセチル化するためにアクセスすることになる。 アスピリンがCOX-1酵素を不可逆的に阻害すれば、抗血小板効果はその血小板の寿命まで続くことを覚えておいてください。 次に、アスピリン併用時のイブプロフェン濃度である。 イブプロフェンの阻害は競合的であるため、血小板凝集はイブプロフェンの濃度に影響されるだけでなく、性質上可逆的である。 したがって、薬物レベルが排泄経路を通じて減少すると、アスピリンの活性部位へのアクセスを阻害できるイブプロフェンの量も減少し、特に半減期が2〜4時間と短いことを考えると、この薬物動態上の特性は、アスピリンが1日1回の投与であるのに対し、イブプロフェンは1日に何度も投与しなおさなければならない理由にもなっています14。 したがって、医学文献に掲載された複数の研究結果にはばらつきがあることがわかる。 このように、この薬物相互作用の臨床的影響は、2つの薬剤の投与順序、使用するアスピリンの用量と製剤、使用するイブプロフェンの用量と投与頻度、研究対象患者集団、およびその研究のエンドポイントの種類によって影響されるのです。
結局のところ、本当の問題は、この相互作用が、臨床的に関連する、あらかじめ定義された患者指向の心血管系の定義されたアウトカムにつながるかどうかということなのです。
- GengoFM, Rubin L, Robson M et al. Effects of ibuprofen on the magnitude and duration of aspirin’s inhibition of platelet aggregation: clinical consequencesin stroke prophylaxis. J Clin Pharmacol 2008;48:117-22.
- GladdingPA, Webster MWI, Farrell HB et al. 健康なボランティアにおける6種類の非ステロイド性抗炎症薬の抗血小板効果とそのアスピリンとの薬力学的相互作用。 Am J Cardiol 2008;101:1060-1063.
- CryerB, Berlin RG, Copper SA et al. アスピリン治療を受けた健康成人ボランティアにおけるトロンボキサンB2濃度に対するイブプロフェンの効果に関する二重盲検無作為並行プラセボ対照研究(Double Blind, randomized, parallel, placebo-controlled study on thromboxane B2 concentrations in aspirin-treated healthy adult volunteers. Clin Ther2005;27:185-191.
- MacDonaldTM, Wei L et al. Effect of ibuprofen on cardioprotective effect ofaspirin.(イブプロフェンがアスピリンの心保護作用に及ぼす影響)。 Lancet 2003;361:573-74.
- KurthT, Glynn RJ, Walker AM et al. Inhibition of clinical benefits of aspirinonon first myocardial infarction by nonsteroidal antiinflammatory drugs.アスピリンによる初回心筋梗塞に対する臨床効果の阻害。 Circulation 2003;108:1191-1195.
- Catella-LawsonF, Reilly MP, Kapoor SC et al. Cyclooxygenase inhibitors and theantiplatelet effects of aspirin.シクロオキシゲナーゼ阻害剤とアスピリン抗血小板作用。 N Engl J Med 2001;345:1809-17.
- EvansAM. プロフェンの薬力学と薬物動態:エナンチオ選択性、臨床的意味、特にS(+)-イブプロフェンについて。 J Clin Pharmacol 1996;36:7S-15S.
- Food&Drug Administration. 医療従事者向け情報:イブプロフェンとアスピリンの併用について。 米国保健省&人間福祉局。 最終アクセス: 09-19-2011.
- FunkCD, Funk LB, Kennedy ME et al. Human platelet/erythroleukemia cellprostaglandin G/H synthase: cDNA cloning, expression, and gene chromosomalassignment. FASEB J 1991;5:2304-12.
- フィッツジェラルドGA. 血小板活性化のメカニズム:他のアゴニストに対する増幅シグナルとしてのトロンボキサンA2. Am J Cardiol 1991;68:11B-15B.
- LollPJ, Picot D, Garavito RM. 不活性化プロスタグランジンH2合成酵素の結晶構造から推測されるアスピリン活性の構造基盤。 Nat Struct Biol 1995;2:637-43.
- LollPJ, Picot D, Ekabo O et al. Synthesis and use of iodinated nonsteroidalantiinflammatory drug analogs as crystallographic probes of the prostaglandinH2 synthase cyclooxygenase active site.(「プロスタグランジンH2合成酵素の活性部位の結晶構造解析プローブとして、非ステロイド性抗炎症薬アナログの生成と使用」)。 Biochemistry 1996;35:7330-40.
- RaoGH, Johnson GG, Reddy KR et al. Ibuprofen protects plateletcyclooxygenase from irreversible inhibition by aspirin.イブプロフェンはアスピリンによる血小板シクロオキシゲナーゼの不可逆的阻害から保護する。 動脈硬化 1983;3:383-8.
.




