Fontan手術後のAmplatzerデバイスによるBlalock-Taussigシャントの閉鎖|Revista Española de Cardiología
編集部へ:
心臓カテーテル治療は、さまざまな先天性心疾患や術直後および術後の後遺症を治療するのに、有効な介入であると言えます。 このたび,Fontan手術で結紮できなかったBlalock-Taussigシャントを有する男児の症例を報告する. 現在7歳の男児は,新生児期に肺閉鎖,心室中隔欠損,右室低形成を伴う大血管L型転位と診断され,その後,肺閉鎖,心室中隔欠損,右室低形成を伴う大血管L型転位と診断された. 新生児期にBlalock-Taussigシャントが施行され,その後2歳時に双方向Glennインターベンションが施行された. Fontan手術終了前に行われた心臓カテーテル検査では,肺動脈の口径は良好であった. 平均血圧は14mmHgで,Blalock-Taussigシャントが開存していた. 下大静脈と右肺動脈との間に心臓外導管が設置された. Blalock-Taussigシャントは,アクセスが困難であったため,開口したままとした. 術後すぐに,治療抵抗性の重篤な全身性静脈うっ血を呈したため,経皮的にシャントを閉鎖することにした. 術後3週間後の心臓カテーテル検査では、平均肺動脈血圧は29mmHgで、シャントの直径は3.6mmで、全身-肺の流れ(Qp/Qs=1.3/1)を示していました(図1A)。 大腿動脈からのアプローチでシャントを閉鎖しようとしましたが、シャントと下行大動脈の角度がきついため、前進はほとんど不可能でした。 そこで,左腋窩動脈から4×6 mmのAmplatzer ductal device(AGA Medical Corporation®)を留置することにした(図1B)。 デバイス設置後、血管造影でシャントの完全閉鎖を確認し(図1C)、デバイスの左肺動脈への突出もなかった。 閉塞後の平均肺動脈圧は16mmHgまで低下し,患者は翌週に退院した
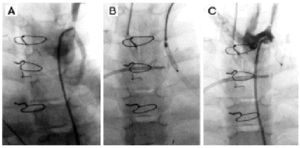
図1. Amplatzerデバイス移植前(A),移植後(C)のBlalock-Taussigシャントの血管造影。 Fontan手術を受けた患者の全身-肺シャントは,血行動態に明らかに悪影響を及ぼす。 外科的な結紮は技術的に困難であるため、経皮的なカテーテル操作によりシャントを閉鎖することができる。 1989年、Perryら4名は、シャント閉鎖に使用したコイルの8%が他の血管を塞栓したと報告している。 Blalock-Taussigシャントでは、望ましくない塞栓の割合が21%と高い。 Burrowsら2 は、Blalock-Taussigシャントをコイルで閉鎖しようとしたところ、29%の患者で肺循環の塞栓を引き起こしたことを明らかにした。 ガイドワイヤーの使用5や肺動脈にステントを留置するなど、肺循環の塞栓を防ぐための他の手法も用いられている6
本患者に対しては、コイルの使用による塞栓のリスクが高いこと、患者の状態が不安定なことから、Amplatzer ductal deviceを使用することにした。 閉塞を行う前に、留置後のデバイスの長さを推定した。 そのため、肺動脈や左鎖骨下動脈への突出を避けるために、シャントより短くすることができ、実際に突出がないことを確認した。 この手技を行う上で、左腋窩動脈からのアクセスの重要性は強調されるべきであろう。 大腿静脈経由ではほとんど不可能であり、この症例ではさらにリスクの高い手術が必要であったと思われる。




