Încălcări ale regulii octetului
Excepția 2: Octeți incompleți
A doua excepție de la regula octetului este atunci când există prea puțini electroni de valență, ceea ce duce la un octet incomplet. Există și mai multe ocazii în care regula octetului nu oferă cea mai corectă reprezentare a unei molecule sau a unui ion. Acesta este, de asemenea, cazul octeților incompleți. Speciile cu octeți incompleți sunt destul de rare și, în general, se găsesc doar în unii compuși de beriliu, aluminiu și bor, inclusiv în hidrurile de bor. Să ne uităm la o astfel de hidrură, \(BH_3\) (Boran).
Dacă ar fi să facem o structură Lewis pentru \(BH_3\) urmând strategiile de bază pentru desenarea structurilor Lewis, probabil că am obține această structură (figura 3):
Problema cu această structură este că borul are un octet incomplet; are doar șase electroni în jurul său. Atomii de hidrogen pot avea, în mod natural, doar 2 electroni în învelișul lor cel mai exterior (versiunea lor de octet) și, ca atare, nu există electroni de rezervă pentru a forma o legătură dublă cu borul. S-ar putea presupune că eșecul acestei structuri de a forma octeți compleți trebuie să însemne că această legătură ar trebui să fie ionică în loc de covalentă. Cu toate acestea, borul are o electronegativitate foarte asemănătoare cu cea a hidrogenului, ceea ce înseamnă că legăturile dintre hidrogen și bor sunt probabil foarte puțin ionice și, ca atare, această structură Lewis, deși nu îndeplinește regula octetului, este probabil cea mai bună structură posibilă pentru reprezentarea BH3 cu ajutorul teoriei Lewis. Unul dintre lucrurile care pot explica octetul incomplet al BH3 este faptul că acesta este în mod obișnuit o specie tranzitorie, formată temporar în reacții care implică mai multe etape.
Să aruncăm o privire la o altă situație de octet incomplet care are de-a face cu borul, BF3 (bor trifluorină). Ca și în cazul BH3, desenul inițial al unei structuri Lewis a BF3 va forma o structură în care borul are doar șase electroni în jurul său (figura 4).
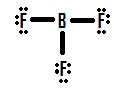
Dacă vă uitați la figura 4, puteți vedea că atomii de fluor posedă perechi solitare suplimentare pe care le pot folosi pentru a face legături suplimentare cu borul, și ați putea crede că tot ce trebuie să faceți este să transformați o pereche solitară într-o legătură și structura va fi corectă. Dacă adăugăm o legătură dublă între bor și unul dintre fluoruri, obținem următoarea structură Lewis (figura 5):
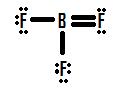
Care fluor are opt electroni, iar atomul de bor are și el opt! Fiecare atom are un octet perfect, nu-i așa? Nu atât de repede. Trebuie să examinăm sarcinile formale ale acestei structuri. Fluorul care împarte o legătură dublă cu borul are șase electroni în jurul său (patru de la cele două perechi de electroni solitari și câte unul de la cele două legături cu borul). Acesta este cu un electron mai puțin decât numărul de electroni de valență pe care l-ar avea în mod natural (elementele din grupa șapte au șapte electroni de valență), astfel că are o sarcină formală de +1. Cele două flourine care împart legături simple cu borul au șapte electroni în jurul lor (șase de la cele trei perechi solitare și unul de la legăturile simple cu borul). Aceasta este aceeași cantitate ca și numărul de electroni de valență pe care le-ar avea singure, deci ambele au o sarcină formală de zero. În cele din urmă, borul are patru electroni în jurul său (câte unul din fiecare dintre cele patru legături pe care le are cu fluorul). Acesta este cu un electron mai mult decât numărul de electroni de valență pe care borul i-ar avea de unul singur și, ca atare, borul are o sarcină formală de -1.
Această structură este susținută de faptul că lungimea de legătură determinată experimental a legăturilor dintre bor și fluor în BF3 este mai mică decât cea care ar fi tipică pentru o legătură simplă (a se vedea Ordinea și lungimile legăturilor). Totuși, această structură contrazice una dintre regulile majore ale sarcinilor formale: Se presupune că sarcinile formale negative trebuie să se regăsească pe atomul (atomii) mai electronegativ(i) dintr-o legătură, dar în structura descrisă în figura 5, o sarcină formală pozitivă se regăsește pe fluor, care nu numai că este elementul cel mai electronegativ din structură, dar este și elementul cel mai electronegativ din întregul tabel periodic (\(\chi=4,0\)). Pe de altă parte, borul, cu o electronegativitate mult mai mică, de 2,0, are sarcina formală negativă în această structură. Acest dezacord sarcină formală-electronegativitate face imposibilă această structură cu dublă legătură.
Cu toate acestea, diferența mare de electronegativitate de aici, spre deosebire de cea din BH3, semnifică legături polare semnificative între bor și fluor, ceea ce înseamnă că această moleculă are un caracter ionic ridicat. Acest lucru sugerează posibilitatea unei structuri semi-ionice, așa cum se vede în figura 6:

Niciuna dintre aceste trei structuri nu este structura „corectă” în acest caz. Cea mai „corectă” structură este, cel mai probabil, o rezonanță a tuturor celor trei structuri: cea cu octet incomplet (figura 4), cea cu dublă legătură (figura 5) și cea cu legătură ionică (figura 6). Structura care contribuie cel mai mult este probabil structura cu octet incomplet (din cauza faptului că figura 5 este practic imposibilă, iar figura 6 nu se potrivește cu comportamentul și proprietățile BF3). După cum puteți vedea, chiar și atunci când există alte posibilități, octeții incompleți pot descrie cel mai bine o structură moleculară.
Ca o notă secundară, este important de remarcat că BF3 se leagă frecvent cu un ion F- pentru a forma BF4-, mai degrabă decât să rămână ca BF3. Această structură completează octetul borului și este mai frecventă în natură. Acest lucru exemplifică faptul că octetele incomplete sunt rare, iar alte configurații sunt de obicei mai favorabile, inclusiv legarea cu ioni suplimentari, ca în cazul BF3 .
Exemplu: \(BF_3\)
Desenați structura Lewis pentru trifluorura de bor (BF3).
Soluție
1. Adăugați electroni (3*7) + 3 = 24
2. Desenați conectivitățile:
3. Adăugați octeți la atomii externi:
4. Adăugați electroni în plus (24-24=0) la atomul central:
5. Electronul central are octet?
- NO. Are 6 electroni
Adaugați o legătură multiplă (legătură dublă) pentru a vedea dacă atomul central poate obține un octet:
6. Borul central are acum un octet (ar exista trei structuri Lewis de rezonanță)
Dar…
- În această structură cu legătură dublă, atomul de fluor împarte electroni în plus cu borul.
- Fluorul ar avea o sarcină parțială „+”, iar borul o sarcină parțială „-„, acest lucru nu este în concordanță cu electronegativitățile fluorului și borului.
- Din acest motiv, structura BF3, cu legături simple și 6 electroni de valență în jurul borului central este cea mai probabilă structură
- BF3 reacționează puternic cu compuși care au o pereche de electroni neîmpărtășită care poate fi folosită pentru a forma o legătură cu borul:




