Perfect Scorer Test Prep: Chemistry: Vad betyder ordet ”mättad”?
I kemi kan ordet mättat användas för att beskriva enskilda molekyler eller hela lösningar/lösningsmedelsblandningar, och det har en annan innebörd i var och en av dessa situationer.
I allmänhet är något som är mättat helt fullt, som i en mättad svamp (en svamp som är fylld med vatten) eller mättnadsbombning (användning av hundratals bomber för att förstöra ett helt område).
Mättade och omättade molekyler
När ordet appliceras på en enskild molekyl betyder det att molekylen inte har några kol-kol dubbelbindningar eller ringar. I molekylerna nedan, lägg märke till att om man ändrar en enkelbindning till en dubbelbindning innebär det att man måste ta bort två väteatomer:
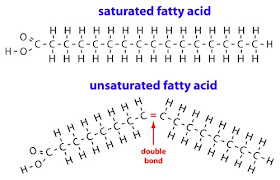
Då kol bara kan ha fyra bindningar, använder tillägget av en C=C-dubbelbindning två ställen som väteatomer kunde ha bundits till i stället.
Den första molekylen har så många väteatomer som den kan rymma (inga dubbelbindningar), så den är mättad, eller full av väteatomer. Eftersom den andra molekylen har en dubbelbindning har den inte alla de väteatomer som den potentiellt skulle kunna ha, och den är omättad.
Viktigt: Fettsyror anses vara mättade om molekylens del av kolvätekedjan inte innehåller några dubbelbindningar. C=O i COOH-gruppen i molekylens vänstra ände beaktas inte.
Bemärk att närvaron av en ring också gör en molekyl omättad. Både raka och grenade pentaner har formeln C5H12, medan den ringformade molekylen cyklopentan har formeln C5H10:
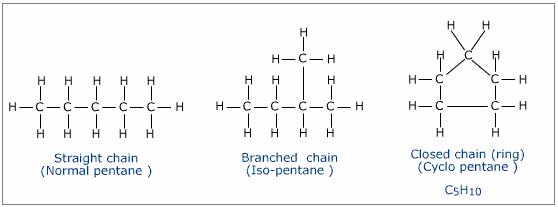
För att bilda ringformen måste man sammanfoga de två kolvätena i kedjans ändar, vilket innebär att man använder sig av två platser att binda där väteatomer skulle ha funnits. Raka och grenade kolväten är mättade, medan ringformade kolväten är omättade.
Förresten finns det inget som heter en övermättad molekyl. Om du ser det alternativet på ett prov är det en trickfråga.
Mättade, omättade och övermättade lösningar
Ordet mättad har en annan innebörd när det används för att beskriva lösningar.
För definitionerna nedan ska du komma ihåg att lösningsmedlet är den kemikalie som lösningsmedlet löser sig i. Det finns alltid mer lösningsmedel än lösta ämne.
Saltvatten är till exempel en lösning av natriumklorid (lösta ämnet) i vatten (lösningsmedlet).
Lösningsmedlet är vanligtvis en vätska, men det behöver det inte vara: luft är en lösning av syre, koldioxid och vattenånga (lösta ämnen) i kväve (lösningsmedlet). Stål är en lösning av kol (lösningen) i järn (lösningsmedlet).

Mättade lösningar innehåller så mycket lösningsmedel som lösningsmedlet kan hålla.
Döda havet är mättat: det innehåller allt salt och alla mineraler det kan hålla. Det innehåller så mycket salt att vattnet är tätare än människokroppen, och människor kan lätt flyta i det. I bilden till höger är de vita fasta bitarna de saltbitar som inte kan lösas upp eftersom vattnet redan är mättat.
Omättade lösningar innehåller mindre lösningsmedel än vad lösningsmedlet kan hålla.
Till skillnad från Döda havet är normalt havsvatten omättat. Även om det är riktigt salt innehåller det inte så mycket salt som det kan hålla.

Övermättade lösningar innehåller mer lösningsmedel än vad lösningsmedlet är tänkt att kunna hålla.
Du kan göra bergodis genom att koka sockervatten och sedan kyla ner det, vilket leder till övermättnad: sockret är tänkt att komma ur lösningen, men det kommer inte att göra det förrän du släpper en frökristall i det. (Avsaknaden av en frökristall är också en av anledningarna till att träd inte fryser på vintern.)
Videon nedan visar hur du kan göra din egen övermättade lösning av natriumacetat och använda den för att göra skulpturer av ”varm is”:
Du behöver också känna till nedanstående termer:
Diluenta lösningar innehåller mycket lite lösta ämne i förhållande till mängden lösningsmedel.
Koncentrerade lösningar innehåller mycket lösningsmedel i förhållande till mängden lösningsmedel.
Trickfrågor
En vanlig trickfråga går ut på att be dig göra den korrekta distinktionen mellan termerna mättad, omättad, övermättad, utspädd och koncentrerad.
En lösning kan vara både mättad och utspädd: När lösligheten är låg, till exempel när jodkristaller tillsätts i sjövatten för att döda bakterier, är lösningen mättad (full av lösta ämnen) och utspädd (inte särskilt koncentrerad) på samma gång. Det är bra att I2 är opolärt och inte särskilt vattenlösligt: om lösningen var koncentrerad skulle du dricka stora mängder av en elementär halogen!
Oceanvatten är å andra sidan både omättat och koncentrerat.
Döda havet är både mättat och koncentrerat.




