La hemoglobina y su medición
La función celular normal depende de un suministro continuo de oxígeno. A medida que el oxígeno se consume durante el metabolismo celular, se produce dióxido de carbono.
Una de las principales funciones de la sangre es el suministro de oxígeno (O2), presente en el aire inspirado, desde los pulmones a todas las células del cuerpo y el suministro de dióxido de carbono (CO2) desde las células a los pulmones, para su eliminación del cuerpo en el aire expirado.
Estas funciones vitales de transporte de gases dependen de la proteína hemoglobina contenida en los eritrocitos (glóbulos rojos). Cada uno de los 5 × 1010 eritrocitos normalmente presentes en 1 mL de sangre contiene alrededor de 280 millones de moléculas de hemoglobina.
1. ESTRUCTURA Y FUNCIÓN DE LA HEMOGLOBINA
La molécula de hemoglobina (Hb) es aproximadamente esférica y comprende dos pares de subunidades diferentes (FIGURA 1).
Cada una de las subunidades es una cadena polipeptídica plegada (la porción de globina) con un grupo hemo (derivado de la porfirina) unido.
En el centro de cada grupo hemo hay un único átomo de hierro en estado ferroso (Fe2+). Así, el hemo es una metaloporfirina, responsable por cierto del color rojo de la sangre.
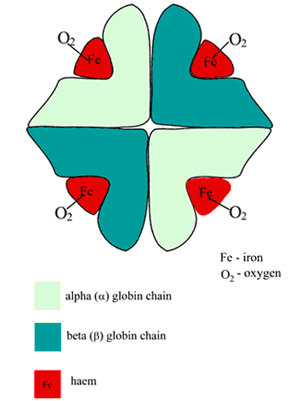
Figura 1: Esquema de la estructura de la hemoglobina oxigenada (HbA)
El sitio de unión del oxígeno de la Hb es el bolsillo del hemo presente en cada una de las cuatro cadenas polipeptídicas; un solo átomo de oxígeno forma un enlace reversible con el hierro ferroso en cada uno de estos sitios, por lo que una molécula de Hb une cuatro moléculas de oxígeno; el producto es la oxihemoglobina (O2Hb).
La función de suministro de oxígeno de la Hb, es decir, su capacidad para «recoger» el oxígeno en los pulmones y «liberarlo» en las células de los tejidos, es posible gracias a los diminutos cambios de conformación de la estructura cuaternaria que se producen en la molécula de hemoglobina y que alteran la afinidad del bolsillo del hemo por el oxígeno. La Hb tiene dos estados estructurales cuaternarios: el estado deoxi (baja afinidad por el oxígeno) y el estado oxi (alta afinidad por el oxígeno).
Una serie de factores ambientales determinan el estado cuaternario de la Hb y, por tanto, su afinidad relativa al oxígeno. El microambiente de los pulmones favorece el estado cuaternario oxi, por lo que la Hb tiene aquí una alta afinidad por el oxígeno.
Por el contrario, el microambiente de los tejidos induce el cambio conformacional en la estructura de la Hb que reduce su afinidad por el oxígeno, permitiendo así que el oxígeno se libere a las células de los tejidos.
1.1. HEMOGLOBINA Y ELIMINACIÓN DEL DIÓXIDO DE CARBONO
Una pequeña cantidad (hasta el 20 %) de CO2 se transporta desde los tejidos a los pulmones vagamente unido al aminoácido N-terminal de las cuatro unidades polipeptídicas de globina de la hemoglobina; el producto de esta combinación es la carbaminohemoglobina. Sin embargo, la mayor parte del CO2 se transporta como bicarbonato en el plasma sanguíneo.
La conversión eritrocitaria de CO2 en bicarbonato, necesaria para este modo de transporte de CO2, da lugar a la producción de iones de hidrógeno (H+). Estos iones de hidrógeno son amortiguados por la hemoglobina desoxigenada.
El papel de la hemoglobina en el transporte de oxígeno y dióxido de carbono se resume en las FIGURAS 2a y 2b.
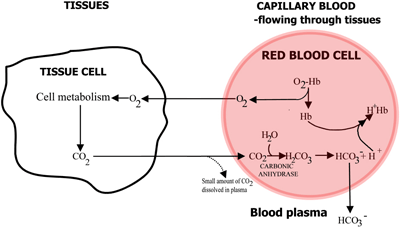
Figura 2a: TEJIDOS El O2 difunde de la sangre a los tejidos, el CO2 difunde de los tejidos a la sangre
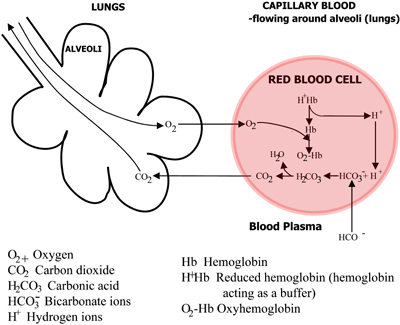
FIGURA 2b: PULMONES El CO2 difunde de la sangre a los pulmones, el O2 difunde de los pulmones a la sangre
En la sangre capilar que fluye por los tejidos el oxígeno se desprende de la hemoglobina y pasa a las células de los tejidos. El dióxido de carbono difunde fuera de las células tisulares hacia los eritrocitos, donde la enzima anhidrasa carbónica de los glóbulos rojos permite su reacción con el agua para formar ácido carbónico.
El ácido carbónico se disocia en bicarbonato (que pasa al plasma sanguíneo) e iones de hidrógeno, que se combinan con la hemoglobina ahora desoxigenada. La sangre fluye hacia los pulmones, y en los capilares de los alvéolos pulmonares las vías anteriores se invierten. El bicarbonato entra en los eritrocitos y aquí se combina con los iones de hidrógeno, liberados de la hemoglobina, para formar ácido carbónico.
Esto se disocia en dióxido de carbono y agua. El dióxido de carbono se difunde desde la sangre hacia los alvéolos de los pulmones y se elimina en el aire expirado. Mientras tanto, el oxígeno se difunde desde los alvéolos a la sangre capilar y se combina con la hemoglobina.
1.2. HEMOGLOBINA QUE NO PUEDE UNIR OXÍGENO
Aunque normalmente sólo están presentes en cantidades mínimas, existen tres especies de hemoglobina: la metahemoglobina (MetHb o Hi), la sulfhemoglobina (SHb) y la carboxihemoglobina (COHb) que no pueden unir oxígeno.
Por lo tanto, son funcionalmente deficientes, y el aumento de las cantidades de cualquiera de estas especies de hemoglobina, normalmente el resultado de la exposición a fármacos específicos o toxinas ambientales, puede comprometer seriamente el suministro de oxígeno.
En la referencia se proporciona una descripción completa de la estructura y la función de la hemoglobina.
ctHb, la concentración total de hemoglobina se define normalmente como la suma de la hemoglobina oxigenada, la hemoglobina desoxigenada, la carboxihemoglobina y la metahemoglobina.
Utilidad clínica de la medición de la ctHb
La principal razón para medir la ctHb es la detección de la anemia y la evaluación de su gravedad.
La anemia puede definirse como una reducción de la capacidad de transporte de oxígeno de la sangre debido a una reducción del número de eritrocitos y/o a una reducción de la ctHb, de modo que la anemia se establece si la ctHb está por debajo del límite inferior del rango de referencia (normal) (TABLA I). Cuanto más baja es la ctHb, más grave es la anemia.
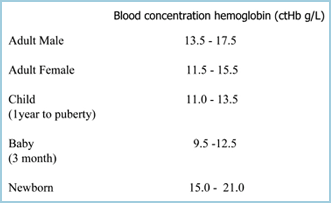
Tabla I: rangos de referencia de la ctHb (Ref 2)
La anemia no es una entidad de la enfermedad, sino una consecuencia o signo de la misma. La razón por la que la ctHb es un análisis de sangre tan frecuentemente solicitado es que la anemia es una característica de una serie de patologías, muchas de las cuales son relativamente comunes (Tabla II).
Los síntomas comunes, la mayoría de los cuales son inespecíficos, incluyen: palidez, cansancio y letargo, dificultad para respirar -especialmente con el esfuerzo-, mareos y desmayos, cefaleas, estreñimiento y aumento del pulso, palpitaciones, taquicardia.

Tabla II: Algunas de las condiciones clínicas asociadas a la anemia
La ausencia de estos síntomas no excluye la anemia; muchos individuos ligeramente anémicos permanecen asintomáticos, particularmente si la anemia se ha desarrollado lentamente.
2.2. POLICITEMIA
Mientras que la anemia se caracteriza por una reducción de la ctHb, una ctHb elevada indica policitemia. La policitemia surge como respuesta a cualquier condición fisiológica o patológica en la que la sangre contiene menos oxígeno de lo normal (hipoxemia).
La respuesta del organismo a la hipoxemia incluye un aumento de la producción de eritrocitos para incrementar el suministro de oxígeno y, como consecuencia, la ctHb se eleva. Esta llamada policitemia secundaria forma parte de la adaptación fisiológica a la altitud y puede ser una característica de la enfermedad pulmonar crónica.
La policitemia primaria es una enfermedad maligna de la médula ósea mucho menos común llamada policitemia vera, que se caracteriza por la producción incontrolada de todas las células sanguíneas, incluidos los eritrocitos. La policitemia, ya sea secundaria o primaria, es generalmente mucho menos común que la anemia.
3.1. PERSPECTIVA HISTÓRICA
La primera prueba clínica de medición de la Hb ideada hace más de un siglo consistía en añadir gotas de agua destilada a un volumen de sangre medido hasta que su color coincidiera con el de un estándar artificial coloreado.
Una modificación posterior implicaba saturar primero la sangre con gas de carbón (monóxido de carbono) para convertir la hemoglobina en la más estable carboxihemoglobina. La hemoglobinometría moderna data de la década de 1950, tras el desarrollo de la espectrofotometría y el método de la hemiglobincianida (cinametohemoglobina).
Luego se adaptó este método y otros para su uso en analizadores de hematología automatizados. En las últimas dos décadas los avances se han centrado en el desarrollo de métodos que permiten realizar pruebas de hemoglobina en el punto de atención (POCT).
Esta sección aborda en primer lugar la consideración de algunos de los métodos utilizados actualmente en el laboratorio y, a continuación, los métodos POCT utilizados fuera del laboratorio.
3.2. HEMIGLOBINCIÁNIDO – UN MÉTODO ESPECTROFOTOMÉTRICO
Casi 40 años después de haber sido adoptado por primera vez como método de referencia para la medición de la hemoglobina por el Comité Internacional de Normalización en Hematología (ICSH), la prueba del hemiglobincianuro (HiCN) sigue siendo el método recomendado por el ICSH con el que se juzgan y normalizan todos los nuevos métodos de ctHb.
La consideración detallada que sigue refleja su continua importancia tanto como método de referencia como de laboratorio de rutina.
3.2.1. Principio de la prueba
La sangre se diluye en una solución que contiene ferricianuro de potasio y cianuro de potasio. El ferricianuro de potasio oxida el hierro del hemo al estado férrico para formar metahemoglobina, que es convertida en hemiglobincianuro (HiCN) por el cianuro de potasio.
El HiCN es un producto de color estable, que en solución tiene un máximo de absorbancia a 540 nm y obedece estrictamente la ley de Beer-Lambert. La absorbencia de la muestra diluida a 540 nm se compara con la absorbencia a la misma longitud de onda de una solución estándar de HiCN cuya concentración de hemoglobina equivalente se conoce.
La mayoría de los derivados de la hemoglobina (oxihemoglobina, metahemoglobina y carboxihemoglobina, pero no la sulfhemoglobina) se convierten en HiCN y, por tanto, se miden con este método.
3.2.1.1. Diluyente del reactivo (solución de Drabkin modificada)
| Ferricianuro de potasio (K3Fe(CN)6) | 200 mg |
| Cianuro de potasio (KCN) | 50 mg |
| Fosfato potásico de dihidrógeno (KH2 PO4) | 140 mg |
| Detergente nodetergente iónico (e.p. ej. Triton X-100) | 1 mL |
| Lo anterior diluido a 1000 mL en agua destilada |
3.2.1.2. Método manual
Se añaden 25 µl de sangre a 5,0 mL de reactivo, se mezclan y se dejan durante 3 minutos. La absorbencia se lee a 540 nm contra un blanco de reactivo. La absorbencia del estándar HiCN se mide de la misma manera.
3.2.1.3. Estándar de HiCN del ICSH
La mayor ventaja de este método es que existe una solución estándar de HiCN fabricada y a la que se le asigna un valor de concentración según criterios muy precisos establecidos y revisados periódicamente por el Consejo Internacional de Normalización en Hematología (ICSH) .
Esta solución estándar internacional es el principal calibrador de las soluciones estándar comerciales utilizadas en los laboratorios clínicos de todo el mundo. Por lo tanto, todos los que utilizan la estandarización HiCN están utilizando efectivamente el mismo estándar, cuyo valor ha sido escrupulosamente validado.
3.2.1.4. Interferencia
La perturbación debida a las proteínas, los lípidos y la materia celular es un problema potencial en la estimación espectrofotométrica de cualquier constituyente de la sangre, incluida la hemoglobina.
La gran dilución (1:251) de la muestra elimina en gran medida el problema, pero pueden producirse resultados de ctHb falsamente elevados en pacientes cuya concentración de proteínas plasmáticas sea especialmente alta .
Las muestras muy lipémicas y las que contienen un número muy elevado de glóbulos blancos (leucocitos) también pueden elevar artificialmente la ctHb por un mecanismo similar.
3.2.1.5. Ventajas del HiCN
- Estándar internacional – preciso
- Fácilmente adaptado a los analizadores de hematología automatizados; por lo tanto, reproducible (baja SD y CV – dentro del CV del lote típicamente
- Bien establecido e investigado a fondo – recomendado por el ICSH
- Reactivo barato
3.2.1.6. Desventajas del HiCN
- El método manual requiere un pipeteo preciso y un espectrofotómetro
- El reactivo (cianuro) es peligroso
- Lo anterior limita su uso fuera del laboratorio
- Sujeto a la interferencia de los lípidos elevados, las proteínas plasmáticas y el número de leucocitos
- No distingue los derivados de la hemoglobina que no tienen capacidad de transporte de oxígeno (MetHb, COHb, SHb). Por lo tanto, puede sobrestimar la capacidad de transporte de oxígeno de la sangre si están presentes en cantidades anormales (más que trazas).
3.3. MÉTODOS DE LABORATORIO ALTERNATIVOS (SIN CÁNIDOS)
El laurilsulfato sódico (SLS) es un tensioactivo que lisa los eritrocitos y forma rápidamente un complejo con la hemoglobina liberada. El producto SLS-MetHb es estable durante unas horas y tiene un espectro característico con una absorbencia máxima a 539 nm .
El complejo obedece a la ley de Beer-Lambert, por lo que existe una correlación lineal precisa entre la concentración de Hb y la absorbancia del SLS-MetHb.
El método consiste simplemente en mezclar 25 µl de sangre con 5,0 mL de una solución de 2,08 mmol/L de SLS (tamponada a un pH de 7,2), y leer la absorbancia a 539 nm. Se ha demostrado que los resultados de ctHb por el método SLS-Hb se correlacionan muy estrechamente (r = 0,998) con el método HiCN de referencia .
El método ha sido adaptado para los analizadores de hematología automatizados y es tan fiable en términos de exactitud y precisión como los métodos HiCN automatizados . Una ventaja importante es que el reactivo no es tóxico. También es menos propenso a la interferencia por la lipemia y el aumento de la concentración de leucocitos .
La inestabilidad a largo plazo de la SDS-MetHb impide su uso como estándar, por lo que el método debe calibrarse con sangre cuya ctHb se haya determinado mediante el método HiCN de referencia.
3.3.2. Método de la azida-metemoglobina
Este método se basa en la conversión de la hemoglobina en un producto estable coloreado de azida-metemoglobina que tiene un espectro de absorbancia casi idéntico al del HiCN .
El reactivo utilizado en este método es muy similar al utilizado en el método de referencia HiCN con la sustitución de la azida de sodio por el cianuro de potasio, más tóxico. Al igual que en el método HiCN, la hemoglobina se convierte en metahemoglobina mediante el ferricianuro de potasio; a continuación, la azida forma un complejo con la metahemoglobina.
Los resultados de la Hb por este método son comparables a los obtenidos por el método HiCN de referencia; se trata de un método manual alternativo aceptable. Sin embargo, el potencial explosivo de la azida sódica impide su uso en analizadores de hematología automatizados. La reacción azida-MetHb ha sido adaptada para los hemoglobinómetros POCT.
3.4. Los métodos POCT considerados aquí son:
- Hemoglobinómetros portátiles
- CO-oximetría – un método utilizado en los analizadores de gases sanguíneos POCT
- Escala de color de la OMS
3.4.1. Hemoglobinómetros portátiles Hemoglobinómetros portátiles
Los hemoglobinómetros portátiles como el HemoCue-B permiten una determinación precisa de la hemoglobina a pie de cama. Son esencialmente fotómetros que permiten medir la intensidad del color de las soluciones.
La microcubeta desechable en la que se realizan estas mediciones actúa también como recipiente de reacción. Los reactivos necesarios tanto para la liberación de Hb de los eritrocitos como para la conversión de Hb en un producto coloreado estable están presentes en forma seca en las paredes de la cubeta.
Todo lo que se requiere es la introducción de una pequeña muestra (normalmente 10 µl) de sangre capilar, venosa o arterial en la microcubeta y la inserción de la microcubeta en el instrumento.
El instrumento viene precalibrado de fábrica utilizando el estándar HiCN, y la absorbancia de la solución de prueba se convierte automáticamente en ctHb. El resultado se muestra en menos de un minuto.
3.4.1.1. Las ventajas de los hemoglobinómetros modernos incluyen
- Portabilidad
- Funciona con batería o con la red eléctrica, puede utilizarse en cualquier lugar
- Pequeño volumen de muestra (10 µL) obtenido por punción del dedo
- Rápido (resultado en 60 segundos)
- Facilidad de uso – no hay que pipetear
- Mínima formación requerida por personal ajeno al laboratorio
- Estandarizado frente a HiCN – resultados comparables a los obtenidos en laboratorio
- Corrección por turbidez. En este aspecto los hemoglobinómetros portátiles son superiores a la mayoría de los métodos de ctHb .
Esta tecnología ha sido ampliamente evaluada en una serie de entornos y la mayoría de los estudios han confirmado una exactitud y precisión aceptables en comparación con los métodos de laboratorio.
3.4.1.2. Desventajas
Sin embargo, algunos estudios han planteado la preocupación de que en manos de personal ajeno al laboratorio los resultados puedan ser menos satisfactorios. A pesar de su sencillez de manejo, estos instrumentos no son inmunes a los errores del operador, y es esencial una formación eficaz.
Hay pruebas que sugieren que los resultados derivados de muestras capilares (pinchazos en el dedo) son menos precisos que los derivados de muestras capilares o venosas bien mezcladas y recogidas en frascos de EDTA.
3.4.2. CO-oximetría
Un CO-oxímetro es un espectrofotómetro especializado, cuyo nombre refleja la aplicación original, que consistía en medir COHb y MetHb.
Muchos analizadores de gases sanguíneos modernos llevan incorporado un CO-oxímetro, lo que permite la estimación simultánea de la ctHb durante el análisis de los gases sanguíneos.
La medición de la ctHb mediante CO-oximetría se basa en el hecho de que la hemoglobina y todos sus derivados son proteínas coloreadas que absorben la luz a longitudes de onda específicas y, por tanto, tienen un espectro de absorbancia característico (FIGURA 3).
La ley de Beer-Lambert dicta que la absorbancia de un solo compuesto es proporcional a la concentración de ese compuesto. Si se conoce la característica espectral de cada sustancia absorbente en una solución, las lecturas de absorbancia de la solución a múltiples longitudes de onda pueden utilizarse para calcular la concentración de cada sustancia absorbente.
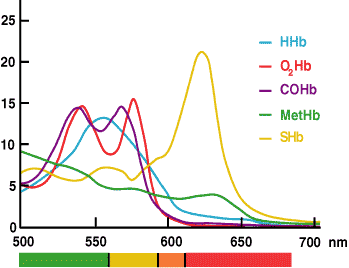
FIGURA 3.
En el CO-oxímetro las mediciones de absorbencia de una muestra de sangre hemolizada en múltiples longitudes de onda a través del rango en que las especies de hemoglobina absorben la luz (520-620 nm) son utilizadas por el software instalado para calcular la concentración de cada uno de los derivados de la hemoglobina (HHb, O2Hb, MetHb y COHb). ctHb es la suma calculada de estos derivados.
Todo lo que se requiere del operador es la inyección de una muestra de sangre arterial bien mezclada en el analizador de gases en sangre/CO-oxímetro.
La muestra, o una parte de ella, se bombea automáticamente a la cubeta de medición del CO-oxímetro, donde -por acción química o física- los eritrocitos se lisan para liberar hemoglobina, que se explora espectroscópicamente como se ha descrito anteriormente.
Los resultados se muestran junto con los resultados de los gases sanguíneos en uno o dos minutos.
Varios estudios han confirmado que los resultados de la ctHb obtenidos por CO-oximetría no son clínicamente diferentes de los derivados de los métodos de laboratorio de referencia. La CO-oximetría proporciona un medio aceptable de estimación urgente de la ctHb en un entorno de cuidados críticos.
3.4.2.1. Las ventajas particulares de la ctHb por CO-oximetría incluyen
- Velocidad de análisis
- Facilidad de análisis
- Pequeño volumen de muestra
- Sin coste de capital o de consumibles más allá del requerido para el análisis de gases en sangre
- Parámetros adicionales (MetHb, COHb, O2Hb) medidos
- No se ve afectado por un alto recuento de glóbulos blancos
3.4.3. Escala de color de la hemoglobina de la OMS (HCS)
Desarrollada para la Organización Mundial de la Salud (OMS), esta prueba de baja tecnología tiene una aplicación limitada en los países desarrollados, pero tiene una enorme importancia para los países económicamente desfavorecidos del mundo en desarrollo, donde la anemia es más frecuente.
En zonas en las que no hay instalaciones de laboratorio ni recursos suficientes para financiar hemoglobinómetros POCT más sofisticados, es prácticamente el único medio para determinar la ctHb.
La prueba HCS se basa en el sencillo principio de que el color de la sangre es una función de la ctHb. Se absorbe una gota de sangre en un papel y se compara su color con una tabla de seis tonos de rojo, cada uno de los cuales representa una ctHb equivalente: el más claro 40 g/L y el más oscuro 140 g/L. Aunque en principio es muy sencillo, en su desarrollo se ha utilizado una considerable cantidad de investigación y tecnología para garantizar la máxima exactitud y precisión posibles .
Por ejemplo, la elección final del papel para la matriz de las tiras reactivas se basó en extensas pruebas con diferentes papeles, y se empleó el análisis espectrofotométrico de la sangre y de las mezclas de colorantes para llegar a la mayor coincidencia posible entre el color de la carta y el color de la sangre en cada ctHb de referencia.
3.4.3.1. Ventajas de la prueba HCS Ventajas de la prueba HCS
- Es fácil de usar – sólo requiere 30 minutos de formación
- No requiere equipo ni energía
- Es rápida – resultado en 1 minuto
- Sólo requiere una muestra de pinchazo en el dedo (capilar)
- Es muy barata (alrededor de 0,12 USD por prueba)
3.4.3.2. Desventajas de la prueba HCS
Los resultados fiables dependen del cumplimiento estricto de las instrucciones de la prueba .
Los errores más comunes son:
- Sangre inadecuada o excesiva en la tira reactiva
- Lectura del resultado demasiado tarde (más de 2 minutos) o demasiado pronto (menos de 30 sceonds)
- Lectura del resultado en condiciones de poca iluminación
La prueba HSC tiene claramente limitaciones inherentes . En el mejor de los casos puede determinar que la ctHb de una muestra de paciente se encuentra dentro de uno de los seis rangos de concentración: 30-50 g/L, 50-70 g/L, 70-90 g/L, 90-110 g/L, 110-130 g/L o 130-150 g/L. Aun así, esto es teóricamente suficiente para identificar a todos los pacientes, excepto a los más anémicos, y dar una indicación de la gravedad.
Un primer estudio demostró la capacidad de la prueba para identificar la anemia (definida como ctHb
SUMARIO
ctHb es uno de los dos parámetros que se utilizan habitualmente para evaluar la capacidad de transporte de oxígeno de la sangre y, por lo tanto, establecer un diagnóstico de anemia y policitemia.
La prueba alternativa, denominada hematocrito (Hct) o volumen celular empaquetado (PCV), fue objeto de un artículo complementario anterior, en el que se analizó la relación entre la ctHb y la Hct . Este artículo se centra en la medición de la ctHb.
Se han ideado numerosos métodos, la mayoría basados en la medición del color de la hemoglobina o de un derivado de la misma. Para esta breve revisión ha sido inevitable ser selectivo. Los métodos elegidos para la discusión se encuentran entre los más utilizados en la actualidad.
Al hacer la selección se ha intentado transmitir la gama de tecnologías que se emplean actualmente y cómo se aplican para satisfacer la demanda clínica de ctHb en entornos que van desde las zonas empobrecidas del mundo en desarrollo, donde la atención médica apenas tiene asidero, hasta el mundo de alta tecnología de la unidad moderna de cuidados intensivos.




