CNIO, új lépések az időskori tüdőfibrózis elleni jövőbeli terápiához
A Spanyol Nemzeti Rákkutató Központ (CNIO) Telomerek és Telomeráz Csoportja hatékony terápiát mutatott ki az öregedés okozta fibrózisban szenvedő egereknél, miután ugyanezt a gyógymódot kifejlesztette a genetikai hiba miatt fibrózisban szenvedő egereknél. A Journal of Cell Biology című folyóiratban közzétett tanulmány olyan génterápiát fejleszt ki, amely aktiválja a szervezet telomeráz termelését.
A diopátiás tüdőfibrózis egy kezeletlen és potenciálisan halálos betegség, amely bizonyos mutációkkal és az öregedéssel is összefügg.
A telomeráz a kromoszómák végeinek javításáért felelős enzim, ahol a telomerek találhatók. A terápia rendkívül hatékony volt az állatoknál, és nem észleltek mellékhatásokat. Ezt Maria Blaso, a tanulmány vezetője magyarázta.
“Ha az emberre gondolunk, eredményünk arra utal, hogy olyan terápiát hozhatunk létre, amely bármely betegnél képes megelőzni az öregedéssel járó tüdőfibrózis kialakulását” – mondja Blasco.
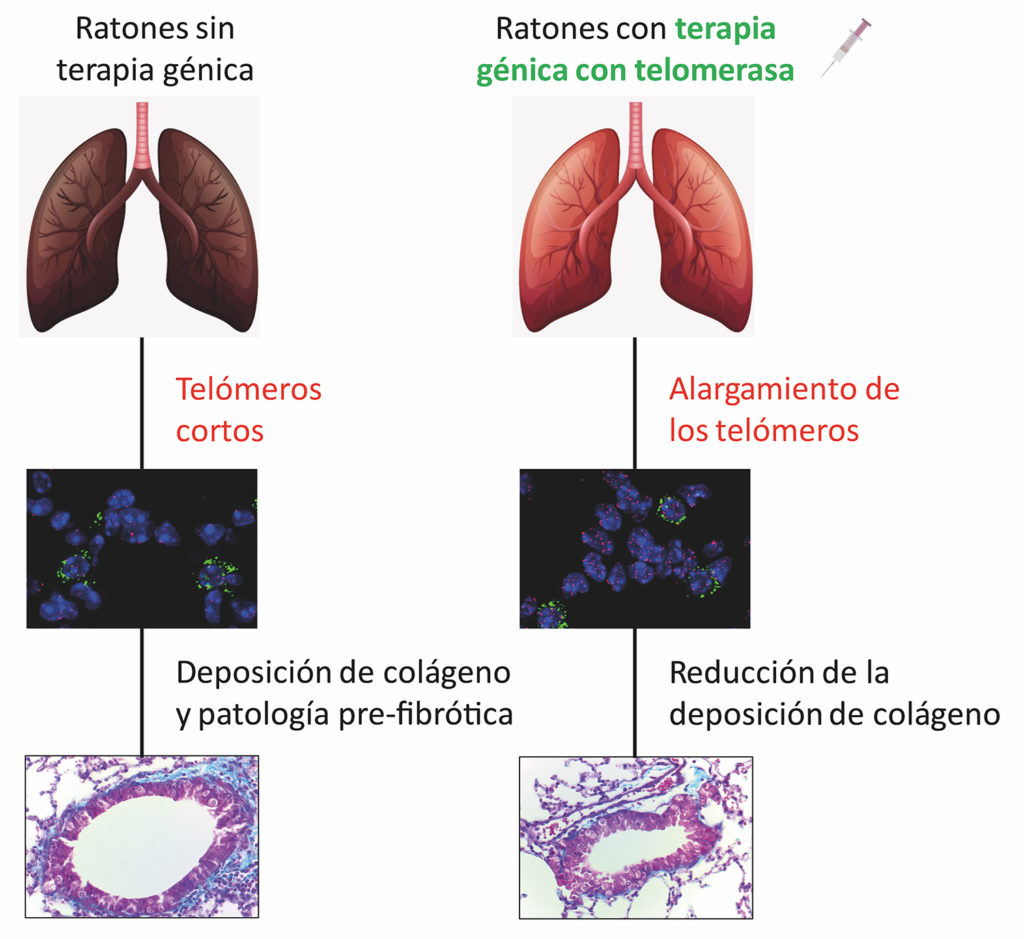
Telomer diszfunkció a fibrózis eredeténél
A tüdőfibrózis Spanyolországban mintegy 8000 embert érint. Ebben a betegségben a tüdőszövet hegesedik és merevvé válik, ami a légzési kapacitás fokozatos csökkenéséhez vezet.
Az okát a genetika és a környezet kombinációjának tulajdonítják: a környezeti mérgek fontos szerepet játszanak, de ahhoz, hogy a betegség megnyilvánuljon, vagy genetikai oknak, vagy az idő múlásával járó öregedésnek is kell lennie.
A CNIO csoport már korábbi tanulmányokban kimutatta, hogy ez a genetikai ok a telomerek hibás működésében rejlik. A telomerek olyan struktúrák, amelyek a sapkákhoz hasonlóan védik a minden sejtben jelen lévő kromoszómák integritását.
2015-ben létrehozták a tüdőfibrózis állati modelljét, egy olyan egeret, amelyből hiányzik a telomeráz gén. Ezekben az állatokban a tüdőszövet regenerációjáért felelős sejtek, az úgynevezett II. típusú alveoláris pneumociták végül elpusztulnak a telomerek diszfunkciója miatt. Az egérben ennek következtében agresszív fibrózis alakul ki, mivel a tüdő hámja nem tud rendszeresen megújulni. Ez az időszakos regeneráció tartja a szöveteket egészségesen, a környezeti toxinok által okozott károsodástól mentesen.
Az öregedéssel összefüggő fibrózis
Ez a telomeráz gén nélküli állatmodell jól reprodukálja azt, ami azoknál a betegeknél történik, akiknél a fibrózis a telomereket érintő mutációk miatt alakul ki. De ezek az emberek kisebbségben vannak. A betegek túlnyomó többségénél semmi sem utal konkrét mutációra, de van egy közös tényező: az előrehaladott életkor.

A telomerek pusztán az öregedés folyamatával is elveszíthetik funkciójukat. Annak tanulmányozása, hogy ez hogyan történik, egy olyan terület, amelyet Blasco csoportja vezet nemzetközi szinten.
A telomerek a kromoszómák végén lévő fehérjekupakok, amelyek minden egyes sejtosztódáskor egy kicsit rövidebbek lesznek. Ebből adódóan a szervezet élete során sok sejtosztódás után elérkezik egy pont, amikor a sejtek olyan rövidek lesznek, hogy elveszítik a kromoszómák védelmét. A sejt ezt hibaként értelmezi, és leállítja az osztódást, így a szövet nem regenerálódik.
A most közzétett munkájukban a kutatók kimutatták, hogy ez az életkorral összefüggő telomer-diszfunkció valóban előfordul a tüdőszövet regenerációs sejtjeiben, a II-es típusú tüdősejtekben. Így megtalálják az öregedés és a tüdőfibrózis közötti, a klinikumban oly egyértelmű kapcsolat molekuláris okát.
A tüdő kenőanyagának elvesztése
A szerzők szerint “az új munka egyik eredménye, hogy nagyon részletesen leírja az öregedésnek a tüdőszövetre gyakorolt hatását”. “Az egyik közvetlenül abból ered, hogy a II-es típusú tüdősejtek abbahagyják a munkájukat” – mondja Sergio Piñeiro, a tanulmány első szerzője.
A szövetek regenerálása mellett ezek a sejtek a tüdő mechanikai munkáját megkönnyítő folyadékot, az úgynevezett pulmonális surfactantot termelnek és bocsátanak ki.
“A tüdőszövetnek minden egyes légzéskor ki kell nyílnia, percenként hat-tíz alkalommal, ami fizikai szempontból nagy erőfeszítés” – magyarázta Jesús Pérez-Gil, a madridi Complutense Egyetem szakértője.
Gil, aki részt vett a tanulmányban, és akinek csapata szakértője ezen a területen, rámutatott, hogy “a tüdő szurfaktánsa elengedhetetlen a szövetek kenéséhez, hogy azok minimális erőfeszítéssel nyithatók és zárhatók legyenek, és rugalmasak maradjanak”.
“Ha a II-es típusú pneumociták nem regenerálódnak, akkor a surfactant sem, és ez hozzájárul ahhoz, hogy a tüdő fokozatosan merevvé és fibrózissá váljon”
Madridi Complutense Egyetem, Jesús Pérez-Gil
A tanulmányban “nagyon egyértelmű kapcsolatot figyeltünk meg a II-es típusú pneumociták telomer állapota, a tüdő surfactant termelése és a fibrózis kialakulása között állatokban” – teszi hozzá Pérez-Gil. “Ebben az együttműködésben kombináltan foglalkozunk a molekuláris szintű, a telomerekre gyakorolt hatásokkal; a sejtekben és szövetekben bekövetkező biológiai és fizikai változásokkal; valamint az állat egészségére, az egész szervezetre gyakorolt következményekkel.”
A terápia mindenféle fibrózisra
A CNIO csoportja 2018-ban olyan génterápiát fejlesztett ki, amely képes gyógyítani a telomeráz gén nélkül kialakult fibrózist az egereknél. A kezelés alapja ennek a genetikai változásnak a visszafordítása, a telomeráz szintézis átmeneti aktiválása az egerekben.

Egereknek intravénásan olyan vírust adnak be, amelynek egyetlen funkciója a telomeráz gén hordozása a szövetekbe. Hatása rövid ideig tart, de elegendő ahhoz, hogy a II. típusú tüdősejtek hosszú telomereket növesszenek és a tüdőszövet regenerálódjon.
Most ugyanezt a terápiát alkalmazták egereken, amelyek egyszerűen öregednek. És működik is. “A telomeráz-aktiváló génterápiával történő kezelés minden egérnél megakadályozta a fibrózis kialakulását, beleértve azokat is, amelyeknél nem volt genetikai elváltozás, de fiziológiailag öregedtek” – magyarázza Blasco.
Ez a tüdőfibrózis gyógyításának lehetőségét a fibrózis szinte minden esetére kiterjeszti, ahogy a kutatók cikkükben megállapítják: “Ezek az eredmények segítenek megmagyarázni az idiopátiás tüdőfibrózis elleni jövőbeli terápiás stratégiák fontosságát.
A tanulmányt a spanyol Tudományos, Innovációs és Egyetemi Minisztérium, a Carlos III Egészségügyi Intézet, a madridi közösség, a Botín Alapítvány és a Banco Santander finanszírozta a Santander Egyetemeken és a World Cancer Research-en keresztül.
A tanulmányt a spanyol Tudományos, Innovációs és Egyetemi Minisztérium, a Carlos III Egészségügyi Intézet, a madridi közösség, a Botín Alapítvány és a Banco Santander finanszírozta a Santander Egyetemeken és a World Cancer Research-en keresztül.




