Nátrium-klorid
A só ismert háztartási felhasználása mellett a mintegy 250 millió tonna/év termelés (2008-as adat) dominánsabb felhasználási területei a vegyipar és a jégtelenítés.
Vegyipari termelésSzerkesztés
A sót közvetlenül vagy közvetve számos vegyszer előállításához használják, amelyek a világ termelésének nagy részét felemésztik.
KlóralkáliiparSzerkesztés
Ez a klóralkáli-folyamat kiindulópontja, a klór és nátrium-hidroxid előállítására szolgáló ipari folyamat, a kémiai egyenlet szerint
2 NaCl + 2 H2O → Cl2 + H2 + 2 NaOH
Az elektrolízist vagy higanycellában, vagy membráncellában, vagy membráncellában végzik. Ezek mindegyike más-más módszert alkalmaz a klór és a nátrium-hidroxid elválasztására. Az elektrolízis magas energiafogyasztása miatt más technológiák is fejlesztés alatt állnak, így a hatékonyság kis mértékű javítása nagy gazdasági megtérüléssel járhat. A klór néhány alkalmazási területe a PVC, a fertőtlenítőszerek és az oldószerek. A nátrium-hidroxid lehetővé teszi a papírt, szappant és alumíniumot előállító iparágak működését.
Szóda-mészkőiparSzerkesztés
A nátrium-kloridot a Solvay-eljárásban nátrium-karbonát és kalcium-klorid előállítására használják. A nátrium-karbonátot viszont üveg, nátrium-hidrogénkarbonát és színezékek, valamint számtalan más vegyi anyag előállítására használják. A Mannheim-eljárásban és a Hargreaves-eljárásban a nátrium-kloridot nátrium-szulfát és sósav előállítására használják.
SzabványSzerkesztés
A nátrium-kloridnak nemzetközi szabványa van, amelyet az ASTM International hozott létre. A szabvány neve ASTM E534-13, és a nátrium-klorid kémiai elemzésének szabványos vizsgálati módszereit tartalmazza. Ezek a felsorolt módszerek eljárásokat biztosítanak a nátrium-klorid elemzésére annak megállapítására, hogy az alkalmas-e a tervezett felhasználásra és alkalmazásra.
Különböző ipari felhasználásokSzerkesztés
A nátrium-kloridot nagymértékben használják, így még viszonylag kisebb alkalmazások is hatalmas mennyiségeket fogyaszthatnak. Az olaj- és gázkutatásban a só a kútfúrásnál a fúrófolyadékok fontos összetevője. A fúrófolyadék flokkulálására és sűrűségének növelésére használják, hogy leküzdjék a magas kút alatti gáznyomást. Amikor a fúrógép sós formációba ütközik, sót adnak a fúrófolyadékhoz az oldat telítése érdekében, hogy minimalizálják a sórétegen belüli oldódást. Sót használnak a cementált burkolatokban a beton száradásának fokozására is.
A textil- és festékgyártásban sót használnak sóoldatos öblítőként a szerves szennyeződések leválasztására, a festékkiválások “kisózásának” elősegítésére, valamint koncentrált festékekkel való keverésre azok standardizálása érdekében. Egyik fő szerepe a pozitív iontöltés biztosítása, hogy elősegítse a színezékek negatív töltésű ionjainak felszívódását.
Az alumínium, a berillium, a réz, az acél és a vanádium feldolgozásánál is használják. A cellulóz- és papíriparban a sót a fapép fehérítésére használják. Ezenkívül nátrium-klorát előállítására is használják, amelyet kénsavval és vízzel együtt adnak hozzá a klór-dioxid, egy kiváló oxigénalapú fehérítő vegyszer előállításához. A klór-dioxid-eljárás, amely az első világháború után Németországból származik, egyre népszerűbbé válik a klórozott fehérítő vegyületek csökkentésére vagy megszüntetésére irányuló környezetvédelmi nyomás miatt. A cserzésben és a bőrkezelésben sót adnak az állati bőrökhöz, hogy gátolják a mikrobiális tevékenységet a bőrök alján, és hogy a nedvességet visszacsalogassák a bőrbe.
A gumigyártásban a sót buna, neoprén és fehér gumitípusok előállításához használják. Sós sót és kénsavat használnak a klórozott butadiénből készült emulgeált latex koagulálásához.
Sót adnak a talaj rögzítéséhez és az autópályák alapjának szilárdságához is. A só úgy hat, hogy minimalizálja a nedvesség és a forgalmi terhelés változásai által az altalajban okozott elmozdulások hatásait.
A nátrium-kloridot néha olcsó és biztonságos nedvszívószerként használják, mivel higroszkópos tulajdonságai miatt a sózás a múltban az élelmiszerek tartósításának hatékony módszerévé vált; a só ozmotikus nyomás révén vizet von ki a baktériumokból, megakadályozva azok szaporodását, ami az élelmiszerek romlásának egyik fő forrása. Bár léteznek hatékonyabb nedvszívószerek, kevés olyan van, amelyet az ember biztonságosan lenyelhet.
VízlágyításSzerkesztés
A kemény víz kalcium- és magnéziumionokat tartalmaz, amelyek zavarják a szappan hatását, és hozzájárulnak a vízkő vagy lúgos ásványi lerakódásokból álló film felhalmozódásához a háztartási és ipari berendezéseken és csöveken. A kereskedelmi és lakossági vízlágyító berendezések ioncserélő gyantákat használnak a keménységet okozó zavaró ionok eltávolítására. Ezeket a gyantákat nátrium-klorid felhasználásával állítják elő és regenerálják.
Útmenti sóSzerkesztés
A só másik fő felhasználási területe az utak jégtelenítése és jégmentesítés, mind a szórótartályokban, mind a téli szolgálat járműveivel történő szórás során. A hóesést megelőzve az utakat optimális esetben “jégtelenítik” sóoldattal (só koncentrált oldata vízben), amely megakadályozza a hójég és az útfelület közötti kötődést. Ezzel az eljárással elkerülhető a hóesés utáni nagymértékű sóhasználat. A jégtelenítéshez sóoldat és só keverékét használják, néha további anyagokkal, például kalcium-kloriddal és/vagy magnézium-kloriddal. A só vagy a sóoldat használata -10 °C alatt hatástalanná válik.

A jégtelenítésre használt só az Egyesült Királyságban túlnyomórészt egyetlen bányából származik, a cheshire-i Winsfordból. A forgalmazás előtt <100 ppm nátrium-ferrocianiddal keverik össze, mint csomósodásgátló anyaggal, amely lehetővé teszi, hogy a kősó szabadon kifolyjon a sószóró járművekből, annak ellenére, hogy a felhasználás előtt felhalmozzák. Az utóbbi években ezt az adalékanyagot az étkezési sóhoz is használják. Az útszóró sóban korábban más adalékanyagokat is használtak a teljes költség csökkentése érdekében. Az Egyesült Államokban például a cukorrépa-feldolgozásból származó melléktermékként keletkező szénhidrátoldatot kevertek kősóhoz, és az 40%-kal jobban tapadt az útfelülethez, mint a laza kősó önmagában. Mivel tovább maradt az úton, a kezelést nem kellett többször megismételni, így időt és pénzt takarítottak meg.
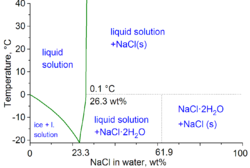
Fizikai-kémiai szaknyelven szólva a víz-só keverék minimális fagyáspontja -21,12 °C (-6,02 °F) 23,31 tömegszázalék só esetén. E koncentráció közelében azonban olyan lassú a fagyás, hogy az eutektikus pont -22,4 °C (-8,3 °F) körülbelül 25 m% só esetén érhető el.
Környezeti hatásokSzerkesztés
A só az édesvizekbe kerül, és károsíthatja a vízi növényeket és állatokat az ozmoregulációs képességük megzavarásával. A só mindenütt jelenléte problémát jelent minden part menti bevonat alkalmazásánál, mivel a csapdába esett sók nagy tapadási problémákat okoznak. A haditengerészeti hatóságok és a hajóépítők az építkezés során ellenőrzik a felületek sókoncentrációját. A felületek maximális sókoncentrációja a hatóságtól és az alkalmazástól függ. Leggyakrabban az IMO-előírást alkalmazzák, amely a nátrium-kloridban mért oldható sók szintjét legfeljebb 50 mg/m2 -ben határozza meg. Ezeket a méréseket Bresle-teszttel végzik. A sósodás (növekvő sótartalom, más néven édesvízi sósodás szindróma) és az azt követő fokozott fémkioldódás folyamatos probléma Észak-Amerikában és az európai édesvizekben.
Az autópályák jégtelenítése során a sót összefüggésbe hozták a hídpályák, a gépjárművek, a betonvasak és drótok, valamint az útépítés során használt védtelen acélszerkezetek korróziójával. A felszíni lefolyás, a járművek permetezése és a szélfúvások a talajra, az út menti növényzetre, valamint a helyi felszíni és felszín alatti vízkészletekre is hatással vannak. Bár a só környezeti terhelésére utaló jeleket találtak a csúcsforgalom idején, a tavaszi esők és az olvadás általában felhígítják a nátrium koncentrációját azon a területen, ahol a sót kijuttatták. Egy 2009-es tanulmány szerint a Minneapolis-St Paul metropolisz területén kijuttatott útszóró só mintegy 70%-a visszamarad a helyi vízgyűjtőben.
HelyettesítésSzerkesztés
Néhány ügynökség sört, melaszt és répalevet használ útszóró só helyett. A légitársaságok a sóalapú megoldások helyett több glikolt és cukrot használnak jégtelenítésre.
Élelmiszeripar és mezőgazdaságSzerkesztés
Néhány mikroorganizmus nem tud sós környezetben élni: sejtjeikből ozmózis útján vonják ki a vizet. Ezért a sót egyes élelmiszerek, például a szalonna, a hal vagy a káposzta tartósítására használják.
A sót akár az élelmiszer-előállító, akár a fogyasztó ízfokozóként, tartósítószerként, kötőanyagként, erjedésgátló adalékanyagként, textúraszabályozó szerként és színfejlesztőként adják az élelmiszerekhez. Az élelmiszeripar sófogyasztása a fogyasztás csökkenő sorrendjében az egyéb élelmiszer-feldolgozó, húscsomagoló, konzervipari, sütőipari, tejipari és malomipari termékekre oszlik. A sót a szalonna, a sonka és más feldolgozott húskészítmények színfejlődésének elősegítésére adják hozzá. Tartósítószerként a só gátolja a baktériumok szaporodását. A só kötőanyagként működik a kolbászokban, hogy húsból, zsírból és nedvességből álló kötőgélt képezzen. A só ízfokozóként és puhítószerként is működik.
Számos tejiparban sót adnak a sajtokhoz szín-, erjedés- és textúraszabályozó szerként. A tejipari alágazat olyan vállalatokat foglal magában, amelyek tejszínes vajat, sűrített és párolt tejet, fagyasztott desszerteket, jégkrémet, természetes és feldolgozott sajtot, valamint különleges tejtermékeket gyártanak. A konzerviparban a sót elsősorban ízfokozóként és tartósítószerként adják hozzá. Emellett más összetevők hordozójaként, dehidratálószerként, enzimgátlóként és zsengeítőszerként is használják. A sütés során a sót a kenyértészta erjedési sebességének szabályozására adják. Használják továbbá a glutén (az egyes tésztákban lévő rugalmas fehérje-víz komplex) erősítésére és ízfokozóként, például a pékáruk feltétjeként. Az élelmiszer-feldolgozási kategória tartalmazza a gabonamalmok termékeit is. Ezek a termékek liszt és rizs őrléséből, valamint gabonafélékből készült reggeli ételek és kevert vagy elkészített liszt gyártásából állnak. A sót fűszerezőként is használják, pl. burgonyachipszekben, perecekben, macska- és kutyatápokban.
A nátrium-kloridot az állatgyógyászatban hányáskeltő szerként használják. Meleg, telített oldat formájában adják. Emesét okozhat kis mennyiségű sima só vagy sókristályok garatba helyezése is.
GyógyászatSzerkesztés
A nátrium-kloridot a vízzel együtt az intravénás terápia egyik elsődleges oldataként használják. Az orrspray gyakran tartalmaz sóoldatot.
TűzoltásSzerkesztés

A nátrium-klorid a fő oltóanyag a tűzoltó készülékekben (Met-L-X, Super D), amelyeket éghető fémek, például magnézium, kálium, nátrium és NaK ötvözetek (D osztály) tüzénél használnak. A keverékhez hőre lágyuló port, valamint vízszigetelő (fémsztearátok) és csomósodásgátló anyagokat (trikalcium-foszfát) adnak az oltóanyaghoz. A tűzre felhordva a só hőleadóként viselkedik, elvezeti a tűzből a hőt, és oxigén-kizáró kéreg képződik, amely megfojtja a tüzet. A műanyag adalékanyag megolvad, és segít a kéregnek megőrizni integritását, amíg az égő fém a gyulladási hőmérséklet alá nem hűl. Ezt a fajta tűzoltó készüléket az 1940-es évek végén találták fel patronos készülékként, bár ma már a tárolt nyomású változatok is népszerűek. Gyakori méretük a 30 font (14 kg) hordozható és a 350 font (160 kg) kerekes.
TisztítószerSzerkesztés
Az emberek legalább a középkor óta használják a sót a háztartási felületekre dörzsölve tisztítószerként. Számos samponmárkában, fogkrémben és népszerűen a kocsifelhajtók és jégfoltok jégtelenítésére is használják.
Optikai felhasználásSzerkesztés
A hibátlan NaCl-kristályok optikai áteresztőképessége az infravörös fényre, konkrétan 200 nm és 20 µm között kb. 90%. Ezért ebben a spektrális tartományban működő optikai alkatrészekben (ablakok és prizmák) használták őket, ahol kevés nem elnyelő alternatíva létezik, és ahol a mikroszkopikus inhomogenitások hiányára vonatkozó követelmények kevésbé szigorúak, mint a látható tartományban. Bár olcsó, a NaCl-kristályok lágyak és higroszkóposak – ha a környezeti levegőnek kiteszik őket, fokozatosan “fagy” borítja be őket. Ez a NaCl alkalmazását száraz környezetre, vákuummal lezárt összeszerelési területekre vagy rövid távú felhasználásra, például prototípusok készítésére korlátozza. Manapság az infravörös spektrumtartományban NaCl helyett olyan anyagokat használnak, mint a cink-szelenid (ZnSe), amelyek mechanikailag erősebbek és kevésbé érzékenyek a nedvességre.




