バリウムの実情
ギリシャ語で「重い」を意味するバリウスにちなんで名付けられたバリウムは、比較的密度が高く、反応しやすいアルカリ土類金属です。 他の元素と結合したときのみ天然に存在し、バリウムを含む化合物は幅広い用途を持っています。殺鼠剤、石油掘削液の重り、バリウム注腸というX線診断検査で腸を見るための白い液体などに含まれています。 Ba
バリウムの発見
17世紀のイタリアの錬金術師ヴィンチェンツォ・カシャロロは、熱にさらされると何年も光り続ける珍しい小石の形で、初めてバリウムに気づいたと英国化学協会が発表している。 彼はこの小石を自分の故郷にちなんで「ボローニャ石」と名付けたが、後に硫酸バリウム(BaSO4)であることが判明した。 18世紀後半には、ドイツの化学者カール・シャイーレとイギリスの化学者ウィザリングによって、それぞれ酸化バリウム(BaO)、炭酸バリウム(BaCO3)が発見されている。
純粋なバリウム金属は、ロンドンの王立研究所で1808年まで単離・同定されませんでした。 著名な化学者で発明家のサー・ハンフリー・デイヴィーは、水酸化バリウム(Ba(OH)2)のような溶融バリウム塩からバリウムを分離するために電気分解を使用しました。 電気分解では、イオン性の物質に電流を流して、イオン同士を分離させる。 バリウム塩は溶けているので、バリウムイオンはマイナス電極の容器に、その他のマイナスイオンはプラス電極の容器に、それぞれ反対方向に移動しやすくなっています。 バリウムは、最も一般的に硫酸塩と炭酸塩と結合しているが、また、水酸化物、塩化物、硝酸塩、塩素酸塩、および他の負イオンとの化合物を形成することができます。 地殻の約0.05%がバリウムで、地殻の中で17番目に多い元素であると、ロバート・E・クレブス氏の著書『The History and Use of Our Earth’s Chemical Elements』で述べられている。 A Reference Guide” (Greenwood Publishing Group, 2006)によると、バリウムは地殻の17番目に多い元素である。 英国、イタリア、チェコ、米国、ドイツに4億トン以上のバリウムが埋蔵されているという。
純粋なバリウム元素を得るには、天然に存在するバリウム化合物に含まれる他の元素から分離する必要があります。 バリウムは、電気分解によって塩化バリウムから抽出することができます。
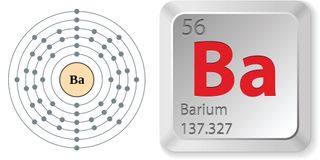
バリウムの性質
純バリウムは銀白色の柔らかい金属である。 アルカリ土類金属に分類され、ベリリウム、マグネシウム、カルシウム、ストロンチウム、ラジウムと一緒に、周期表のグループ、または列、2に位置しています。 それぞれの原子は2個の価電子を持つ。 バリウムは5番目の殻に価電子を持ち、電子を失いやすく、また酸化されやすい。 8111>
バリウムの商用利用
元素のバリウムは、やはり反応性が高いため、あまり実用的ではありません。 しかし、酸素への強い吸引力は、真空管内の空気の最後の痕跡を削除するための “ゲッター “として有用である。 また、純バリウムは他の金属と組み合わせて合金を作ることができ、ベアリングや内燃機関のスパークプラグなどの機械要素に使われる。 バリウムは電子の保持が緩いため、その合金は加熱すると容易に電子を放出し、スパークプラグの効率を向上させるとクレブス氏は言う。
バリウムを含む化合物は、さまざまな商業用途がある。 硫酸バリウム、またはバライトは、リトポン(プリンター用紙や塗料の光沢顔料)、油井の掘削液、ガラス製造、ゴムの作成に使用されています。 炭酸バリウムは殺鼠剤として使用され、硝酸バリウムと塩素酸バリウムは花火の緑色を作り出す。
Barium in your body
バリウムは、ニンジン、タマネギ、レタス、豆、穀物などの食品に含まれているため、一般成人には約22mgのバリュームが含まれています。 歯に含まれるバリウムの量は、赤ちゃんが母乳から固形食に移行する時期を科学者が判断するのに役立ちます。 このような低レベルのバリウムは生物学的な役割はなく、有害ではありません。
しかし、大量の可溶性バリウム塩は毒性があり、死に至ることさえあると、ジョン・エムズリーは著書「The Elements of Murder」の中で述べています。 A History of Poison” (Oxford University Press, 2005) によると、大量のバリウム塩は有害であり、死に至ることもあるという。 バリウムは嘔吐、疝痛、下痢、震え、麻痺を引き起こすことがある。 バリウム化合物による殺人事件は一握りで、1994年にはテキサス州マンスフィールドで、16歳の娘マリー・ロバーズが高校の化学実験室から酢酸バリウムを盗んで男性を殺害した事件もある。 また、バリウム浣腸と呼ばれる消化器系の診断検査で、不溶性の硫酸バリウムではなく、水溶性の炭酸バリウムが誤って使用され、数名の患者がバリウムによって誤って死亡しています。
Johns Hopkins Medicineによると、医師は大腸と直腸の異常を視覚化し診断するために、バリウム注腸を実施します。 その際、硫酸バリウムを直腸から注入し、大腸の内壁をコーティングします。 次に、バリウムの被膜が表面の異常をすべて埋めることを確認するために、通常、空気が投与される。 その後、X線を用いて下部消化管の画像を作成します。 硫酸バリウムはX線を吸収するため、X線フィルムに白く写り、空気や周囲の組織が黒く写るのと対照的です。 バリウム注腸のX線画像を解析することにより、潰瘍性大腸炎、クローン病、ポリープ、がん、過敏性腸症候群などの診断が可能になります。




