波動関数の定義
Ψ
電子などの基本粒子は、粒子または波として記述されることがあります。
電子は波動関数を用いて記述することができる。波動関数の記号はギリシャ文字のサイ、Ψまたはψである。

波動関数Ψは数学式である。波動関数から、量子数n、l、mlの形で、電子のエネルギー、角運動量、軌道の向きを得ることができるのです。
1926年、エルヴィン・シュレーディンガーは、すべての原子の中で最も単純な水素の波動関数を推論しました。
シュレーディンガー方程式は量子力学の方程式であり、計算された波動関数は原子や分子に結合した電子に対して離散的な許容値を持ち、他のすべての値は禁止されている。
Ψの重要性に加え、その二乗Ψ2も化学において非常に重要である。
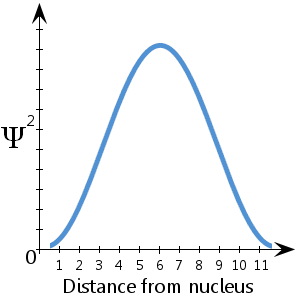
例えば、核からの距離に対するΨ2を示す、ここにプロットした(架空の)概略図では、電子は核から約 5-7 単位の間に見つかる可能性が最も高いことがわかります。
電子がどこかに存在する確率は100%で、言い換えれば確率は1です。
Ψは電子が1個の原子、すなわちH、He+、Li2+、Be3+、B4+、C5+などに対してのみ正確に計算できます。数学用語としては、1電子系に対してのみΨの解析的解が可能になると言います。「
他のすべての原子、イオン、および分子では、Ψの解析解は得られません。様々なΨ2分布が水素の電子軌道です。実際に占有される軌道は、電子の持つエネルギー量によって決定される。
水素の軌道の例
2s
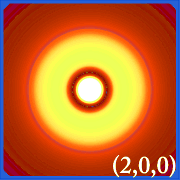
2pz
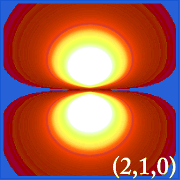
2px

3dz2

3dxz

3dxy






