Beräkning av moläritet
Relaterade ämnen:
Mer kemilektioner
Detta är en serie föreläsningar i videoklipp som täcker ämnen inom kemi som lärs ut i gymnasieskolor.
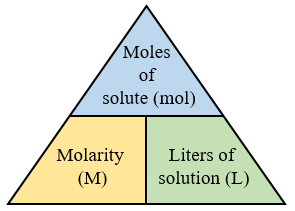
Det följande diagrammet visar hur man konverterar mellan moläritet, mol och volym. Scrolla nedåt på sidan för fler exempel och lösningar.
Övningsuppgifter om molaritet
Övningsuppgifter om molaritet, beräkna mol och liter för att hitta den molära koncentrationen.
Hur man använder omräkningsfaktorer för att omvandla mellan gram och mol, och mellan milliliter och liter.
Exempel:
1. Beräkna molariteten i en lösning som framställs genom att lösa 9,8 mol fast NaOH i tillräckligt mycket vatten för att få fram 3,62 L lösning.
2. Du löser 152,5 g CuCl2 i vatten för att få fram en lösning med en slutvolym på 2,25L. Vad är dess molaritet?
3. En lösning har en volym på 375 mL och innehåller 42,5 g NaCl. Vad är dess molaritet?
- Visa steg-för-steg-lösningar
Hur löser man molaritetsproblem?
Exempel:
1. Hur många mol NaCl finns i 3,5L av en 1,5M lösning av NaCl?
2. Om du har 4,1 mol glukos och vill ha en 0,25 M-lösning med det, vad blir lösningens slutliga volym?
3. Om en elev har 35,0 g FeCl3 och behöver göra en 1.5 molär lösning med den, vad blir då lösningens volym?
4. Hur många gram NaOH måste du lösa upp för att göra 725 mL av en 2,5 M-lösning?
- Visa steg-för-steg-lösningar
Så här beräknar du moläritet | Övningsproblem nr 1
Exempel:
Vad är moläriteten hos en lösning som framställs genom att 1,461 g NaCl löses upp i 250,0 mL vatten? (MM av NaCl = 58,443 g/mol)
- Visa steg-för-steg-lösningar
Hur man beräknar molaritet | Övningsproblem #2
Hur många gram AgNO3 behövs för att bereda 250mL 0,0125M AgNO3? (MM AgNO3 = 169,87 g/mol)
- Visa steg-för-steg-lösningar
Koncentrationsberäkningar 1 (molaritet)
En handledning i att beräkna en lösnings molaritet eller koncentration.
Exempel:
1. Om 1,25 mol NaCl löses upp i 250 ml vatten, bestäm molariteten.
2. Om 12,0 gram kalciumbromid löses upp i 500 ml vatten, bestäm molariteten.
- Visa steg-för-steg-lösningar
Koncentrationsberäkningar 2 (ppm)
En handledning i hur man beräknar koncentrationen av en lösning i miljondelar.
Exempel:
1. Jane löser upp 2,5 gram rengöringsmedel i 1250 ml vatten för att rengöra en vattenkanna. Bestäm koncentrationen av den resulterande lösningen i ppm.
2. Om 1,3 × 10-2 mol bariumnitrat löses upp i 750 mL vatten, vad skulle koncentrationen vara i ppm?
- Visa steg-för-steg-lösningar
Prova den kostnadsfria Mathway-kalkylatorn och problemlösaren nedan för att öva olika matematiska ämnen. Prova de givna exemplen eller skriv in ditt eget problem och kontrollera ditt svar med hjälp av de stegvisa förklaringarna.