Benigne Neoplasmen der Vulva | GLOWM
Condyloma Acuminatum
Humane Papillomavirus (HPV)-Infektionen der Vulva sind häufige klinische Erscheinungen. HPV-Infektionen werden als klinisch oder subklinisch eingestuft, abhängig von der Infektiosität des Virus und der Reaktion des betroffenen Epithels. Der typische Ausdruck ist eine weiche, rosa-weiße, papilläre Epithelläsion. Diese Läsionen können einzeln oder in Clustern auftreten, die konfluierend werden können (Abb. 1). Die üblichen Lokalisationen der Vulva sind das Präputium, das Vestibulum und der Dammkörper. Auch perianale und anale Lokalisationen werden häufig gesehen.
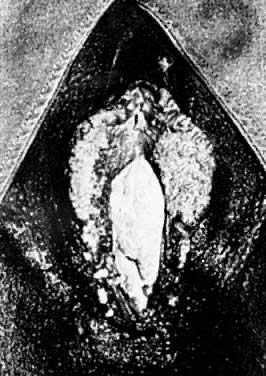 Abb. 1. Multiple vulväre Condylomata acuminata.
Abb. 1. Multiple vulväre Condylomata acuminata.
Obwohl es mehr als 60 HPV-Subtypen gibt, befallen nur relativ wenige die Vulva.1 Die HPV-Subtypen, die am häufigsten an der Vulva vorkommen, sind HPV 6 und HPV 11. HPV 2, das Virus, das mit häufigen Epithelwarzen in Verbindung gebracht wird, kommt auch im Plattenepithel der Vulva vor.2 HPV-Subtypen, die mit einer höheren Inzidenz maligner Transformationen am Gebärmutterhals in Verbindung gebracht werden, insbesondere HPV 16, 18, 31 und 35, können auch bei vulvären Läsionen vorhanden sein.1 Die Häufigkeit der Diagnose von vulvären, vaginalen und zervikalen HPV-Läsionen hat in den letzten drei Jahrzehnten erheblich zugenommen.3 Dieser Anstieg ist zum Teil auf Fortschritte bei den Diagnosetechniken zurückzuführen, wie z. B. die Polymerase-Kettenreaktion und DNA-Hybridisierungsverfahren. Obwohl es schwierig ist, die Inzidenz oder Prävalenz der Infektion zu schätzen, liegt der geschätzte Prozentsatz der Patienten mit klinischer und subklinischer HPV-Infektion in einigen Hochschulpopulationen bei über 40 %.1 Es gibt keine zuverlässige Methode zur Identifizierung subklinischer oder ruhender Infektionen. Selbst wenn man nur die klinisch exprimierten HPV betrachtet, sind sie heute eine der häufigsten sexuell übertragbaren Krankheiten. Einige HPV-Infektionen können sich zu einer vulvären intraepithelialen Neoplasie (VIN) entwickeln, und ein noch kleinerer Teil kann zu einem invasiven Plattenepithelkarzinom der Vulva fortschreiten, doch die meisten Läsionen beschränken sich auf die HPV-Kutaneus-Expression, die als Feigwarze oder Kondylom bekannt ist. Immunsuppression und Schwangerschaft sind mit der Vergrößerung und dem Fortschreiten der kondylomatösen Läsionen verbunden (Abb. 2).3
 Abb. 2: Hypertrope Condylomata acuminata bei einer schwangeren Patientin.
Abb. 2: Hypertrope Condylomata acuminata bei einer schwangeren Patientin.
Histologisch gesehen erscheinen Kondylome als epitheliale Papillome mit Akanthose und Parakeratose (Abb. 3). Einige Epithelzellen weisen atypische Zellkerne und perinukleäre Halos auf, die vermutlich eine Manifestation einer HPV-Infektion sind.2 Diese Zellen werden als Koilozyten bezeichnet. Das darunter liegende Stroma weist in der Regel eine leichte Entzündungsreaktion auf. Bei behandlungsresistenten oder anormal aussehenden kondylomatösen Läsionen sollten zur histologischen Absicherung der Diagnose Biopsien durchgeführt werden. Dann kann zwischen Kondylomen und Vulvapapillomatose oder anderen vulvären Läsionen unterschieden werden.
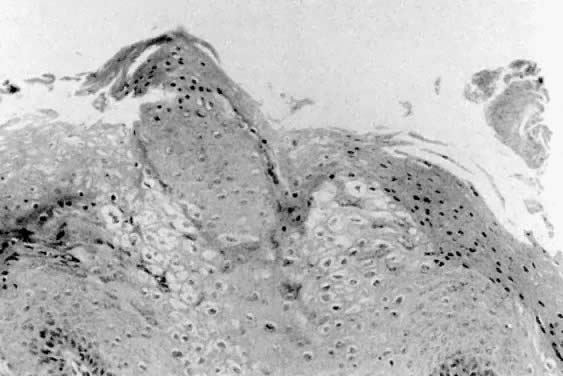 Abb. 3. Kondylome mit Akanthose, Parakeratose und koilozytotischen Veränderungen.
Abb. 3. Kondylome mit Akanthose, Parakeratose und koilozytotischen Veränderungen.
Die Behandlung besteht in der Zerstörung der kutanen Manifestationen der HPV-Infektion. Eine Eradikation des Virus aus dem Epithel ist klinisch nicht möglich. Die Kontrolle der epithelialen Virusexpression kann mit topischen Mitteln wie Trichloressigsäure, Bichloressigsäure, Podophyllin oder seinen Derivaten oder topischem 5-Fluorouracil (5-FU) erreicht werden. Weitere Behandlungsmethoden sind Kryotherapie, Laservaporisation, Elektroexzision oder Exsikkation. Die intraläsionale oder systemische Verabreichung von Interferon ist eine weitere therapeutische Option, die in der Regel nur bei rezidivierenden Läsionen eingesetzt wird. Rezidivierende virale Hautveränderungen werden in der Regel mit alternativen Behandlungen oder Kombinationen von Behandlungen behandelt.
Das Vulvakarzinom erscheint als großes Kondylom oder als Läsion mit Verdacht auf ein invasives Karzinom. Die Läsion, die erstmals von Buschke und Lowenstein als Riesenkondylom beschrieben wurde,2 ist mit dem viralen Subtyp HPV 6 assoziiert.1 Das verruköse Karzinom kann große Bereiche der Vulva betreffen und hat eher eine schiebende als eine infiltrierende Grenze. Charakteristischerweise ist es auf die Vulva beschränkt. Die Behandlung erfolgt am besten durch eine breite Exzision und eine sorgfältige postoperative Untersuchung.
Vulväre intraepitheliale Neoplasie
Vulväre intraepitheliale Neoplasie ist eine hyperplastische Plattenepithelläsion mit Atypien, die auf das Epithel beschränkt ist. Die VIN wird histologisch in drei Kategorien eingeteilt: VIN I (leichte Dysplasie), VIN II (mäßige Dysplasie) und VIN III (schwere Dysplasie und Karzinom in situ). VIN-Läsionen sind ausreichend atypisch, um als prämaligne Läsionen betrachtet zu werden. Die Inzidenz der Progression zu einem malignen invasiven Prozess ist relativ gering (10 % bis 15 %), und der Zeitrahmen für die Progression kann sich über mehrere Jahre erstrecken.4
Bowen-Krankheit, VIN III und Karzinom in situ sind klinisch synonyme Begriffe. Diese Läsionen erscheinen als hyperkeratotische, erhabene und häufig pigmentierte Epithelverdickungen (Abb. 4). Sie treten in der Regel bei Frauen ab dem sechsten Lebensjahrzehnt auf; ein jüngeres Alter schließt die Diagnose jedoch nicht aus. Der Biopsiebefund zeigt eine vollflächige Epithelatypie und mitotische Aktivität (Abb. 5). Die betroffenen Stellen können asymptomatisch sein oder durch Kratzen exkoriert werden. Jede verdickte, erhabene oder hyperkeratotische Läsion, die bei einer gynäkologischen Untersuchung festgestellt wird, sollte unabhängig von den damit verbundenen Symptomen für eine Biopsie in Betracht gezogen werden. Vulväre Läsionen können multifokal sein; daher werden mehrere Biopsien empfohlen. Die Anreicherung von Läsionen mit Farbstoffen wie Toluidinblau wird empfohlen, um die multifokale Natur dieser Läsionen zu berücksichtigen. Toluidinblau sollte die Bereiche mit Kernkonzentration anfärben, die mit VIN III assoziiert sind; die meisten Läsionen sind jedoch hyperkeratotisch, und die Keratinoberfläche verhindert das Eindringen des Farbstoffs in die Epithelkerne. Ein wirksamerer Ansatz ist die Anwendung einer verdünnten Essigsäurelösung auf der Vulva. Bereiche mit VIN- und HPV-Expression werden nach mehrminütigem Einweichen acetoweiß.4 Die Vulva kann dann mit einer Lupe oder einem Kolposkop untersucht werden. Auf diese Weise lassen sich subtile epitheliale Veränderungen leichter erkennen.
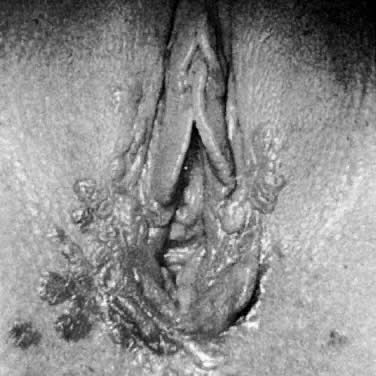 Abb. 4. Karzinom in situ mit hyperkeratotischer pigmentierter Epithelverdickung.
Abb. 4. Karzinom in situ mit hyperkeratotischer pigmentierter Epithelverdickung.
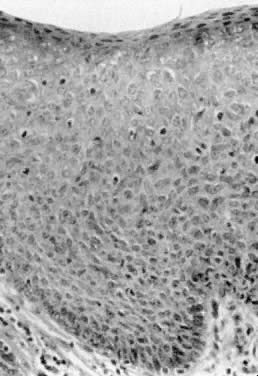 Abb. 5. Carcinoma in situ mit epithelialer Atypie in der gesamten Epithelschicht.
Abb. 5. Carcinoma in situ mit epithelialer Atypie in der gesamten Epithelschicht.
Der Morbus Bowen oder VIN III sollte durch chirurgische, Laser- oder elektrische Exzision behandelt werden.4 Es ist vorzuziehen, die Läsion mit einer Technik zu entfernen, die Gewebe für weitere histologische Untersuchungen liefert. Der Einsatz von 5-FU oder systemischem Interferon hat sich als wenig erfolgreich erwiesen.3,5 Die chirurgische Exzision mit Beurteilung der Ränder bleibt die bevorzugte Behandlungsoption. Eine engmaschige Nachbeobachtung zur Beurteilung des Wiederauftretens wird empfohlen.
Die Bowenoid-Papillose hat ein klinisches und pathologisches Erscheinungsbild, das dem von VIN III ähnelt. Sie tritt bei Patienten im zweiten, dritten und vierten Lebensjahrzehnt auf. Sie äußert sich in Form multipler papillomatöser Läsionen, die mehr als einen Bereich der Vulva betreffen können.3,4 Diese Läsionen werden mit HPV-Infektionen in Verbindung gebracht. Der Biopsiebefund zeigt eine Epithelatypie mit koilozytotischen Veränderungen von HPV. Eine Progression zu einem invasiven Malignom tritt in seltenen Fällen auf, z. B. bei immunsupprimierten oder immungeschwächten Patienten. Die Behandlung ist konservativ, es sei denn, es liegen prämaligne Veränderungen vor. Prämaligne Läsionen werden ähnlich wie VIN behandelt.
Basalzellkarzinom
Basalzellkarzinome sind in der Regel asymptomatisch, bis sie groß genug sind, um vom Patienten bemerkt zu werden, oder bis sich Ulzerationen und Blutungen entwickeln. Der Tumor ist fest mit eingerollten Rändern und findet sich am häufigsten an den großen Schamlippen postmenopausaler Frauen. Eine Metastasierung ist selten. Die Behandlung besteht in einer breiten Exzision des Tumors mit angemessenen Rändern. Eine Untersuchung auf Metastasen sollte in Erwägung gezogen werden, wenn das exzidierte Präparat eine Invasion des subkutanen Fettgewebes, eine Tumordicke von mehr als 1 cm oder eine Beteiligung der Harnröhre oder Vagina aufweist. Basalzellkarzinome machen 2 bis 4 % der gutartigen Neubildungen der Vulva aus.6
Histologisch weisen diese Tumoren eine periphere Palisadierung der Basalzellen an den Epithelrändern auf. Der Rest des Tumors besteht aus dicht gepackten, einheitlichen Zellen mit basophilen Kernen und wenig Zytoplasma. Mitosefiguren sind häufig. Diese Tumoren sind lokal invasiv; daher ist eine gründliche Untersuchung der gesamten Läsion erforderlich. Insbesondere die Ränder sollten auf ihre Angemessenheit hin untersucht und gemeldet werden. Bei Rändern von weniger als 4 mm besteht ein höheres Risiko für ein Rezidiv.
Acrochordon
Fibroepitheliale Polypen sind im Epithel der Vulva häufig. Sie werden auch als Skin Tags bezeichnet. Diese Läsion hat kein bösartiges Potenzial. Es handelt sich um weiche, fleischfarbene, polypoide Strukturen. Hautanhangsgebilde und Haare sind für Akrochordon nicht charakteristisch. Die Therapie besteht in der lokalen Exzision der symptomatischen Läsionen.
Histologisch wird das Akrochordon als fibrovaskulärer Stiel mit reifem hyperkeratotischem Plattenepithel beschrieben. Epidermale Anhängsel sind selten, und das Gefäßmuster kann verstärkt sein.
Hidradenom
Hidradenome sind Tumore der apokrinen Schweißdrüsen. Einige können ihren Ursprung in den ekkrinen Schweißdrüsen haben. Sie haben in der Regel einen Durchmesser von weniger als 1 cm und treten an der medialen Seite der großen Schamlippen auf (Abb. 6). Die Läsionen sind fest und frei beweglich. Wenn die Läsion mit der Epitheloberfläche in Berührung kommt, können Ulzerationen und Schmerzen auftreten. Die Behandlung besteht in der chirurgischen Exzision.
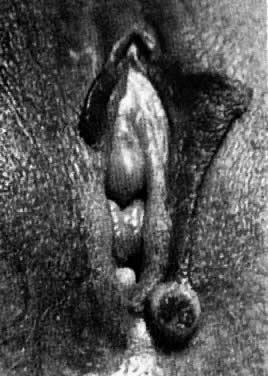 Abb. 6. Hidradenom der Vulva.
Abb. 6. Hidradenom der Vulva.
Histologisch weist das Hidradenom zystische Räume auf, die mit säulenförmigen Zellen ausgekleidet sind. Die Läsion ist außerdem durch viele komplexe Falten, papilläre Strukturen und eine ausgeprägte Drüsenproliferation gekennzeichnet (Abb. 7). Diese Läsion kann mit einem Adenokarzinom verwechselt werden. Zu den Unterscheidungsmerkmalen des Hidradenoms gehören das Fehlen von Pleomorphismus, das Aufeinanderstapeln von Zellen und die Kernkonformität.
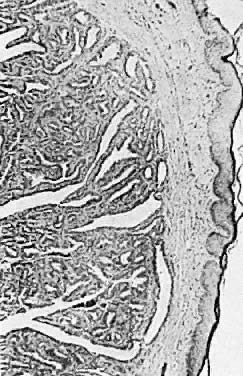 Abb. 7. Hidradenom der Vulva ( × 25)
Abb. 7. Hidradenom der Vulva ( × 25)
Syringom
Syringome sind kleine, gutartige Hamartome der ekkrinen Schweißdrüsen. In der Regel liegen multiple Läsionen vor, die an mehr als einer Stelle des Körpers auftreten können. Die Läsionen sind asymptomatisch und bedürfen keiner Behandlung, es sei denn, es treten Schmerzen oder Juckreiz auf.7
Mikroskopisch gesehen handelt es sich um Tumore aus erweiterten Schweißdrüsengängen und Zysten, die mit gutartigen quaderförmigen Zellen ausgekleidet sind (Abb. 8). Eine minimale Entzündungsreaktion ist vorhanden, es sei denn, die Zysten brechen auf.
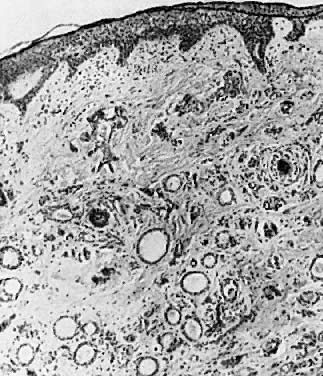 Abb. 8 . Syringom Zahlreiche erweiterte Schweißdrüsengänge sind zu sehen ( × 35).
Abb. 8 . Syringom Zahlreiche erweiterte Schweißdrüsengänge sind zu sehen ( × 35).
Pigmentierte Vulvatumoren
Pigmentierte Vulvarialläsionen treten bei 10 bis 12 % aller Frauen auf. Zwei Prozent haben pigmentierte Veränderungen mit prämalignen Merkmalen. Gutartige pigmentierte Läsionen werden als Lentigines, vulväre Melanose und Nävi klassifiziert.
Lentigines sind kleine (1 bis 4 mm), gut umschriebene Makel. Sie treten bei 3 bis 6 % der Frauen auf. Lentigines sind auch Teil mehrerer Syndrome, zu denen Vorhofmyxome und andere kardiale Struktur- und Leitungsstörungen gehören (LAMB-Syndrom, LEOPARD-Syndrom).8 Eine Therapie ist nicht erforderlich.
Histologisch ähneln Lentigines junktionalen Nävi. Es besteht eine Hyperplasie in der Epidermis und eine erhöhte Melaninproduktion in der Basalschicht der Haut. Eine Kernatypie ist im hyperplastischen Gewebe nicht zu erkennen.
Die Vulvamelanose ist eine Läsion, die größer als eine Lentigo ist und einen unregelmäßigen Rand aufweist. Histologisch ist eine erhöhte Anzahl von Melanozyten und dermalen Melanophagen zu erkennen. Es kommt zu Melaninablagerungen in den basalen und suprabasalen Epidermisschichten. Die Vulvamelanose und die Lentigines sind Teil eines Spektrums von Pigmentveränderungen an der Vulva. Es ist wichtig, sie von Melanomen zu unterscheiden, indem eine Biopsie eines repräsentativen Bereichs durchgeführt wird.
Vulväre Nävi treten bei 2 % der Frauen auf. Nävi werden in intradermale, junktionale und zusammengesetzte Nävi unterteilt. Der intradermale Naevus entsteht in der Dermis (Abb. 9), und der junktionale Naevus entsteht in der basalen Epidermisschicht (Abb. 10). Der Compound-Nävus weist Merkmale sowohl des intradermalen als auch des junktionalen Nävus auf (Abb. 11). Die histologische Untersuchung der Melanozyten auf atypische Architektur und zytologische Veränderungen unterscheidet pigmentierte Nävi von Melanomen. Irritierte oder blutende Nävi sollten exzidiert werden. Ein hoher Verdachtsindex und ein großzügiger Einsatz der Exzision sollten Teil des Behandlungsschemas sein.
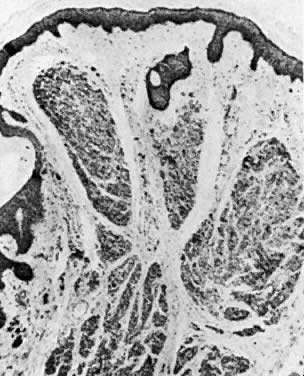 Abbildung 9. Intradermaler Naevus. Naevuszellen sind in der oberen Dermis zu sehen (× 40)
Abbildung 9. Intradermaler Naevus. Naevuszellen sind in der oberen Dermis zu sehen (× 40)
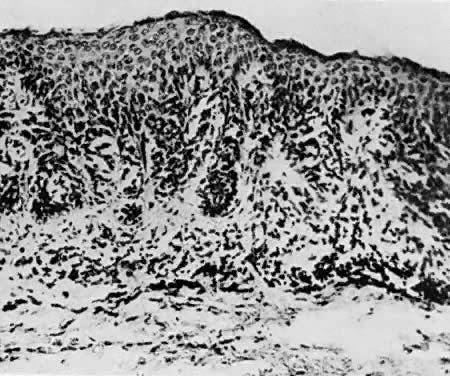 Abb. 10. Junctional Naevus. Dieser Typ kann bösartig werden ( × 50)
Abb. 10. Junctional Naevus. Dieser Typ kann bösartig werden ( × 50)
 Abb. 11. Zusammengesetzter Naevus. Nävuszellen sind an der Grenze zwischen Epidermis und Dermis und in der oberen Dermis zu sehen (× 50)
Abb. 11. Zusammengesetzter Naevus. Nävuszellen sind an der Grenze zwischen Epidermis und Dermis und in der oberen Dermis zu sehen (× 50)




