Perfect Scorer Test Prep: Chemie: Was bedeutet das Wort „gesättigt“?
In der Chemie kann das Wort „gesättigt“ verwendet werden, um einzelne Moleküle oder ganze Lösungsmittelgemische zu beschreiben, und es hat in jeder dieser Situationen eine andere Bedeutung.
Gemeinsam gesprochen ist etwas, das gesättigt ist, völlig voll, wie bei einem gesättigten Schwamm (der mit Wasser gefüllt ist) oder bei einem Sättigungsbombardement (der Einsatz von Hunderten von Bomben, um ein ganzes Gebiet zu zerstören).
Gesättigte und ungesättigte Moleküle
Wenn das Wort auf ein einzelnes Molekül angewendet wird, bedeutet es, dass das Molekül keine Kohlenstoff-Kohlenstoff-Doppelbindungen oder Ringe hat. Bei den folgenden Molekülen ist zu beachten, dass die Umwandlung einer Einfachbindung in eine Doppelbindung bedeutet, dass zwei Wasserstoffatome entfernt werden müssen:
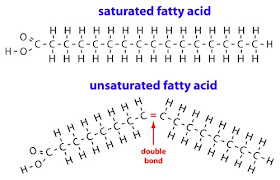
Da Kohlenstoff nur vier Bindungen haben kann, werden durch das Hinzufügen einer C=C-Doppelbindung zwei Plätze verbraucht, an die stattdessen Wasserstoff hätte gebunden werden können.
Das erste Molekül hat so viele Wasserstoffatome, wie es aufnehmen kann (keine Doppelbindungen), ist also gesättigt oder voller Wasserstoff. Da das zweite Molekül eine Doppelbindung hat, verfügt es nicht über alle Wasserstoffatome, die es enthalten könnte, und ist daher ungesättigt.
Wichtig: Fettsäuren gelten als gesättigt, wenn der Teil der Kohlenwasserstoffkette des Moleküls keine Doppelbindungen enthält. Das C=O in der COOH-Gruppe am linken Ende des Moleküls wird nicht berücksichtigt.
Beachte, dass auch das Vorhandensein eines Rings ein Molekül ungesättigt macht. Geradkettiges und verzweigtes Pentan haben beide die Formel C5H12, während das ringförmige Molekül Cyclopentan die Formel C5H10 hat:
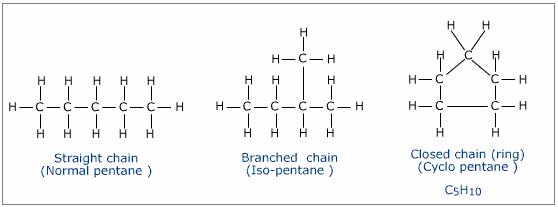
Bei der Bildung der Ringform werden die beiden Kohlenstoffe an den Enden der Kette miteinander verbunden, wodurch zwei Bindungsstellen in Anspruch genommen werden, an denen sich sonst Wasserstoffatome befinden würden. Geradkettige und verzweigtkettige Kohlenwasserstoffe sind gesättigt, während ringförmige Kohlenwasserstoffe ungesättigt sind.
Übrigens gibt es kein übersättigtes Molekül. Wenn Sie diese Option in einem Test sehen, handelt es sich um eine Trickfrage.
Gesättigte, ungesättigte und übersättigte Lösungen
Das Wort „gesättigt“ hat eine andere Bedeutung, wenn es zur Beschreibung von Lösungen verwendet wird.
Bei den folgenden Definitionen ist zu beachten, dass das Lösungsmittel die Chemikalie ist, in der sich der gelöste Stoff auflöst. Es gibt immer mehr Lösungsmittel als gelöste Stoffe.
Zum Beispiel ist Salzwasser eine Lösung von Natriumchlorid (dem gelösten Stoff) in Wasser (dem Lösungsmittel).
Das Lösungsmittel ist normalerweise eine Flüssigkeit, aber es muss nicht sein: Luft ist eine Lösung von Sauerstoff, Kohlendioxid und Wasserdampf (gelöste Stoffe) in Stickstoff (dem Lösungsmittel). Stahl ist eine Lösung von Kohlenstoff (dem gelösten Stoff) in Eisen (dem Lösungsmittel).

Gesättigte Lösungen enthalten so viel gelösten Stoff, wie das Lösungsmittel aufnehmen kann.
Das Tote Meer ist gesättigt: Es enthält so viel Salz und Mineralien, wie es aufnehmen kann. Es enthält so viel Salz, dass das Wasser eine höhere Dichte als der menschliche Körper hat und Menschen darin leicht schwimmen können. In der Abbildung rechts sind die weißen festen Teile die Salzstücke, die sich nicht auflösen können, weil das Wasser bereits gesättigt ist.
Ungesättigte Lösungen enthalten weniger gelöste Stoffe, als das Lösungsmittel aufnehmen kann.
Im Gegensatz zum Toten Meer ist normales Meerwasser ungesättigt. Obwohl es sehr salzig ist, enthält es nicht so viel Salz, wie es aufnehmen kann.

Übersättigte Lösungen enthalten mehr gelöste Stoffe, als das Lösungsmittel aufnehmen kann.
Man kann Kandiszucker herstellen, indem man Zuckerwasser kocht und es dann abkühlt, was zu einer Übersättigung führt: Der Zucker soll aus der Lösung kommen, aber er tut es nicht, bis man einen Impfkristall hineinwirft. (Das Fehlen eines Impfkristalls ist auch einer der Gründe dafür, dass Bäume im Winter nicht erfrieren.)
Das folgende Video zeigt, wie du deine eigene übersättigte Natriumacetatlösung herstellen und sie zur Herstellung von Skulpturen aus „heißem Eis“ verwenden kannst:
Dazu musst du auch die folgenden Begriffe kennen:
Verdünnte Lösungen enthalten im Vergleich zur Menge des Lösungsmittels sehr wenig gelösten Stoff.
Konzentrierte Lösungen enthalten im Verhältnis zur Menge des Lösungsmittels sehr viel gelöste Stoffe.
Trickfragen
Eine häufige Trickfrage besteht darin, dass Sie die Begriffe gesättigt, ungesättigt, übersättigt, verdünnt und konzentriert richtig unterscheiden sollen.
Eine Lösung kann sowohl gesättigt als auch verdünnt sein: Wenn die Löslichkeit gering ist, wie z. B. bei der Zugabe von Jodkristallen in Seewasser, um Keime abzutöten, ist die Lösung gleichzeitig gesättigt (voll mit gelösten Stoffen) und verdünnt (nicht sehr konzentriert). Es ist gut, dass I2 unpolar und nicht sehr wasserlöslich ist: Wäre die Lösung konzentriert, würde man große Mengen eines elementaren Halogens trinken!
Ozeanwasser hingegen ist sowohl ungesättigt als auch konzentriert.
Das Tote Meer ist sowohl gesättigt als auch konzentriert.




