Violações da Regra do Octeto
Excepção 2: Octetos incompletos
A segunda excepção à Regra do Octeto é quando há muito poucos electrões de valência que resultam num Octeto incompleto. Há ainda mais ocasiões em que a regra do octeto não dá a representação mais correta de uma molécula ou íon. Este é também o caso dos octetos incompletos. Espécies com octetos incompletos são bastante raras e geralmente são encontradas apenas em alguns compostos de berílio, alumínio e boro, incluindo os hidretos de boro. Vamos dar uma olhada em um desses hidretos, \(BH_3\) (Borano).
Se fosse para fazer uma estrutura de Lewis para \(BH_3\) seguindo as estratégias básicas para desenhar as estruturas de Lewis, provavelmente se criaria esta estrutura (Figura 3):
O problema com esta estrutura é que o boro tem um octeto incompleto; ele tem apenas seis elétrons em torno dele. Os átomos de hidrogênio podem naturalmente ter apenas 2 elétrons em sua casca mais externa (sua versão de um octeto), e como tal não há elétrons sobressalentes para formar uma dupla ligação com o boro. Pode-se supor que a falha desta estrutura em formar octetos completos deve significar que esta ligação deve ser iónica em vez de covalente. No entanto, o boro tem uma eletronegatividade muito semelhante ao hidrogênio, o que significa que provavelmente há muito pouco caráter iônico nas ligações hidrogênio-boro, e como tal esta estrutura de Lewis, embora não cumpra a regra do octeto, é provavelmente a melhor estrutura possível para representar o BH3 com a teoria de Lewis. Uma das coisas que pode explicar o octeto incompleto de BH3 é que ele é geralmente uma espécie transitória, formada temporariamente em reações que envolvem múltiplos passos.
Vejamos outra situação de octeto incompleto lidando com o boro, BF3 (Boron trifluorine). Como com BH3, o desenho inicial de uma estrutura de Lewis de BF3 formará uma estrutura onde o boro tem apenas seis elétrons em torno dele (Figura 4).
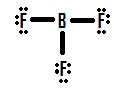
Se você olhar a Figura 4, você pode ver que os átomos de flúor possuem pares solitários extras que eles podem usar para fazer ligações adicionais com o boro, e você pode pensar que tudo o que você tem que fazer é fazer um par solitário em uma ligação e a estrutura estará correta. Se adicionarmos uma ligação dupla entre o boro e um dos flúor, obtemos a seguinte estrutura de Lewis (Figura 5):
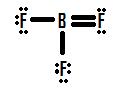
Cada flúor tem oito electrões, e o átomo de boro também tem oito! Cada átomo tem um octeto perfeito, certo? Não tão rápido. Temos de examinar as cargas formais desta estrutura. O flúor que compartilha uma dupla ligação com o boro tem seis elétrons ao seu redor (quatro de seus dois pares únicos de elétrons e um de cada um de suas duas ligações com o boro). Este é um elétron a menos do que o número de elétrons de valência que teria naturalmente (Grupo sete elementos têm sete elétrons de valência), portanto tem uma carga formal de +1. As duas farinhas que compartilham ligações simples com o boro têm sete elétrons ao seu redor (seis de seus três pares solitários e um de suas ligações simples com o boro). Esta é a mesma quantidade que o número de elétrons de valência que eles teriam por si mesmos, de modo que ambos têm uma carga formal de zero. Finalmente, o boro tem quatro elétrons ao seu redor (um de cada uma de suas quatro ligações compartilhadas com o flúor). Este é mais um elétron do que o número de elétrons de valência que o boro teria por si só, e como tal o boro tem uma carga formal de -1,
Esta estrutura é suportada pelo fato de que o comprimento de ligação experimentalmente determinado das ligações do boro ao flúor em BF3 é menor do que o que seria típico para uma única ligação (ver Ordem e Comprimento das Ligações). No entanto, esta estrutura contradiz uma das principais regras das acusações formais: As cargas formais negativas devem ser encontradas no(s) átomo(s) mais electronegativo(s) de uma ligação, mas na estrutura descrita na Figura 5, uma carga formal positiva é encontrada no flúor, que não só é o elemento mais electronegativo na estrutura, mas o elemento mais electronegativo em toda a tabela periódica (\chi=4.0\)). Já o boro, com a eletronegatividade muito menor de 2,0, tem a carga formal negativa nesta estrutura. Esta discordância formal carga-electronegatividade torna impossível esta estrutura de dupla ligação.
No entanto a grande diferença de eletronegatividade aqui, ao contrário de BH3, significa ligações polares significativas entre o boro e o flúor, o que significa que existe um elevado carácter iónico nesta molécula. Isto sugere a possibilidade de uma estrutura semi-iônica como a vista na Figura 6:

Nenhuma destas três estruturas é a estrutura “correta” neste caso. A estrutura mais “correta” é muito provavelmente uma ressonância das três estruturas: aquela com o octeto incompleto (Figura 4), aquela com a dupla ligação (Figura 5), e aquela com a ligação iônica (Figura 6). A estrutura que mais contribui é provavelmente a estrutura do octeto incompleto (devido ao fato da Figura 5 ser basicamente impossível e da Figura 6 não corresponder ao comportamento e propriedades do BF3). Como você pode ver mesmo quando outras possibilidades existem, octetos incompletos podem retratar melhor uma estrutura molecular.
Como uma nota lateral, é importante notar que BF3 frequentemente se liga com um íon F a fim de formar BF4- em vez de ficar como BF3. Esta estrutura completa o octeto de boro e é mais comum na natureza. Isto exemplifica o fato de que octetos incompletos são raros, e outras configurações são tipicamente mais favoráveis, incluindo a ligação com íons adicionais como no caso de FB3 .
Exemplo: \(BF_3\)
Desenhar a estrutura de Lewis para trifluoreto de boro (BF3).
Solução
1. Adicionar electrões (3*7) + 3 = 24
2. Desenhar conectividades:
3. Adicionar octetos aos átomos exteriores:
4. Adicionar electrões extra (24-24=0) ao átomo central:
5. O electrão central tem octeto?
- NO. Tem 6 elétrons
- Adicionar uma ligação múltipla (ligação dupla) para ver se o átomo central pode alcançar um octeto:
6. O Boro central agora tem um octeto (haveria três estruturas Lewis de ressonância)
No entanto…
- Nesta estrutura com dupla ligação o átomo flúor está compartilhando elétrons extras com o boro.
- O flúor teria uma carga parcial ‘+’, e o boro uma carga parcial ‘-‘, isto é inconsistente com as eletronegatividades do flúor e do boro.
- Assim, a estrutura de BF3, com ligações simples, e 6 elétrons de valência ao redor do boro central é a estrutura mais provável
- BF3 reage fortemente com compostos que têm um par de elétrons não partilhados que podem ser usados para formar uma ligação com o boro:




