Az oktett-szabály megsértése
2. kivétel: Nem teljes oktett
A második kivétel az oktett-szabály alól az, amikor túl kevés valenciaelektron van, ami nem teljes oktettet eredményez. Még több olyan eset van, amikor az oktett-szabály nem a leghelyesebb ábrázolást adja egy molekuláról vagy ionról. Ilyen eset a hiányos oktett is. A nem teljes oktettekkel rendelkező fajok meglehetősen ritkák, és általában csak néhány berillium-, alumínium- és bórvegyületben fordulnak elő, beleértve a bórhidrideket is. Nézzünk meg egy ilyen hidridet, az \(BH_3\) (bórán).
Ha az \(BH_3\) Lewis-szerkezetét a Lewis-szerkezetek rajzolásának alapvető stratégiáit követve elkészítenénk, valószínűleg ezt a szerkezetet kapnánk (3. ábra):
A probléma ezzel a szerkezettel az, hogy a bórnak hiányos a nyolcadrendszere; csak hat elektron veszi körül. A hidrogénatomok természetesen csak 2 elektronnal rendelkezhetnek a legkülső héjukban (a nyolcas változatukban), és így nincsenek tartalék elektronok ahhoz, hogy kettős kötést alakítsanak ki a bórral. Feltételezhetjük, hogy mivel ez a szerkezet nem képes teljes oktetteket képezni, ez azt jelenti, hogy ennek a kötésnek nem kovalens, hanem ionos kötésnek kell lennie. A bór elektronegativitása azonban nagyon hasonló a hidrogénéhez, ami azt jelenti, hogy a hidrogén és a bór közötti kötésnek valószínűleg nagyon kevés ionos jellege van, és így ez a Lewis-szerkezet, bár nem teljesíti a nyolcas szabályt, valószínűleg a lehető legjobb szerkezet a BH3 Lewis elmélettel történő ábrázolására. A BH3 hiányos oktettjét többek között az is magyarázhatja, hogy a BH3 általában átmeneti faj, amely több lépésből álló reakciókban átmenetileg keletkezik.
Nézzünk meg egy másik hiányos oktett helyzetet, amely a bórral, a BF3 (bór-trifluorin) bórral foglalkozik. A BH3-hoz hasonlóan a BF3 Lewis-szerkezetének kezdeti rajzolásakor olyan szerkezetet kapunk, amelyben a bór csak hat elektron veszi körül (4. ábra).
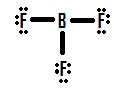
Ha megnézzük a 4. ábrát, láthatjuk, hogy a fluoratomok extra magányos párokkal rendelkeznek, amelyeket felhasználhatnak további kötések kialakítására a bórral, és azt gondolhatnánk, hogy csak egy magányos párt kell kötéssé alakítani, és a szerkezet helyes lesz. Ha a bór és az egyik fluor között egy kettős kötést adunk hozzá, akkor a következő Lewis-szerkezetet kapjuk (5. ábra):
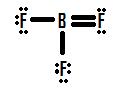
Minden fluoratomnak nyolc elektronja van, és a bóratomnak is nyolc! Minden atomnak tökéletes nyolctagja van, igaz? Nem olyan gyorsan. Meg kell vizsgálnunk ennek a szerkezetnek a formális töltéseit. A bórral kettős kötést osztó fluort hat elektron veszi körül (négy a két magányos elektronpárjából és egy-egy a bórral való két kötéséből). Ez eggyel kevesebb elektron, mint ahány valenciaelektronja természetes módon lenne (a hetedik csoportba tartozó elemeknek hét valenciaelektronjuk van), ezért formális töltése +1. A bórral közös egyszerű kötésen osztozó két flourin körül hét elektron van (hat a három magányos párjukból és egy a bórral való egyszerű kötésükből). Ez ugyanannyi, mint ahány valenciaelektronjuk lenne önmagukban, így mindkettő formális töltése nulla. Végül a bórnak négy elektronja van körülötte (egy-egy a fluorral közös négy kötéséből). Ez eggyel több elektron, mint ahány valenciaelektronja lenne a bórnak önmagában, és így a bór formális töltése -1.
Ezt a szerkezetet támasztja alá az a tény, hogy a BF3-ban a bór-fluor kötések kísérletileg meghatározott kötéshossza kisebb, mint ami egy egyszerű kötésre jellemző lenne (lásd kötésrend és kötéshossz). Ez a szerkezet azonban ellentmond a formális töltések egyik fő szabályának: Az 5. ábrán látható szerkezetben azonban pozitív formális töltés található a fluoron, amely nemcsak a szerkezetben, hanem az egész periódusos rendszerben is a legelektronegatívabb elem (\(\chi=4,0\)). A bór viszont, amelynek elektronegativitása sokkal kisebb, 2,0, negatív formális töltéssel rendelkezik ebben a szerkezetben. Ez a formális töltés-elektronegativitás eltérés lehetetlenné teszi ezt a kettős kötésű szerkezetet.
A nagy elektronegativitás különbség azonban itt, szemben a BH3-mal, jelentős poláris kötéseket jelent a bór és a fluor között, ami azt jelenti, hogy ez a molekula magas ionos jelleget mutat. Ez egy olyan félionos szerkezet lehetőségét sugallja, mint amilyen a 6. ábrán látható:

A három szerkezet egyike sem a “helyes” szerkezet ebben az esetben. A legvalószínűbb “helyes” szerkezet valószínűleg mindhárom szerkezet rezonanciája: a hiányos oktett (4. ábra), a kettős kötés (5. ábra) és az ionos kötés (6. ábra). A leginkább hozzájáruló szerkezet valószínűleg a nem teljes oktett szerkezet (mivel az 5. ábra gyakorlatilag lehetetlen, a 6. ábra pedig nem felel meg a BF3 viselkedésének és tulajdonságainak). Mint látható, még akkor is, ha más lehetőségek is léteznek, a hiányos oktettszerkezetek ábrázolhatják a legjobban a molekulaszerkezetet.
Mellékletként fontos megjegyezni, hogy a BF3 gyakran kötődik egy F-ionhoz, hogy BF4-et képezzen, ahelyett, hogy BF3-ként maradna. Ez a szerkezet teszi teljessé a bór oktettjét, és ez a természetben gyakoribb. Ez jól példázza azt a tényt, hogy a nem teljes oktett ritka, és más konfigurációk jellemzően kedvezőbbek, beleértve a további ionokkal való kötést, mint a BF3 esetében .
Példa: \(BF_3\)
Rajzoljuk meg a bórtrifluorid (BF3) Lewis-szerkezetét.
Solution
1. Adjunk hozzá elektronokat (3*7) + 3 = 24
2. Rajzoljunk kapcsolódási pontokat:
3. Adjunk oktetteket a külső atomokhoz:
4. Adjunk plusz elektronokat (24-24=0) a központi atomhoz:
5. Adjunk hozzá plusz elektronokat (24-24=0) a központi atomhoz:
5. Van-e a központi elektronnak oktettje?
- NEM. Van 6 elektronja
- Adjunk hozzá egy többszörös kötést (kettős kötés), hogy lássuk, a központi atom elérheti-e az oktettet:
6. A központi bórnak most már oktettje van (három rezonancia Lewis szerkezet lenne)
Mégis…
- Egy kettős kötéssel rendelkező szerkezetben a fluoratom extra elektronokat oszt meg a bórral.
- A fluornak “+” parciális töltése lenne, a bórnak pedig “-” parciális töltése, ez nincs összhangban a fluor és a bór elektronegativitásával.
- Ezért a BF3 szerkezete, egyszerű kötésekkel és 6 valenciaelektronnal a központi bór körül a legvalószínűbb szerkezet
- A BF3 erősen reagál olyan vegyületekkel, amelyeknek van egy osztatlan elektronpárjuk, amely felhasználható a bórral való kötés kialakítására:




