Brott mot oktettregeln
Exception 2: Ofullständiga oktetter
Det andra undantaget från oktettregeln är när det finns för få valenceelektroner vilket resulterar i en ofullständig oktett. Det finns ännu fler tillfällen då oktettregeln inte ger den mest korrekta avbildningen av en molekyl eller jon. Detta är också fallet med ofullständiga oktetter. Arter med ofullständiga oktetter är ganska sällsynta och förekommer i allmänhet endast i vissa beryllium-, aluminium- och borföreningar, inklusive borhydriderna. Låt oss ta en titt på en sådan hydrid, \(BH_3\) (boran).
Om man skulle göra en Lewisstruktur för \(BH_3\) enligt de grundläggande strategierna för att rita Lewisstrukturer skulle man troligen få fram den här strukturen (figur 3):
Problemet med denna struktur är att bor har en ofullständig oktett; den har bara sex elektroner runt omkring sig. Väteatomer kan naturligtvis bara ha endast två elektroner i sitt yttersta skal (deras version av en oktett), och därför finns det inga extra elektroner för att bilda en dubbelbindning med bor. Man skulle kunna anta att det faktum att denna struktur inte kan bilda kompletta oktetter måste innebära att denna bindning borde vara jonisk i stället för kovalent. Bor har dock en elektronegativitet som är mycket lik väte, vilket innebär att det sannolikt finns mycket lite jonisk karaktär i bindningarna mellan väte och bor, och därför är denna Lewisstruktur, även om den inte uppfyller oktettregeln, sannolikt den bästa möjliga strukturen för att avbilda BH3 med hjälp av Lewis-teorin. En av de saker som kan förklara BH3:s ofullständiga oktett är att det vanligen är en övergående art, som bildas tillfälligt i reaktioner som innefattar flera steg.
Låt oss ta en titt på en annan ofullständig oktett-situation som handlar om bor, BF3 (Boron trifluorine). Precis som med BH3 kommer den inledande ritningen av en Lewisstruktur av BF3 att bilda en struktur där boret bara har sex elektroner runt omkring sig (figur 4).
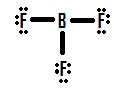
Om man tittar på figur 4 kan man se att fluoratomerna besitter extra ensamma par som de kan använda för att göra ytterligare bindningar med boret, och man skulle kunna tänka sig att det räcker med att göra ett ensamt par till en bindning för att strukturen ska bli korrekt. Om vi lägger till en dubbelbindning mellan bor och en av fluorinerna får vi följande Lewisstruktur (figur 5):
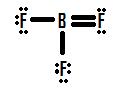
Varje fluor har åtta elektroner, och boratomen har också åtta! Varje atom har en perfekt oktett, eller hur? Inte så snabbt. Vi måste undersöka de formella laddningarna i denna struktur. Fluoret som delar en dubbelbindning med boret har sex elektroner runt omkring sig (fyra från dess två ensamma elektronpar och en vardera från dess två bindningar med boret). Detta är en elektron mindre än det antal valenceelektroner som den skulle ha naturligt (grundämnen i grupp sju har sju valenceelektroner), så den har en formell laddning på +1. De två flouriner som delar enkelbindningar med bor har sju elektroner omkring sig (sex från deras tre ensamstående par och en från deras enkelbindningar med bor). Detta är lika mycket som antalet valenceelektroner som de skulle ha på egen hand, så de har båda en formell laddning på noll. Bor slutligen har fyra elektroner runt omkring sig (en från var och en av dess fyra bindningar som delas med fluor). Detta är en elektron mer än det antal valenselektroner som bor skulle ha på egen hand, och därför har bor en formell laddning på -1.
Denna struktur stöds av det faktum att den experimentellt bestämda bindningslängden för bindningarna mellan bor och fluor i BF3 är mindre än vad som skulle vara typiskt för en enkelbindning (se Bindningsordning och bindningslängder). Denna struktur motsäger dock en av de viktigaste reglerna för formella laddningar: Negativa formella laddningar ska finnas på de mer elektronegativa atomerna i en bindning, men i den struktur som visas i figur 5 finns en positiv formell laddning på fluor, som inte bara är det mest elektronegativa elementet i strukturen, utan det mest elektronegativa elementet i hela det periodiska systemet (\(\chi=4,0\)). Bor å andra sidan, med en mycket lägre elektronegativitet på 2,0, har den negativa formella laddningen i denna struktur. Denna oenighet mellan formell laddning och elektronegativitet gör denna dubbelbundna struktur omöjlig.
Den stora skillnaden i elektronegativitet här, till skillnad från i BH3, innebär dock betydande polära bindningar mellan bor och fluor, vilket innebär att det finns en hög jonisk karaktär i denna molekyl. Detta tyder på möjligheten av en semi-jonisk struktur som den som ses i figur 6:

Ingen av dessa tre strukturer är den ”korrekta” strukturen i detta fall. Den mest ”korrekta” strukturen är sannolikt en resonans av alla tre strukturerna: den med den ofullständiga oktetten (figur 4), den med dubbelbindningen (figur 5) och den med jonbindningen (figur 6). Den mest bidragande strukturen är förmodligen den ofullständiga oktettstrukturen (på grund av att figur 5 är i princip omöjlig och att figur 6 inte stämmer överens med BF3:s beteende och egenskaper). Som man kan se även när andra möjligheter finns kan ofullständiga oktetter bäst skildra en molekylär struktur.
Som en sidobemärkning är det viktigt att notera att BF3 ofta binder sig med en F-jon för att bilda BF4- i stället för att stanna kvar som BF3. Denna struktur fullbordar borets oktett och är vanligare i naturen. Detta exemplifierar det faktum att ofullständiga oktetter är sällsynta, och andra konfigurationer är vanligtvis mer gynnsamma, inklusive bindning med ytterligare joner som i fallet BF3 .
Exempel: \(BF_3\)
Rita Lewisstrukturen för bortrifluorid (BF3).
Lösning
1. Lägg till elektroner (3*7) + 3 = 24
2. Rita konnektiviteter:
3. Lägg till oktetter till de yttre atomerna:
4. Lägg till extra elektroner (24-24=0) till den centrala atomen:
5. Har den centrala elektronen en oktett?
- NO. Den har 6 elektroner
- Lägg till en multipelbindning (dubbelbindning) för att se om den centrala atomen kan uppnå en oktett:
6. Den centrala boronen har nu en oktett (det skulle finnas tre resonans-Lewis-strukturer)
Hursomhelst…
- I den här strukturen med en dubbelbindning delar fluoratomen extra elektroner med boronen.
- Fluoret skulle ha en ”+” partiell laddning och boret en ”-” partiell laddning, detta är oförenligt med fluorets och borets elektronegativitet.
- Därmed är BF3:s struktur med enkla bindningar och 6 valenselektroner runt det centrala boret den mest sannolika strukturen
- BF3 reagerar starkt med föreningar som har ett odelat elektronpar som kan användas för att bilda en bindning med boret:




