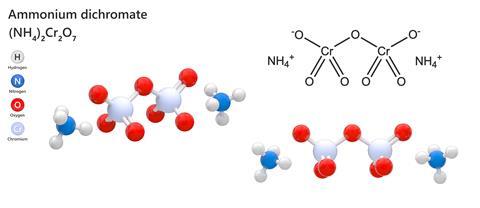
Ammoniumdichromat
Meera Senthilingam
In dieser Woche erinnert sich Brian Clegg an eine einfache, aber explosive Verbindung.
Brian Clegg
Von allen chemischen Verbindungen, die man in den alten Zeiten, als noch nicht alles auf Gesundheit und Sicherheit ausgerichtet war, in einem Chemiebaukasten finden konnte, war Ammoniumdichromat in seiner Einfachheit vielleicht die befriedigendste. Diese relativ komplexe anorganische Verbindung verbindet zwei Ammoniumionen mit dem doppelt negativ geladenen Cr2O7 zu einem recht attraktiven orangefarbenen Kristall, der so harmlos aussieht wie Kupfersulfat. Wenn man ihn jedoch anzündet – was bei einer kristallinen Substanz erstaunlich einfach ist -, spuckt er große Mengen federartigen, dunkelgrünen Chromoxidpulvers mit einer Vielzahl leuchtend orangefarbener Funken und einer so beeindruckenden Kraft aus, dass man ihm den Spitznamen „Vesuvfeuer“ gegeben hat. Vergessen Sie Modellvulkane, die mit Natriumbikarbonat und Essig betrieben werden, ein Ammoniumdichromat-Vulkan ist das einzig Wahre.

Quelle: ©
Um der Chemiepolizei gegenüber fair zu sein: Ammoniumdichromat ist reizend, giftig, mit ziemlicher Sicherheit krebserregend und kann explodieren, wenn es in einem geschlossenen Behälter erhitzt wird. Die Kristallstruktur ist thermodynamisch instabil, so dass bei Auslösung einer Flamme oder ausreichender Hitze eine exotherme Reaktion einsetzt, die zu einer starken Volumenausdehnung führt, wenn sich der größte Teil, aber nicht das gesamte Dichromat in das Oxid umwandelt. Dabei wird Stickstoff freigesetzt, und die Reaktion wird manchmal in Laboratorien genutzt, um reineren Stickstoff zu erzeugen, der nicht ohne weiteres aus der Luft extrahiert werden kann.
Die Verbindung beginnt als das natürlich vorkommende Mineral Chromit, FeCr2O4, das in einem Ofen mit Natriumhydroxid und Kalziumoxid geröstet wird, um Natriumchromat herzustellen. Der Hauptzweck dieses Verfahrens ist die Herstellung von basischem Chromsulfat, das für die Ledergerberei unerlässlich ist, aber ein Teil wird über Natriumdichromat verarbeitet, um das Ammoniumsalz zu erzeugen.
Industriell ist Ammoniumdichromat so etwas wie eine „Verbindung von gestern“. In den Anfängen der Fotografie gehörte es zu einer Reihe von – meist gefährlichen – chemischen Stoffen, die zur Aufnahme eines Bildes verwendet wurden. Die direkteste Anwendung war die Gummibichromat-Fotografie (Bichromat ist nur ein älterer, alternativer Begriff für Dichromat).
Ammoniumdichromat wird immer ein bisschen ein Angeber sein, eine Verbindung, die immer für Aufregung und Aufregung sorgen wird
Das Verfahren geht auf die 1850er Jahre zurück und erzeugt Abzüge, die vollfarbig oder monochrom sein können. Dabei wird das Papier mit einer Mischung aus Pigmenten – in der Regel Aquarellfarben – und Gummi arabicum, dem Saft des Akazienbaums, beschichtet, wobei einige moderne Anwender das Gummi durch PVA-Kleber ersetzen. Die Schicht wird dann mit Ammonium- (und manchmal Kalium-) Dichromat behandelt, das sie lichtempfindlich macht und das Gummi oxidiert, um das Pigment dort zu halten, wo es auf das Licht trifft. Nach der Belichtung mit einem Bild (durch einen Farbfilter, wenn ein volles Farbergebnis gewünscht ist) wird die Schicht mit Wasser gewaschen, wodurch die Pigmente, die nicht belichtet wurden, entfernt werden. Um zusätzliche Farben hinzuzufügen, wird der Vorgang in Schichten mit verschiedenen Pigmenten wiederholt, wodurch ein eindrucksvolles, eher malerisches Bild als eine herkömmliche Fotografie entsteht.
Gummibichromat wird heute nur noch von spezialisierten Enthusiasten verwendet, ebenso wie eine andere fotografische Verwendung von Ammoniumdichromat, der Cyanotypie-Sonnendruck. Hier wird die Verbindung mit Ammoniumeisenoxalat und Kaliumferricyanid gemischt und in Papier eingeweicht. Sobald das Papier trocknet, ist es lichtempfindlich und färbt sich bei Sonneneinstrahlung blau. Die Bilder werden in der Regel durch teilweises Abdecken des Papiers mit Gegenständen erzeugt, um negative Schatten zu erzeugen.
Auch wenn es heute kaum noch verwendet wird, hat die pyrotechnische Industrie Ammoniumdichromat in einige ihrer Feuerwerkskörper eingearbeitet, und zwar sowohl allein in frühen Indoor-Feuerwerkskörpern (bevor es als zu gefährlich angesehen wurde) als auch in einer Mischung, die als Oxidationsmittel und expandierendes Treibmittel dient.
Quelle: ©
Der gleiche allmähliche Rückzug aus der Verwendung ist bei einer anderen Anwendung von Ammoniumdichromat zu beobachten. Dichromate erwiesen sich als wirksame Beizmittel in der Färberei. Ursprünglich war ein Beizmittel eine Schließe oder die Schnalle eines Gürtels – etwas, das festhält – und der Begriff wurde auf die Färbereiindustrie übertragen, wo man eine Möglichkeit suchte, Farbstoffe an Materialien festzuhalten, die sie von Natur aus abstoßen. Das Beizmittel fungiert als eine Art Vermittler, der mit dem Farbstoff einen Komplex bildet, der sich mit einer Faser des Stoffes verbindet. Da es andere ebenso wirksame, aber weniger gefährliche Beizmittel gibt, wird Ammoniumdichromat heute nur noch selten verwendet.
Eine letzte Anwendung, die viel schneller verschwand als das Beizmittel, war die Unterstützung bei der Herstellung von Bildschirmen für Fernseher und Computer. Das Dichromat wurde in einem ähnlichen Verfahren wie in der Gummibichromat-Fotografie verwendet, um Cluster des phosphoreszierenden Materials als Pixel auf dem Bildschirm anzubringen. Die Oberfläche wurde mit dem Gemisch beschichtet und dann mit einer Schattenmaske belichtet, die das Muster der Punkte auf dem Bildschirm erzeugte, bevor das Zwischenmaterial abgewaschen wurde. Aber die Einführung von LCD-, Plasma- und LED-Bildschirmen hat den Markt, auf dem Ammoniumdichromat seine letzte Hightech-Anwendung hatte, praktisch zerstört, so dass Bildschirme auf Phosphorbasis nur noch eine Rarität für Fachleute sind.
Wir müssen akzeptieren, dass Ammoniumdichromat trotz der scheinbar unschuldigen Schönheit dieser glitzernden orangefarbenen Kristalle zu unsicher ist, um ein Spielzeug zu sein. Aber unter kontrollierten Bedingungen kann diese sprudelnde Vulkanreaktion auch dem zynischsten Chemiker ein breites Grinsen ins Gesicht zaubern. Ammoniumdichromat wird immer ein bisschen ein Angeber sein, eine Verbindung, die immer für Aufregung und Aufregung sorgen wird.
Meera Senthilingam
Wissenschaftsautor Brian Clegg über die vulkanische Chemie von Ammoniumdichromat. Nächste Woche geht es um den Stoffwechsel.
Nate Adams
Die Gruppe der Cytochrom-p450-Proteine ist wahrscheinlich die wichtigste molekulare Maschine in unseren Zellen. Sie sind die Enzyme, die den Prozess des Abbaus oder der Verstoffwechselung von normalerweise giftigen oder gefährlichen Molekülen einleiten, die unser Körper nicht will oder nicht mehr braucht.
Meera Senthilingam
Und entdecken Sie die Chemie, die dahinter steckt, indem Sie Nate Adams in der nächsten Woche in Chemie in ihrem Element begleiten. Bis dahin, danke fürs Zuhören, ich bin Meera Senthilingam.




