PANS e PANDAS Diagnóstico e Tratamento
PANS e PANDAS são diagnósticos clínicos e baseados em se os sintomas apresentam os critérios diagnósticos, conforme estabelecido pelo National Institute of Mental Health (NIMH). O reconhecimento do PANS/PANDAS pode ser um desafio mesmo para os clínicos mais qualificados. Muito frequentemente, crianças e adolescentes são erroneamente diagnosticados como tendo uma doença mental, quando na verdade, eles têm uma doença auto-imune, desencadeada por uma infecção.
Cunningham Panel™ Assiste Clínicos no Diagnóstico de PANS e PANDAS
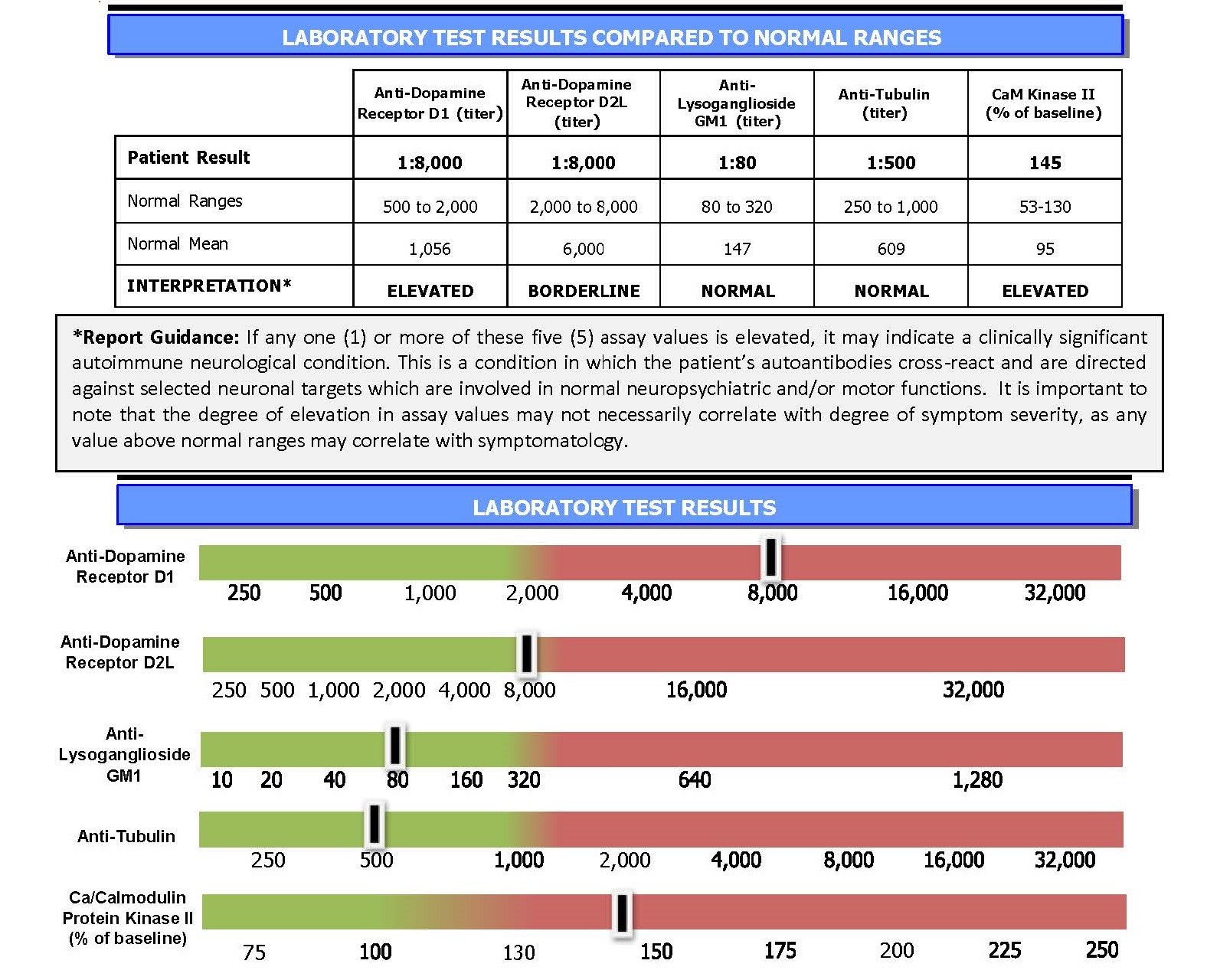

O Painel de testes de Cunningham pode ajudar os clínicos a fazer o diagnóstico correto. O Painel fornece informações sobre como o sistema imunológico de uma criança está funcionando. Especificamente, o teste mede os níveis de certos auto-anticorpos (responsáveis por causar os sintomas) que circulam na corrente sanguínea de uma criança. Quanto maiores forem os níveis, maior a probabilidade de que os comportamentos psiquiátricos e neurológicos do paciente sejam devidos a uma infecção.
Estas condições neurológicas auto-imunes tratáveis compartilham muitas semelhanças na apresentação dos sintomas, mas os critérios diagnósticos e a etiologia por trás de cada um diferem. O PANDAS é desencadeado por uma infecção por Strep, enquanto o PANS é causado pela exposição a uma série de infecções, incluindo a gripe, sinusite, micoplasma pneumonia e doença de Lyme.
Características do PANS e PANDAS
PANDAS é caracterizado por um início súbito e dramático do TOC e/ou tiques após uma infecção por Strep em crianças pré-pubescentes. Para atender aos critérios diagnósticos, um paciente também deve apresentar anormalidades neurológicas (hiperatividade motora ou movimentos coreiformes). Embora não faça parte dos critérios, a presença de sintomas neuropsiquiátricos co-mórbidos é universal em crianças com PANDAS. PANDAS Diagnostic Criteria
Os traços característicos do PANS incluem um início abrupto do TOC ou uma severa restrição alimentar, em conjunto com o início agudo de vários sintomas neuropsiquiátricos descritos nos critérios NIMH. Não há critérios de idade para PANS, porém a maioria dos pacientes tem um início de doença durante seus anos de idade escolar. Critérios Diagnósticos PANS
Tratamento de PANS e PANDAS
PANS e tratamento PANDAS inclui a erradicação do agente infeccioso subjacente e a redução da resposta imunológica que tem sido relatada para causar os sintomas neuropsiquiátricos. Em alguns casos, o desafio está em identificar corretamente o agente infeccioso específico.


PANS pode ser desencadeado por uma série de infecções, incluindo Borrelia burgdorferi (doença de Lyme), mycoplasma pneumonia, herpes simples, resfriado comum e vírus varicela.1-5 Independentemente disso, os sintomas são causados pela reação do sistema imunológico à infecção.6,7
Estudos encontraram vários tratamentos PANDAS eficazes que podem resultar na rápida resolução dos sintomas, incluindo terapia antibiótica, troca de plasma (plasmaférese) e tratamentos com imunoglobulina intravenosa (IVIG).8,9 Outras terapias de suporte incluem medicamentos antidepressivos (ISRS) e terapia cognitiva comportamental (CBT).
Resolução dos sintomas de PANDAS tem sido mostrada em estudos

A eficácia no tratamento de infecções por estreptococos do grupo A, com subsequente resolução dos sintomas de PANDAS, tem sido demonstrada em vários estudos. Um estudo relatou a resolução confirmada dos sintomas e tiques do TOC após o tratamento com antibióticos e subseqüente cultura negativa da garganta em pacientes com estreptococos do grupo A.10
E, há algumas crianças que são definidas como portadoras de estreptococos do grupo A e são assintomáticas, sem sinais de amigdalofaringite. Estes indivíduos podem continuar a gerar os anticorpos relacionados com estreptococos e os organismos que abrigam na nasofaringe.11,12,13
A Rede de Médicos PANDAS fornece uma lista mais abrangente de opções de tratamento.
Referências de Literatura
- Dale RC, Church AJ, Heyman I. Encefalite estriatal após infecção por varicela zoster complicada pelo Tourettismo. Distúrbios do movimento : revista oficial da Movement Disorder Society. Dez 2003;18(12):1554-1556.
- Fallon BA, Nields JA, Parsons B, Liebowitz MR, Klein DF. Manifestações psiquiátricas da borreliose de Lyme. The Journal of clinical psychiatry. Jul 1993;54(7):263-268.
- Muller N, Riedel M, Blendinger C, Oberle K, Jacobs E, Abele-Horn M. Mycoplasma pneumoniae infection and Tourette’s syndrome. Pesquisa psiquiátrica. Dez 15 2004;129(2):119-125.
- Hoekstra PJ, Manson WL, Steenhuis MP, Kallenberg CG, Minderaa RB. Associação de constipação comum com exacerbações em pacientes pediátricos mas não adultos com transtorno do tique: um estudo prospectivo longitudinal. Revista de psicofarmacologia infantil e adolescente. Abr 2005;15(2):285-292.
- Mink J, Kurlan R. Acute postinfectious movement and psychiatric disorders in children and adolescents. Journal of child neurology. Fev 2011;26(2):214-217.
- Kirvan CA, Swedo SE, Heuser JS, Cunningham MW. Mimicry e sinalização celular neuronal mediada por autoanticorpos na coréia de Sydenham. Medicina da natureza. Jul 2003;9(7):914-920.
- Kirvan CA, Swedo SE, Snider LA, Cunningham MW. Sinalização celular neuronal mediada por anticorpos em distúrbios de comportamento e movimento. Journal of neuroimmunology. Out 2006;179(1-2):173-179.
- Perlmutter SJ, Leitman SF, Garvey MA, et al. Troca terapêutica de plasma e imunoglobulina intravenosa para distúrbios obsessivo-compulsivos e distúrbios de carrapatos na infância. Lanceta. Oct 2 1999;354(9185):1153-1158.
- Nicolson R, Swedo SE, Lenane M, et al. Um estudo aberto da troca plasmática na infância – transtorno obsessivo-compulsivo sem exacerbações póstreptococócicas. Journal of the American Academy of Child and Adolescent Psychiatry. Out 2000;39(10):1313-1315.
- Murphy ML, Pichichero ME. Potencial identificação e tratamento de crianças com distúrbio neuropsiquiátrico autoimune pediátrico associado a infecção estreptocócica do grupo A (PANDAS). Arquivos de pediatria & medicina da adolescência. Abr 2002;156(4):356-361.
- Cleary PP, Zhang Y, Park HS. Tecido linfóide nasal associado &Células M, uma janela para infecções estreptocócicas persistentes. A revista indiana de pesquisa médica. Maio 2004;119 Suppl:57-60.
- Wang B, Li S, Southern PJ, Cleary PP. Modulação estreptocócica da invasão celular através da sinalização TGF-beta1. Anais da Academia Nacional de Ciências dos Estados Unidos da América. Fev 14 2006;103(7):2380-2385.
- Sela S, Neeman R, Keller N, Barzilai A. Relação entre o transporte assintomático de Streptococcus pyogenes e a capacidade das estirpes de aderir e ser interiorizadas por células epiteliais cultivadas. Diário de microbiologia médica. Jun 2000;49(6):499-502.




